Vankomicin
| Vankomicin | |
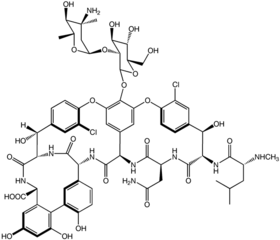
| |
| Azonosítás | |
|---|---|
| N o CAS | |
| N o ECHA | 100,014,338 |
| N o EC | 215-772-6 |
| ATC kód | A07 , J01 |
| DrugBank | DB00512 |
| PubChem | 14969 |
| Mosolyok |
CC1C (C (CC (O1) OC2C (C (C (OC2OC3 = C4C = C5C = C3OC6 = C (C = C (C = C6)) C (C (C (= O) NC (C (= O) NC5C ( = O) NC7C8 = CC (= C (C = C8) O) C9 = C (C = C (C = C9C (NC (= O) C (C (C1 = CC (= C (O4) C = C1)) ) Cl) O) NC7 = O) C (= O) O) O) O) CC (= O) N) NC (= O) C (CC (C) C) NC) O) Cl) CO) O) O) (C) N) O , |
| InChI |
InChI: InChI = 1 / C66H75Cl2N9O24 / c1-23 (2) 12-34 (71-5) 58 (88) 76-49-51 (83) 26-7-10-38 (32 (67) 14- 26) 97-40-16-28-17-41 (55 (40) 101-65-56 (54 (86) 53 (85) 42 (22-78) 99-65) 100-44-21-66 ( 4.70) 57 (87) 24 (3) 96-44) 98-39-11-8-27 (15-33 (39) 68) 52 (84) 50-63 (93) 75-48 (64 (94) 95) 31-18-29 (79) 19-37 (81) 45 (31) 30-13-25 (6-9-36 (30) 80) 46 (60 (90) 77-50) 74-61 ( 91) 47 (28) 73-59 (89) 35 (20-43 (69) 82) 72-62 (49) 92 / h6-11,13-19,23-24,34-35,42, 44,46- 54,56-57,65,71,78-81,83-87H, 12,20-22,70H2,1-5H3, (H2,69,82) (H, 72,92) (H, 73,89) (H, 74,91) (H, 75,93) (H, 76,88) ( H, 77,90) (H, 94,95) / t24-, 34 +, 35-, 42 +, 44-, 46 +, 47 +, 48-, 49 +, 50-, 51 +, 52 +, 53 +, 54 -, 56 +, 57 +, 65-, 66- / m0 / s1 / f / h72-77,94H, 69H2 |
| Megjelenés | Szilárd |
| Kémiai tulajdonságok | |
| Brute formula |
C 66 H 75 Cl 2 N 9 O 24 [izomerek] |
| Moláris tömeg | 1449,254 ± 0,071 g / mol C 54,7%, H 5,22%, Cl 4,89%, N 8,7%, O 26,5%, |
| Ökotoxikológia | |
| DL 50 |
430 mg · kg -1 egér iv 5000 mg · kg -1 egér sc 1734 mg · kg -1 egér ip |
| Farmakokinetikai adatok | |
| Biológiai hozzáférhetőség | ~ 0% szóban |
| Anyagcsere | Nem metabolizálódik |
| Felezési ideje eliminálódik. | 4-11 óra (felnőttek) 6-10 óra (veseelégtelenség) |
| Kiválasztás | |
| Terápiás szempontok | |
| Terápiás osztály | Glikopeptid antibiotikum |
| Az alkalmazás módja | Intravénás |
| Terhesség | Lehet használni , ha szükséges |
| Egység SI és STP hiányában. | |
A vancomycin egy antibiotikum a család glükopeptidek . Terjedelmes ( 1500 a 2000 dalton ) és összetett, ez a molekula, mint a β-laktámok , inhibitor peptidoglikán szintézisének a bakteriális fal (azaz, ez elpusztítja a baktériumokat úgy, hogy megelőzi az épület a borítékba).
Nagy súlya miatt azonban nem tudja kölcsönadni a Gram-negatív baktériumok külső membránjának pórusait ( porinjait ) . Hatásspektruma ezért csak Gram-pozitívra korlátozódik . A vankomicin baktericid hatású , de ez a baktericid lassan jelenik meg; annak biológiai hozzáférhetősége a szájon át elhanyagolható, az intravénás út Ezért szükség van az összes jelzések egy kivételével, a szájon át történő kezelésére álhártyás vastagbélgyulladás . A fő mellékhatások a vese- és halláskárosodás, ezért a plazma vankomicinszint rendszeres ellenőrzése indokolt. Végül, költsége nem elhanyagolható, és gyakran a legvégső megoldás.
Számos antibiotikum-rezisztencia előfordulása után a vankomicin 2.0 változata, majd a vankomicin 3.0. (2017) fejlesztették ki. A 3. verzió három különböző antibiotikum tulajdonságot ötvöz ugyanazon molekulában, ami megnehezíti a baktériumok számára a rezisztencia kialakulását. 2017-ben a gyártó bejelentette, hogy 25 000-szer erősebb, mint az előző.
A glikopeptidek javallatai
Kúrában a következő helyzetekre korlátozódnak:
- β-laktámokkal szemben rezisztens baktériumok súlyos fertőzései , vagy ha a beteg allergiás rájuk;
- Clostridium difficile pseudomembranosus colitis .
Két megelőző helyzet lehetséges:
- a bakteriális endocarditis antibiotikus profilaxisa kockázatos szívbetegségben szenvedő, β-laktámokra allergiás és kockázatos eljáráson áteső betegeknél ;
- A műtéti fertőzések antibiotikus profilaxisa műtétekben staph kockázat (szívműtét, érrendszeri, ortopédiai, idegsebészeti műtétek), olyan esetekben, amikor a meticillinnel szemben rezisztens Staphylococcus fertőzés megnövekedett (különösen a korai revízió műtétje), vagy a β-laktámokra allergiás betegeknél .
Hatásspektrum
A vankomicin ezért csak a gram-pozitívokra gyakorolja hatását :
- a staphylococcusok , például a Staphylococcus aureus vagy a koaguláz-negatív staphylococcusok, még a meticillinnel szemben is rezisztensek . Az ellenállás továbbra is kivételes;
- bármilyen típusú streptococcus , ideértve a penicillin iránti csökkent érzékenységű törzseket is ;
- az enterococcusok . Humán klinikákon azonban találkozhatunk glikopeptidekkel szemben rezisztens enterococcus törzsekkel (különösen az E. faeciumban );
- Gram-pozitív szigorú anaerobok : anaerob kokkok, Clostridium ( C perfringens és C difficile ). Az orális vankomicin aktív a C difficile pseudomembranosus colitisben ;
- Listeria monocytogen: bakteriosztatikus aktivitás in vitro, de a vankomicin diffúziója véletlenszerű a cerebrospinalis folyadékban, amikor az agyhártya gyulladt; klinikailag ezeket az agyhártyagyulladásokat ampicillinnel kezelik , és még akkor is, ha az agyhártyagyulladás kezelésének kezdetén az empirikus kezelés már tartalmaz IV vankomicint, ampicillint adunk hozzá, ha a körülmények (idős beteg vagy immunszuppresszált például) a Listeriát okozzák ügynök.
Farmakodinamika
Ami a β-laktámokat illeti , a vankomicin a baktériumfal peptidoglikán szintézisének gátlója. Hatásmechanizmusa azonban más: a lipopeptid prekurzorok peptidil-D-Ala-D-Ala végeihez kötődik, amikor azok a citoplazmatikus membránból kilépve, azon áthaladva, és így gátolják a transzglikozilezési és transzpeptidációs lépéseket, a peptidoglikán jó szintézise, a transzpeptidáz későbbi hatása (amely katalizálja a terminális D-Ala eltávolítását és a peptidoglikán térhálósítását).
Prózai szempontból úgy működik, hogy a Gram-pozitív baktériumok falának összetevőihez kötődik, és ez utóbbiak lebomlását okozza.
Farmakokinetika
- Az orális biohasznosulás elhanyagolható. A parenterálisan , intravénás beadása adagja 1 g teszi lehetséges, két órával az injekció után, átlagos szérum szintek 25 ug · ml -1 . A 11 -én óra, a koncentráció 3 , hogy 12- mikrogramm · ml -1 .
- A plazmafehérjéhez való kötődés terápiás koncentrációban 30-60%.
- A szérum felezési ideje, amely egyénenként nagyon eltérő, 4–11 óra.
- A vankomicin diffúziója jó a pleurális, szinoviális, peritonealis és pericardialis folyadékokban; másrészt nulla a cerebrospinális folyadékban, amikor az agyhártya egészséges, és véletlenszerű, ha gyulladt.
- A vankomicin nem metabolizálódik a szervezetben, és körülbelül 90% -át a vesék választják ki aktív formában (ebből 75% 24 órán belül).
Mellékhatások
- A hisztamin-felszabadulás által kiváltott anafilaxiás reakciók közé tartozik a pulzáló típusú fájdalom a hát és a nyak izomzatában, a nyak és a váll bőröblítésének reakciói, finom átmeneti kiütéssel, esetleg csalánkiütéssel: ez a szindróma. "a vörös ember". Kivételesen alacsony vérnyomást vagy akár kardiovaszkuláris összeomlást figyeltek meg (különösen gyermekeknél és csecsemőknél) a gyors injekciók során. A legtöbb esetben ezek a reakciók elkerülhetők lassú infúzióval (legalább 60 perc) és elegendő hígítással.
- Hányinger és hányás lehetséges mellékhatások.
- Helyi vénás toxicitás (endoveinitis) a perifériás úton történő beadást követi. Arra ösztönzi az embereket, hogy a központi útvonalat részesítsék előnyben.
- A cochlearis ototoxicitás és a nephrotoxicitás (tubulopathia) kockázata jelentősen megnő a vankomicin plazmakoncentrációjának emelkedésével vagy a kezelés elhúzódásával. Annál is inkább, amikor a beteg veseelégtelenségben szenved. Néhány visszafordíthatatlan vesekárosodást leírtak. Az ototoxicitás, különösképpen a 70 - 80 mg / l -1 feletti plazmakoncentrációknál tapasztalt , és a nephrotoxicitás más oto- és nephrotoxikus molekulákkal, például aminoglikozidokkal együtt adva erősödik meg .
- A túlérzékenységi reakciók megfigyelhető elsősorban a 7 th nap: generalizált bőrkiütés, eosinophilia , láz.
- A hosszan tartó kezelés során ritkán beszámoltak thrombocytopeniáról (immunallergiás okról, azaz vérlemezke-ellenes antitestek képződéséről a vérben) és neutropeniáról , amelyek néha súlyosak, de a kezelés abbahagyása után gyorsan visszafordíthatók.
- A súlygyarapodást egy tanulmány írta le az endocarditis kezelésében .
Ellenállás
1956 óta használják és annak ellenére, hogy végső megoldásként alkalmazzák, a vankomicin azonban nem mentes a rezisztencia kialakulásától. Léteznek tehát VRE-k , vankomicinnel szemben rezisztens enterococcusok , amelyekben a peptidoglikán prekurzorok D-Ala-D-Ala szerkezetét egy D-Ala-D-laktát szerkezet váltja fel, amely nem teszi lehetővé a vankomicin megkötését. Nagyon kevés utolsó vonalbeli kezelés érhető el ezek ellen a baktériumok ellen. Például megemlítjük a linezolidot . Annak kockázata, hogy az ilyen rezisztencia megjelenik más baktériumcsoportok között, beleértve a staphylococcusokat is , tovább korlátozza annak alkalmazását.
Külső linkek
- Svájci Gyűjteményében gyógyszerek: Különlegességek tartalmazó Vancomycin
Hivatkozások
- számított molekulatömege a „ atomsúlya a Elements 2007 ” on www.chem.qmul.ac.uk .
- Robert Service (2017), a szuperantibiotikum 25 000-szer erősebb, mint elődje , 2017. május 30.
- Annette Von Drygalski, Brian R. Curtis, Daniel W. Bougie, Janice G. McFarland, Scott Ahl, Indra Limbu, Kelty R. Baker, Richard H. Aster, vankomicin által kiváltott immun trombocitopénia , New Eng J Med, 2007; 356 : 904-910
- Thuny F, Richet H, Casalta JP, Angelakis E, Habib G, Raoult D, A fertőző endocarditis vankomicin-kezelése összefügg a közelmúltban szerzett elhízással , PLoS ONE 5 (2): e9074. doi: 10.1371 / folyóirat.pone.0009074
- Y Domart. Glikopeptidek. Méd Chir enciklika (Elsevier, Párizs), Gyógyászat gyakorlati enciklopédiája , 5-0060, 1998, 2 p
- J. Tankovic, [Antibakteriális antibiotikumok. Általános adatok a hatásmódról és az ellenállás mechanizmusairól]. Rev Prat. 2000; 50 (4); 425-32