Reduktív elimináció
Reduktív elimináció egy elemi lépést a fémorganikus kémiában , ahol a oxidációs állapotban a fém centrum csökken, miközben képező új kovalens kötés a két ligandum . Ez az oxidatív addíció fordított reakciója, és sok katalitikus folyamatban gyakran képezi a terméket. Mivel az oxidatív addíció és a reduktív elimináció fordított reakció, mindkét folyamatra ugyanazok a mechanizmusok vonatkoznak, és a termék egyensúlya mindkét reakció termodinamikájától függ.
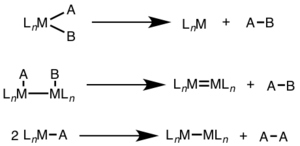
A reduktív elimináció gyakran megfigyelhető magas oxidációs állapotokban, és magában foglalhat két elektronváltást egyetlen fémközpontban (mononukleáris) vagy egy elektronváltozást a két fémközpont mindegyikében (binukleáris, dinukleáris vagy bimetál).
A mononukleáris reduktív eliminációhoz a fém oxidációs állapota kettővel csökken, míg a fém d pályáján az elektronok száma kettővel növekszik. Ez az út gyakori d 8 fémek (Ni (II), Pd (II) és Au (III)) és d 6 fémek (Pt (IV), Pd (IV), Ir (III) és a Rh (III)). Ezenkívül a mononukleáris reduktív elimináció megköveteli, hogy az eltávolított csoportok egymáshoz viszonyítva cisz legyenek a fém közepén.

A binukleáris reduktív eliminációhoz az egyes fémek oxidációs állapota eggyel csökken, míg az egyes fémek d elektronjának száma eggyel növekszik. Ez a fajta reaktivitás általában az első vonalbeli fémeknél figyelhető meg, amelyek előnyben részesítik az oxidációs állapot egy egységnyi változását, de a második és a harmadik vonal fémjeinél.
Az oxidatív addícióhoz hasonlóan a reduktív eliminációval is számos mechanizmus lehetséges. Az uralkodó mechanizmus egy összehangolt mechanizmus , ami azt jelenti, hogy ez egy három központú, nem poláris átmeneti állapot , a sztereokémia megtartásával . Ezen túlmenően, egy S N 2 mechanizmus , amely úgy megy végbe, hogy a sztereokémia megfordul, vagy egy gyökös mechanizmussal , amely úgy megy végbe, a relatív a sztereokémia megfordul, más lehetséges utat a reduktív elimináció.
Megjegyzések és hivatkozások
- Robert H. Crabtree , Az átmenetifémek fémorganikus kémiája , Wiley,2014, 173 p. ( ISBN 978-1-118-13807-6 )
- John F. Hartwig , Organotransition Metal Chemistry, a kötéstől a katalízisig , University Science Books,2010, 321 p. ( ISBN 978-1-891389-53-5 )
- Gillie és Stille, „ A palládium 1,1-reduktív eliminációjának mechanizmusai ”, J. Am. Chem. Soc. , vol. 102, n o 15,1980, P. 4933–4941 ( DOI 10.1021 / ja00535a018 )
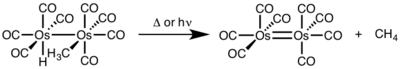
- Okrasinski és Nortom, „ A reduktív elimináció mechanizmusa. 2. A Dinuclear vs. A metán mononukleáris eliminációja cisz-hidridometil-tetrakarbonil-moszmiumból ”, J. Am. Chem. Soc. , vol. 99,1977, P. 295–297 ( DOI 10.1021 / ja00443a076 )
- Crabtree, Robert H. (2014). Az átmenetifémek szerves fémkémiája (6 szerk.). Wiley. o. 173. ( ISBN 978-1-118-13807-6 ) .