Diels-Alder reakció
A Diels-Alder reakció egy kémiai reakció használt szerves kémiában , amelyben egy alkén (dienofil) hozzáad egy konjugált dién alkotnak egy származékát ciklohexén . Otto Diels és Kurt Alder 1950-ben kémiai Nobel-díjat kapott a reakcióval kapcsolatos munkáért.
A fejlett anyagok és a rugalmas robotika területén „Diels-Alder polimerekről” ( „Diels-Alder polimerek” ) beszélünk, hogy leírjuk a hőre fordítható kovalens hálózatokból álló polimereket. Egy ilyen anyagot a közelmúltban (2016-2017) sikeresen teszteltek a rugalmas robotika három pneumatikus működtetőjének (egy rugalmas bilincs, egy kéz és a mesterséges izmok) öngyógyulásának az elváltozások után a szóban forgó polimer szúrásával, szakadásával vagy fújásával.
Cyclo-addíciók
A Diels-Alder reakció egy általánosabb reakcióosztály speciális esete: a π rendszerek közötti ciklus- addíciós reakciók . A Diels-Alder reakcióban a dién 4 π elektronja reagál a 2 π elektronokat tartalmazó alkén kettős kötésével. Emiatt ezt a reakciót ciklloaddíciónak nevezzük [4 + 2].
Ezeknek a reakcióknak a végrehajtása általában melegítést igényel.
Éger szabály
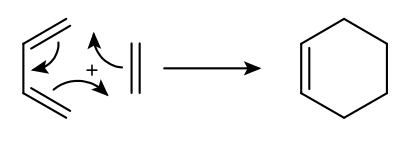
A Diels-Alder reakció könnyűsége nagymértékben függ a dién és a dienofil szubsztituensek természetétől. Az alábbi prototípus-reakció etén és but-1,3-dién között nehezen megy végbe, és meglehetősen alacsony ciklohexénhozamot eredményez.
Alder szabálya lehetővé teszi azon körülmények meghatározását, amelyek megkönnyítik ezen ciklusaddíciók előállítását: a reakció könnyebben megy végbe egy elektronokban gazdag és az elektronokban szegény dienofil között. Más szavakkal, a "jó" diént atomokkal vagy atomcsoportokkal helyettesítik, amelyek elektront adnak, a "jó" dienofileket atomokkal vagy atomcsoportokkal, amelyek vonzzák (elfogadják) az elektronokat.
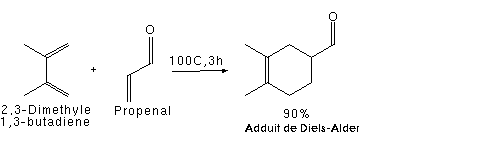
Ezek a szereplők, vonzók vagy donorok lehetnek induktív , mesomerikus vagy hiperkonjugációs hatásúak . Az alábbiakban a 2,3-dimetil-buta-1,3-dién (2 elektronadományozó metilcsoport ) és a propenal ( elektront kivonó aldehidcsoport ) reakciója jó hozammal megy végbe.
A vonzó csoportokkal szubsztituált alkin jó dienofil, és Diels-Alders reakciónak van kitéve. Valóban, a reakció egy etincsoport szubsztituált 2 elektronszívó csoportok (például CH 3 OOC) -C = C- (COOCH 3 ) a buta-1,3-dién ad egy lehetséges reakciót. Másrészt egy két konjugált π kötést tartalmazó vegyület, amelyek közül legalább az egyik alkin, rossz dién, mivel nem helyezhető el az s-cisz konformációban. A reakcióhoz magas hőmérsékletre van szükség.
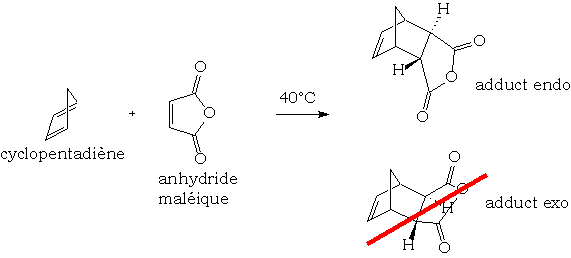
A reakció sztereokémiája
Ez a [4 + 2] cikloaddíciós reakció orbitális irányítás alatt áll, ami általában endo sztereoizomer képződését eredményezi, ha a dién ciklikus. Ezt a szelektivitást gyakran igazolják az endo megközelítést stabilizáló másodlagos határok:
A reakció visszafordítható. Az endo vegyület általában a termodinamikailag a legstabilabb. Ha hagyjuk, hogy a reakció nagyon hosszú ideig folytatódjon, akkor az egyensúly az exo termék javára válik.
Megfordítható karakter
Ez a reakció visszafordítható. A fordított reakciókat, az úgynevezett retro-Diels-Alder felhasználhatjuk vegyületek előállítására. Például a ciklohexén termikus krakkolása lehetővé teszi butadién és etén előállítását .
Egyes szerzők helytelenül használják a "reverzibilis" kifejezést a "reverzibilis" helyett, miközben bármilyen kémiai átalakulás entrópiát hoz létre.
Gyakorlatban
A Diels-Alder reakció problematikus lehet, például a ciklopentadién tárolásával összefüggésben, amely szobahőmérsékleten lassan dimerizálódik és triciklusos vegyületet képez, önmagában Diels-Alder reakcióval. A kapott, szobahőmérsékleten (T eb = 140 ° C ) stabil vegyületet lassan desztilláljuk, hogy retro-Diels-Alder reakcióval kinyerjük a ciklopentadiént (T eb = 41 ° C ) .
Megjegyzések és hivatkozások
- (de) O. Diels és K. Alder , „ Synthesen in der hydroaromatischen Reihe. I. Mitteilung: Anlagerungen von Di-en kohlenwasserstoffen ” , Liebigs Ann. Chem , vol. 460, n o 1,1928, P. 98–122 ( ISSN 0075-4617 , DOI 10.1002 / jlac.19284600106 ).
- (de) O. Diels és K. Alder , „ Synthesen in der hydroaromatischen Reihe. III. Mitteilung: Synthese von Terpenen, Camphern, hydroaromatischen und heterocyclischen Systemen ” , Liebigs Ann. Chem , vol. 470, n o 1,1929, P. 62–103 ( ISSN 0075-4617 , DOI 10.1002 / jlac.19294700106 ).
- (de) O. Diels és K. Alder , „ Synthesen in der hydroaromatischen Reihe. IV. Mitteilung: Über die Anlagerung von Maleinsäure-anhydrid an arylierte Diene, Triene und Fulvene ” , Ber. Dtsch. Chem. Ges. , vol. 62, n o 8,1929, P. 2081–2087 ( ISSN 0365-947X , DOI 10.1002 / cber.19290620829 ).
- (de) O. Diels és K. Alder , „ Synthesen in der hydroaromatischen Reihe. V. Mitteilung: Über Δ 4 -Tetrahydro-o-phthalsäure ” , Ber. Dtsch. Chem. Ges. , vol. 62, n o 8,1929, P. 2087–2090 ( ISSN 0365-947X , DOI 10.1002 / cber.19290620830 ).
- Seppe Terryn, Joost Brancart, Dirk Lefeber, Guy Van Assche & Bram Vanderborght (2017), Öngyógyító puha pneumatikus robotok | Tudományos robotika | 2017. augusztus 16 .: Vol. 2. szám, 9. szám, eaan4268 | DOI: 10.1126 / scirobotics.aan4268 | absztrakt