Adenozin-trifoszfát
| Adenozin-trifoszfát | |
 Az adenozin-trifoszfát ATP 4– szerkezete , domináns faj vizes oldatban   |
|
| Azonosítás | |
|---|---|
| IUPAC név | adenozin-5 '- (tetrahidrogén-trifoszfát) |
| Szinonimák |
Adenozin-5'-trifoszfát |
| N o CAS | |
| N o ECHA | 100 000 258 |
| N o EC | 200-283-2 |
| DrugBank | DB00171 |
| PubChem | 5957 |
| ChEBI | 15422 |
| Mosoly |
Nc1ncnc2n (cnc12) [C @ H] 1O [C @ H] (COP (O) (= O) OP (O) (= O) OP (O) (O) = O) [C @ H] ( O) [C @ H] 1O , |
| InChI |
Std. InChI: InChI = 1S / C10H16N5O13P3 / c11-8-5-9 (13-2-12-8) 15 (3-14-5) 10-7 (17) 6 (16) 4 (26-10) 1-25-30 (21.22) 28-31 (23.24) 27-29 (18.19) 20 / h2-4.6-7,10,16-17H, 1H2, (H, 21.22) (H, 23.24) (H2.11) 12,13) (H2,18,19,20) / t4-, 6-, 7-, 10- / m1 / s1 Std. InChIKey: ZKHQWZAMYRWXGA-KQYNXXCUSA-N |
| Kémiai tulajdonságok | |
| Képlet |
C 10 H 16 N 5 O 13 P 3 [Az izomerek] |
| Moláris tömeg | 507,181 ± 0,014 g / mol C 23,68%, H 3,18%, N 13,81%, O 41,01%, P 18,32%, |
| Egység SI és STP hiányában. | |
A adenozin-trifoszfát vagy ATP , egy nukleotid kialakítva nukleozid egy trifoszfát . A biokémia az összes ismert élőlény, ATP szolgáltatja az energiát szükséges kémiai reakciók az anyagcsere , a mozgás , a sejtosztódás , illetve a hatóanyag szállítására a kémiai anyagok között a biológiai membránok . Annak érdekében, hogy kiadja ezt az energiát, az ATP molekulát hasítjuk , a hidrolízis , a adenozin-difoszfát (ADP) és foszfát , mely reakció kíséri változás szabványos szabad entalpiája ΔG 0 ' a -30,5 kJ mol -1 . A sejtek ezután az ADP-ből az ATP-t lényegében három módon regenerálják: oxidatív foszforilezéssel a sejtlégzés keretében , fotofoszforilezéssel a fotoszintézis részeként , valamint foszforilezéssel a szubsztráton bizonyos exergonikus kémiai reakciók során, például glikolízis vagy Krebs-ciklus során. . Így az emberi test bármikor csak körülbelül 250 g ATP-t tartalmaz, de minden nap a saját súlyának nagyságrendjében fogyaszt és regenerálódik ATP-ben.
- A sejtek , ATP folyamatosan hidrolizáljuk , hogy az ADP és regenerált ADP.
Az ATP-molekula egy trifoszfát-csoport kötődik a atom a szén-dioxid- 5 „végén egy maradékot a ribóz , a pentóz , beleértve a szénatom 1” kötődik az atom a nitrogén 9 „egy maradéka adenin , egy bázis purin . A trifoszfátcsoport két P - O - P foszfoanhidrid kötése nagy átviteli potenciállal rendelkező kötés, vagyis hogy hidrolízissel hasítva nagy mennyiségű energiát szabadít fel: ez exergon reakció . Egy ilyen exergon reakció összekapcsolása endergon reakcióval , vagyis olyan energiával, amely elnyeli az energiát, ez utóbbi termodinamikailag lehetővé válik. Ily módon az anyagcsere-reakciók, amelyek energiát igényelnek, például a bioszintézis- reakciók , amelyek spontán, nagyon lassan vagy egyáltalán nem fordulnak elő, a sejtekben sokkal gyorsabban lejátszódhatnak.
ATP a prekurzor számos kofaktorok enzim fontos, mint a NAD + , vagy CoA . Ez egy foszfátcsoport transzfer koenzim, amely nem kovalensen kapcsolódik a kináz család enzimjeihez . Az utóbbi részt vesznek a transzdukció egyes sejt jelátviteli utak , a foszforiláció a megcélzott fehérjék és enzimek, az aktivitása, amely így szabályozott, vagy foszforilezése lipidek . Az ATP az adenilát-cikláz szubsztrátja is , amely ciklikus AMP-vé alakítja át . Ez egy intracelluláris másodlagos hírvivő, amely átveszi különösen a hormonoktól , mint például a glukagon és az adrenalin , hogy befolyásolja a glikogén , a szénhidrátok és általában a lipidek metabolizmusát . Az ATP koncentrációja és az AMP koncentrációja közötti arányt a sejtek energiaterhelésük, vagyis a rendelkezésükre álló energiamennyiség meghatározásához használják fel, amely az esettől függően lehetővé teszi számukra, hogy anyagcseréjüket a termelés felé irányítsák, ill. az anyagcsere-energia tárolása. Továbbá az ATP-t az RNS-polimerázok használják a DNS riboszomális RNS-be és messenger-RNS- be történő transzkripciójának folyamatában .
Az ATP-t 1929-ben fedezte fel Karl Lohmann német biokémikus , ezzel párhuzamosan pedig amerikai biokémikusok, Cyrus Fiske és Indian Yellapragada Subbarao (in) . A német Fritz Albert Lipmann javasolta, hogy közvetítő szerepet töltsön be az energiát felszabadító reakciók és az azt elnyelő reakciók között. Az ATP-t először a laboratóriumban szintetizálták 1948-ban, Alexander Robert Todd .
Tulajdonságok
Fizika és kémia
Az ATP adeninből , ribózból és három foszfátcsoportból áll , amelyek trifoszfátcsoportot alkotnak . Ezt a három foszfátcsoportot ribózztól kifelé görög α ( alfa ), β ( béta ) és γ ( gamma ) betűkkel jelöljük . Az ATP tehát szorosan kapcsolódik az AMP-hez , az RNS egyik monomerjéhez és a dAMP-hoz , a DNS egyik monomerjéhez . Az ATP vízben nagyon jól oldódik. A vizes oldatban viszonylag stabil marad , pH-ja 6,8 és 7,4 között van, de savasabb vagy bázikusabb pH-n gyorsan hidrolizál . Ezért az ATP leginkább vízmentes sóként tárolható .
Az ATP viszont instabil, amint már nincs semleges pH pufferoldatban . Ezután hidrolizálódik ADP-vé és foszfáttá. Ennek az az oka, hogy az egyrészt a vízmolekulák, másrészt az ADP és a foszfát közötti hidrogénkötések erősebbek, mint a P - O - P foszfoanhidridkötések, amelyek egyesítik a foszfátcsoportokat az ATP molekulában. Ezért az ATP hajlamos hosszabb vagy rövidebb idő elteltével szinte teljes mértékben disszociálni ADP-be és foszfátba, amikor vízben oldódik.
Semleges vizes oldatban az oldott ATP-t négyszer ionizálják , így az ATP 4– anion képződik , kis arányban ATP 3– ionokkal .
Mivel az ATP-nek több negatív töltésű csoportja van semleges oldatban, nagy affinitással kelátképezheti a fém kationjait . A közös fémkationok némelyikének kötési állandója moláris értéke a következő:
Ezek a kölcsönhatások elég erősek ahhoz, hogy az ATP 4– nagy része jelen legyen az Mg 2+ -val komplexált sejtekben .
Termodinamika
Ha a termodinamikai rendszer messze van az egyensúlytól, akkor van egy szabad entalpija, amely lehetővé teszi a termodinamikai értelemben vett munka elvégzését . Az élő sejtek az ATP és az ADP közötti koncentrációarányt közel 5 értéken tartják, ami körülbelül tíz nagyságrenddel magasabb, mint az egyensúlyi helyzetben kialakult koncentrációarány, ahol szinte minden ATP disszociál ADP-ben és foszfátban. Ennek az egyensúlytól való eltérésnek köszönhetően az ATP hidrolízise ADP-vel és foszfáttal nagy mennyiségű energiát szabadít fel.
A molekula energiáját felszabadítja az ATP szomszédos foszfátcsoportjait megkötő két foszfoanhidrid kötés hidrolízise. Emiatt a kényelem kedvéért, de helytelenül ezeket a foszfoanhidrid kötéseket gyakran energiadús kötéseknek nevezik. Ez a tulajdonság azonban félrevezető, mivel ezek a kötelékek önmagukban nem tartalmaznak több energiát, mint a többiek, és szakadásukhoz aktivációs energiához kell hozzájárulni, mint bármely más kötés megszakadásához; csak molekuláris környezetükben van hidrolízisük exergonikus , standard szabad entalpia- variációja −30,5 kJ mol −1 (negatív, mert energia szabadul fel a reakció során):
ATP + 2 H 2 O→ ADP + Pi + H 3 O + : ΔG 0 ′ = −30,5 kJ mol −1 .Ezzel szemben az ADP és az ATP közötti foszforilezési reakció endergonikus , a szokásos szabad entalpia-változás 30,5 kJ mol −1 (pozitív, mert az energia felszívódik a reakció során):
ADP + Pi + H 3 O +→ ATP + 2 H 2 O : ΔG 0 ′ = 30,5 kJ mol -1 .Az ATP hidrolízisreakciója AMP-vel és pirofoszfát HP 2 O 7 3-exergonikusabb, standard szabad entalpia-variációja −45,6 kJ mol −1 :
ATP + 2 H 2 O→ AMP + PPi + H 3 O + : ΔG 0 ′ = −45,6 kJ mol −1 .Biológiai funkciók
A sejtek anyagcseréje, szerveződése és mobilitása
ATP fogyasztják sejtek által biokémiai és élettani folyamatok , amelyek megkövetelik az energia, az úgynevezett endergonic , és folyamatosan újratermelődik, amely eljárásokat energiát bocsátanak, az úgynevezett exergonic . Ily módon az ATP lehetővé teszi az energia átadását a térben elkülönülő folyamatok között. Ez a fő energiaforrás a legtöbb celluláris funkciók, mint például a metabolizmus , bioszintézis , aktív transzport révén a biológiai membránokon , vagy akár a motilitás a sejtek és a mozgásszervi komplex organizmusok ( izomösszehúzódás )..
Az ATP a sejtszerkezet fenntartásában, valamint mobilitásában is részt vesz, megkönnyítve a citoszkeleton elemeinek összeszerelését és szétszerelését . Hasonlóképpen biztosítja az izomösszehúzódás energiáját az aktin és a miozin szálak rövidülésének katalizálásával , amely az állatok alapvető szükséglete , elengedhetetlen a mozgásukhoz és a légzésükhöz - mind tüdőjük szellőztetése, mind pedig a működése szempontjából. azok szívét , felelős keringő azok oxigéndús vért az egész testet .
Sejtjelzés
Az ATP részt vesz a sejtjelzés mechanizmusaiban abban, hogy purinerg receptorok (in) ismerik fel őket , amelyek talán az emlősök szöveteiben a leggyakoribb receptorok . Ebben emberben , ezt a szerepet a sejt jelátviteli fontos mind a központi idegrendszerben , és a perifériás idegrendszerben . A P2-purinerg receptorok aktiválódnak azáltal, hogy az ATP felszabadul a szinapszisokból , az axonokból és a gliasejtekből . A P2Y receptorok (in) például kapcsolt receptorok G-fehérjék, amelyek modulálják az intracelluláris kalciumszintet, és néha a ciklikus AMP szintjét is .
A sejtek belsejében az ATP-t a kinázok használják foszfátcsoportok forrásaként foszforilezések végrehajtására . A fehérjék és a membrán lipidek foszforilezése a jelátvitel általános formája . Például a fehérjék aktiválódását a MAP kinázokkal végzett kaszkádos foszforilációk figyelhetik meg . Az ATP az adenilát-cikláz szubsztrátja is , amely ciklikus AMP-t termel , egy másodlagos hírvivőt, amely kiváltja a kalcium felszabadulását intracelluláris tárolási pontjaiból. A jelátvitel ilyen formája különösen fontos az agy működésében , bár más sejtes folyamatok sokaságában is részt vesz.
- Átalakítása ATP ciklikus AMP által az adenilát-ciklázt .
DNS replikáció és transzkripció RNS-be
Az összes ismert élőlény, a dezoxi-ribonukleotidok alkotó DNS előállítása egy ribonukleotid reduktáz (RNR) a megfelelő ribonukleotidok . Ezek az enzimek csökkentik a maradékot a ribóz a dezoxiribóz egy csoportja szulfhidril -SH a maradékot cisztein képező diszulfidkötés egy másik cisztein-maradék a reakcióban. Redukált formájuk tioredoxin vagy glutaredoxin hatására regenerálódik .
A ribonukleotid-reduktázok és a kapcsolódó enzimek szabályozása fenntartja a sejtben az egyensúlyt a dezoxiribonukleotidok és a ribonukleotidok között egymáshoz viszonyítva. A dezoxiribonukleotidok túl alacsony koncentrációja gátolja a DNS-helyreállítást és -replikációt , ami végső soron elpusztítja a sejtet, míg a különböző dezoxiribonukleotidok koncentrációinak rendellenes kapcsolata mutagén, mivel megnő a valószínûsége annak, hogy a DNS-polimerázok DNS-replikációja során hibás nukleáris bázist építenek be . A ribonukleotid-reduktázok szabályozása vagy a specifikussági különbségek valószínűleg e dezoxiribonukleotidkészleten belüli egyensúly megváltozásának eredetét jelentik, amelyet sejtes stressz , például hipoxia esetén észleltek .
A DNS riboszomális RNS-be és messenger RNS- be történő átírása során az ATP egyike annak a négy nukleotidnak, amelyeket az RNS-polimerázok beépítettek az RNS- be . A polimerizáció előállításához szükséges energia az ATP pirofoszfát- csoportjának hidrolíziséből származik . A folyamat megegyezik a DNS bioszintézisével, azzal az eltéréssel, hogy ATP-t használnak a dezoxi- adenozin- trifoszfát (dATP) helyett .
Regenerálás
Az ATP intracelluláris koncentrációja jellemzően 1-10 mmol / l nagyságrendű . Az ATP regenerálható az ADP-ből a szénhidrátok vagy lipidek oxidációjával felszabaduló energia segítségével, amelyet sejtlégzésnek neveznek . Körülbelül 30 ATP molekula állítható elő minden oxidált glükózmolekulához . Az ózok (cukrok) már részben oxidált molekulák, így egy zsírsav szénatomonként több ATP-molekulát képes előállítani (16 a palmitát és 6 a glükóz esetében), és a test tartalékainak és energiaellátásának nagy részét képezi; de a cukrok vízben oldódva könnyebben hozzáférhetők és oxidálhatók. A nem fotoszintetikus eukarióták által előállított ATP legnagyobb része a mitokondriumban található oxidatív foszforilációból származik . A β-oxidáció és a Krebs-ciklus a mitokondriumokban is végbemegy, amelyek akár a sejt térfogatának negyedét is elfoglalhatják; Az ezen organizmusok által termelt ATP fennmaradó részét foszforilezéssel regenerálják a szubsztrát szintjén , például glikolízis során vagy a citoplazmában történő fermentációval . A növények és a fotoszintetikus baktériumok viszont lényegében fotofoszforilezést hoznak létre ATP-ben .
Glikolízis
A glükóz alakítjuk piruvát egy metabolikus út nevű glikolízis . A legtöbb élőlény megvalósítani ezt az átalakítást a citoplazmában való sejtek , de néhány egysejtűek , mint például a class of kinetoplastid , magatartás organelle szakosodott úgynevezett glycosome . Az így oxidált glükózmolekulákhoz két ATP-molekula termelődik két enzim szintjén, amelyek foszforilezést hajtanak végre a szubsztrát szintjén : foszfoglicerát-kináz és piruvát-kináz . Két NADH molekula is termelődik a NAD + -ból , amelyeket a légzési lánc oxidálhat és további ATP-molekulákat állíthat elő. A glikolízis végén keletkező piruvát a Krebs-ciklus szubsztrátja .
Krebs ciklus
A mitokondriumok , piruvát van oxidálva a piruvát-dehidrogenáz komplex alkotnak acetil-CoA . Ez utóbbi CO 2 -vá oxidálódik, NADH és FADH 2a Krebs-ciklus által , szintén GTP előállításával , amely energetikailag egyenértékű az ATP-vel.
NADH és FADH 2átadják elektronok nagy transzfer potenciál a légzési lánc , amely termel további ATP molekulák oxidatív foszforiláció , amelynek mértéke 2-3 molekula ATP egy molekula NADH, és 1-től 2 molekula ATP per FADH 2. A nem fotoszintetikus sejtek ATP- jének legnagyobb részét ily módon állítják elő. Bár a Krebs-ciklus nem igényli közvetlenül oxigén O 2 jelenlétét, nem tud működni nélküle, mert az oxigén az utolsó elfogadója az elektronoknak a légzési láncban, lehetővé téve a NAD + és FAD regenerálódását a NADH-ból és a FADH-ból 2a Krebs-ciklus produkálja: oxigén hiányában ez utóbbi NAD + és FAD hiánya miatt megszűnik .
Oxidatív foszforiláció
Az elektronok áramlása a légzési láncon keresztül lehetővé teszi a protonok kiszivattyúzását a mitokondriális mátrixból , amely a kapott protonkoncentráció- gradiens miatt membránelektrokémiai potenciált generál a belső mitokondriális membránon . A disszipáció e elektrokémiai membránpotenciál által ATP szintetázok biztosítja a szükséges energiát a foszforiláció a ADP ATP: ezt nevezik kemiozmotikus kapcsolási között légzési lánc és foszforilezését ADP. Az ATP-szintáz egy komplex enzim, amelynek molekuláris rotora van, amelyet a protonok visszafolyása hajt a mitokondriális intermembrán térből, és amely utóbbi energiáját az ADP-foszforiláció szintjére továbbítja.
Regenerálása ATP mitokondriumok a NADH elő a citoszolban magában halad a belső mitokondrium-hártyán keresztül NADH a mitokondriális mátrixban és NAD + a másik irányba. Valójában ezek a molekulák önmagukban nem képesek átjutni ezen a membránon, ezért nagy átviteli potenciállal rendelkező elektronjaik keresztezik azt. Az eukarióta ennek lényegében két módját használja: a malát-aszpartát transzfert , és kisebb mértékben a glicerin-3-foszfát transzferjét .
- A malát-aszpartát inga első magában foglalja egy malát-dehidrogenáz , amely csökkenti a citoszolban oxálacetát molekula malát . Az utóbbi átjut a belső mitokondrium-hártyán felvételével egy antiport malate- α-ketoglutarát , és miután elérte a mitokondriális mátrixban , a malát oxidált ismét oxálacetát egy mitokondriális izoforma mitokondriális malát-dehidrogenáz (mMDH), konvertáló egy molekula NAD + a NADH-ba. Mitokondriális oxálacetát alakítjuk aszpartát hatása alatt egy mitokondriális aszpartát-aminotranszferáz (MAST) átutalással egy amin -csoport a glutamát , az utóbbi akkor így α-ketoglutarát . Az aszpartát kölcsönvesz egy glutamát-aszpartát antiportot, hogy átlépje a belső mitokondriális membránt és csatlakozzon a citoszolhoz, míg az α-ketoglutarát ugyanezt teszi egy malát- α-ketoglutarát antiport alkalmazásával . A citoszolos aszpartátot citoszolos aszpartát-aminotranszferáz (cAST) alakítja oxaloacetáttá, amely az a-ketoglutarátból glutamátot is termel .
- A glicerin-3-foszfát transzfer kevésbé elterjedt, mint az előző, de nem igényli a belső mitokondriális membrán keresztezését, ami gyorsabbá teszi, bár kevesebb ATP keletkezéséhez vezet egy oxidált NADH molekulánként, így előnyösen sejtek, amelyek nagy mennyiségű energia, azaz főleg az izmok és az agy gyors mobilizálását igénylik . Az oldható glicerin-3-foszfát-dehidrogenáz ( EC ) először átalakítja a dihidroxi- aceton- foszfátot (DHAP) glicerin-3-foszfáttá , amely a NAD + -ot regenerálja a NADH-ból. A belső mitokondriális membrán glicerin-3-foszfát-dehidrogenáz ( EC ) Elektronokat bocsát ki a glicerin-3-foszfátból egy FAD molekulába, és így FADH 2-t kap.és a DHAP regenerálása; a FADH 2viszont csökkenti az ubikinont , amelynek elektronai a Q koenzim - citokróm c reduktáz ( III komplex ) szintjén csatlakoznak a légzési lánchoz .
ATP / ADP transzlok
A NAD + esetében megfigyeltekhez hasonlóan a mitokondriumokban regenerált ATP-t főleg a citoplazmában és a magban fogyasztják , ahol ADP képződik, amelyet a sejteken belül ATP-nek kell foszforilezni. Ezek az anyagáramok magukban foglalják az ADP keringését a belső mitokondriális membránon keresztül a citoszoltól a mitokondriális mátrixig, míg a mitokondriumokban regenerált ATP keresztezi ezt a membránt fordított irányban, hogy a citoszolban és a magban elfogyasszák. Mivel a belső mitokondriális membrán az ADP-t és az ATP-t is áthatolhatatlan, ezeknek a molekuláknak átengedniük kell az integrált membránfehérjéket, az úgynevezett ATP / ADP transzlokákat, hogy átkeljenek rajta.
A növények , az ATP által termelt photophosphorylation a membrán a tilakoidok belsejében a kloroplasztok . Az elv hasonló a végrehajtott keretében oxidatív foszforiláció , a kemiozmotikus kapcsolási az azonos jellegű, azzal a különbséggel, hogy a fényenergiát a fotonok által rögzített fotoszintetikus pigmentek , és nem a oxidációját a szénhidrátok és lipidek . Ennek az ATP-nek egy részét a kloroplaszt fogyasztja szénhidrátok előállítására a Calvin-ciklus során .
A test ATP készletei nem haladják meg a fogyasztás néhány másodpercét. Elvileg az ATP-t folyamatosan újrahasznosítják, és minden olyan folyamat, amely blokkolja a regenerálódását, gyorsan a szennyezett szervezet halálát okozza. Ez a helyzet például az egyes harci gázok erre a célra tervezett, vagy a mérgek, mint például a cianid , amely blokkolja a citokróm c -oxidáz a légzési lánc a mitokondriumokban , illetve arzén , amely helyettesíti a foszfor, és teszi használhatatlanná a foszfor-molekulák.
A kreatin akkumulátorként játszhat, amely nagy potenciálú foszfátcsoport transzfert tárol egy ATP-molekulától, amelyet később át lehet vinni egy ADP-molekulába az ATP regenerálásához:
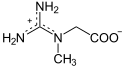
|
+ ATP ADP + |

|
| Kreatin | Foszfokreatin | |
| Kreatin-kináz - EC | ||
ATP, mint olyan nem lehet tárolni a sejtekben, így a metabolikus energia tárolódik például lipidek a zsírszövetben vagy a szénhidrátok , például a glikogén az állatok vagy a keményítő a állatokban. Növényekben .
Szabályozás
Az ATP termelődését az eukarióta aerob sejtekben szorosan szabályozza az alloszterikus , a visszacsatolás és a glikolízis és az oxidatív foszforiláció különféle enzimjeinek szubsztrátjainak koncentrációja . Az ellenőrzési pontok olyan reakciókban találhatók, amelyek termodinamikailag annyira kedvezőek, hogy fiziológiai körülmények között valójában irreverzibilisek.
Glikolízis
A hexokinázt közvetlenül gátolja az általa katalizált reakció terméke , nevezetesen a glükóz-6-foszfát , míg a piruvát-kinázt maga az ATP gátolja. A glikolízis szabályozásának fő pontja a foszfofruktokináz (PFK), amelyet alloszterikusan gátolnak, ha az ATP bőséges, de akkor aktiválódik, amikor az AMP bőséges. Ennek az enzimnek az ATP általi gátlása szokatlan, mivel az ATP a katalizált reakció szubsztrátja. Ennek az enzimnek biológiailag aktív formája egy tetramer, amely két lehetséges konformációban létezik, amelyek közül csak az egyik kötődhet a fruktóz-6-foszfáthoz , amely ennek az enzimnek a második szubsztrátja. A fehérje két ATP-kötőhellyel rendelkezik: az aktív hely mindkét konformációban hozzáférhető, de az ATP a gátló helyhez való kötődése stabilizálja a konformációt, amely csak gyengén kötődik a fruktóz-6-foszfáthoz. Bizonyos számú más kis molekula képes kompenzálni az ATP gátló hatását, és ezáltal újra aktiválni a foszfofruktokinázt; ez a helyzet például a ciklikus AMP , az ionok ammónium , ionok foszfátjának , a fruktóz-1,6-biszfoszfát és fruktóz-2,6-biszfoszfát .
Krebs ciklus
A Krebs-ciklust alapvetően kulcsfontosságú szubsztrátjainak elérhetősége szabályozza , különös tekintettel a NAD + és NADH koncentrációjának, valamint a kalcium , foszfát , ATP, ADP és AMP koncentrációinak arányára . A citrát egy inhibitora a citrát-szintáz keresztül ható visszacsatolás , és inhibitora foszfofruktokináz , amely kötődik a szabályozás a Krebs-ciklus, hogy, hogy a glikolízis .
Oxidatív foszforiláció
Az oxidatív foszforilezés szabályozása lényegében a citokróm c- oxidázon alapul , amelyet a szubsztrátja, nevezetesen a redukált citokróm c elérhetősége szabályoz . A rendelkezésre álló redukált citokróm c mennyisége közvetlenül függ a többi szubsztrát mennyiségétől:
1 / 2 NADH + oxidált cyt c + ADP + Pi 1 / 2 NAD + + csökkentett cyt c + ATP,ezért az alábbi egyenlet levonható ebből az egyensúlyból:
Tehát a magas [NADH] ⁄ [NAD + ] koncentráció arány vagy a magas [ADP] [Pi] ⁄ [ATP] koncentráció arány (ennek az egyenlőségnek a jobb oldala) egy [ csökkentett cyt c ] ⁄ koncentráció arányt jelent [ oxidált cyt c ] (bal végtag), azaz a redukált citokróm c magas koncentrációja és a citokróm c oxidáz erős aktivitása .
További szabályozási szintet vezet be az ATP és NADH transzport sebessége a mitokondriális mátrix és a citoszol között .
Fehérjekötések
Egyes fehérjék , amelyek kötődnek az ATP van egy jellegzetes összecsukható úgynevezett Rossmann szeres , egy általános szerkezeti motívum a fehérjék, amelyek kötődnek a nukleotidokat , mint például azok, amelyek kötődnek az NAD . A leggyakoribb ATP-kötő fehérjék, az úgynevezett kinázok , néhány közös szerkezeti jellemzővel rendelkeznek. A protein kinázok , amelyek a kinázok legnagyobb csoportja, és az ATP kötődésében és a foszfát csoport transzferekben speciális szerkezeti jellemzőkkel rendelkeznek.
ATP általában megköveteli a jelenlétét egy kétértékű kation képez komplexet a fehérjékkel . Szinte mindig a magnézium Mg 2+ kationja , amely az ATP foszfátcsoportjaihoz kötődik. Ez a kation lényegesen csökkenti a disszociációs állandója az ATP - protein komplex anélkül képes a enzimet , hogy katalizálja a kémiai reakció , ha az ATP megkötését. A magnézium-kationok jelenléte mechanizmust jelenthet a kinázok szabályozására.
ATP analógok
In vitro kísérletekben gyakran használják , hogy tanulmányozzák a biokémiai folyamatok járó ATP, és inhibitorai a enzimek ATP-t használva, mint például kinázok , hasznos eszközök vizsgálata kötődési és átmeneti állapotokra. Részt olyan reakciókban, amelyek bevonják az ATP. Az ATP -hez hasonlóan használják a röntgenkristályográfiában is , hogy a fehérjék szerkezetét komplex képezzék az ATP-vel, gyakran más szubsztrátokkal kombinálva. A leghasznosabb ATP-analógok azok, amelyek nem hidrolizálnak, mint az ATP, és blokkolják az enzimet az ATP-enzim komplexhez közeli állapotban. Az adenozin 5 '- [γ-tio] trifoszfát (ATPγS) például az ATP analógja, amelyet nagyon gyakran használnak a laboratóriumban: a γ foszfát oxigénatomjának egyik atomját kénatom helyettesíti , és az ATPγS lényegesen lassabban hidrolizál, mint az ATP, így gátolja az ATP-molekula hidrolízisétől függő folyamatokat. Vannak azonban olyan enzimek, amelyek elég nagy koncentrációban képesek meglehetősen nagy sebességgel hidrolizálni őket, ami azt jelenti, hogy óvatosan kell értelmezni az ilyen inhibitorokkal elért eredményeket.
A krisztallográfia, hidrolízis átmeneti állapotok vannak vizsgáltuk komplexek vanadát ionok .
Megjegyzések és hivatkozások
- számított molekulatömege a „ atomsúlya a Elements 2007 ” on www.chem.qmul.ac.uk .
- (in) szabad energia változás , a helyszínen a Marc Kirschner (in) , a Harvard Medical School .
- (in) 'A Nature elemei segíthették a korai életformák működését " a Science Daily oldalán , 2010. május 25(elérhető : 2016. augusztus 23. )
- (a) David E. Bryant, Katie ER Marriott Stuart A. MacGregor Colin Kilner, Matthew A. Pasek és Terence P. Kee , " A prebiotikus potenciálját Csökkentett foszfor oxidációs állapotban: a H-foszfinát piruvát rendszer " , Chemical Communications , vol. 46, n o 21, 2010. június 7, P. 3726-3728 ( PMID 20386792 , DOI 10.1039 / C002689A , Bibcode 2010LPICo1538.5264B , olvassa el online )
- (in) Susanna Törnroth-Horsefield és Richard Neutze , " A kapu metabolitjának megnyitása és bezárása " , Proceedings of the National Academy of Sciences of the United States of America , vol. 105, n o 50, 2008. december 16, P. 19565-19566 ( PMID 19073922 , PMCID 2604989 , DOI 10.1073 / pnas.0810654106 , online olvasás )
- (a) Eunus S. Ali, Hua Jin, Claire H. Wilson, George A. Tallis, Fiona H. Zhou, Y. Grigorij Rychkov és Greg J. Barritt , " A glukagon-szerű peptid-1-analóg exendin-4 megfordítja károsodott intracelluláris Ca 2+ jelátvitel a szteatotikus májsejtekben ” , Biochimica et Biophysica Acta (BBA) - Molecular Cell Research , vol. 1863 n o 9, 2016. szeptember, P. 2135-2146 ( PMID 27178543 , DOI 10.1016 / j.bbamcr.2016.05.006 , online olvasás )
- (in) D. Grahame Hardie és Simon A. Hawley , " AMP-aktivált protein-kináz: az energiaterhelés hipotézise felülvizsgálva " , BioEssays , vol. 23, n o 12, 2001. december, P. 1112-1119 ( PMID 11746230 , DOI 10.1002 / bies.10009 , online olvasás )
- (a) Karl Lohmann , " Über die im Pyrophosphatfraktion Muskel " , Naturwissenschaften , vol. 17, n o 31, 1929. augusztus, P. 624-625 ( DOI 10.1007 / BF01506215 , olvassa el online )
- (in) Koscak Maruyama , " Az adenozin-trifoszfát felfedezése és szerkezetének kialakítása " , Journal of the History of Biology , vol. 24, n o 1, 1991. március, P. 145-154 ( DOI 10.1007 / BF00130477 , JSTOR 4331161 , online olvasás )
- (in) AC Storer és A. Cornish-Bowden : " Az MgATP 2 és más ionok koncentrációja oldatban. A társuló ionok keverékeiben jelenlévő fajok valódi koncentrációjának kiszámítása ” , Biochemical Journal , vol. 159, n o 1, 1976. október, P. 1–5 ( PMID 11772 , PMCID 1164030 , DOI 10.1042 / bj1590001 , online olvasás )
- (in) John E. Wilson és Arnold Chin , " A kétértékű kationok kelátja ATP segítségével, titrált kalorimetriával tanulmányozva " , Analytical Biochemistry , vol. 193, n o 1, 1991. február 15, P. 16–19 ( PMID 1645933 , DOI 10.1016 / 0003-2697 (91) 90036-S , online olvasható )
- (in) ' Magnézium a szívenergia metabolizmusában " , Journal of Molecular and Cellular Cardiology , Vol. 18, n o 10, 1986. október, P. 1003-1013 ( PMID 3537318 , DOI 10.1016 / S0022-2828 (86) 80289-9 , online olvasás )
- (in) Britton Chance Howard Lees és John R. Postgate , " The Meaning of" fordított Electron Flow "és a" High Energy Electron "Biokémiai " , Letters to Nature , vol. 238, n ° 5363, 1972. augusztus 11, P. 330-331 ( PMID 4561837 , DOI 10.1038 / 238330a0 , online olvasás )
- A sejt molekuláris biológiája : Harvey Lodish, Arnold Berk, Paul Matsudaira, James Darnell , Chris A. Kaiser, Pierre L. Masson - 301. oldal
- (a) Neeti Sanan Mishra és Renu Tuteja Narendra Tuteja , " Signalling keresztül MAP kináz hálózatok növényekben " , Archives of Biochemistry and Biophysics , Vol. 452, n o 1, 2006. augusztus, P. 55–68 ( PMID 16806044 , DOI 10.1016 / j.abb.2006.05.001 , online olvasás )
- (in) Margarita Kamenetsky Sabine Middelhaufe, Erin M. Bank, Lonny R. Levin, Jochen Buck és Clemens Steegborn , " Molecular Details of cAMP Generation in Mammalian Cells: A Tale of Two Systems " , Journal of Molecular Biology , vol. 362, n o 4, 2006. szeptember 29, P. 623-639 ( PMID 16934836 , PMCID 3662476 , DOI 10.1016 / j.jmb.2006.07.045 , online olvasás )
- (in) Jacques és Nicole Defer Hanoune , " Az adenilil-cikláz izoformák szabályozása és szerepe " , Annual Review of Pharmacology and Toxicology , Vol. 41, 2001. április, P. 145-174 ( PMID 11264454 , DOI 10.1146 / annurev.pharmtox.41.1.145 , online olvasható )
- (in) JoAnne Stubbe , " Ribonukleotid-reduktáz: csodálatos és zavaros " , Journal of Biological Chemistry , vol. 265, n o 10, 1990. április 5, P. 5329-5332 ( PMID 2180924 , online olvasás )
- (a) Catherine M. Joyce és Thomas A. Steitz , " polimeráz szerkezet és funkció: variációk egy témára? ” , Journal of bakteriology , vol. 177, n o 22, 1995. november, P. 6321-6329 ( PMID 7592405 , PMCID 177480 , online olvasás )
- (in) I. Beis és EA Newsholme , " Adenin- nukleotidok, glikolitikus intermedierek és néhány foszfagén tartalma gerincesektől és gerinctelenektől nyugvó izmokban " , Biochemical Journal , vol. 152, n o 1, 1975. október, P. 23-32 ( PMID 1212224 , PMCID 1.172.435 , DOI 10,1042 / bj1520023 , olvasható online )
- (en) PR Rich , „ Keilin légzési láncának molekuláris gépezete ” , Biochemical Society Transactions , vol. 31, n o 6, 2003. december, P. 1095-1105 ( PMID 14641005 , DOI 10.1042 / bst0311095 , online olvasás )
- http://biochimej.univ-angers.fr/Page2/COURS/Zsuite/3BiochMetab/8BetaOxydation/1BetaOxydation.htm
- (a) Marilyn Parsons , " glycosomes: paraziták és a divergencia peroxiszómális célú " , Molecular Microbiology , Vol. 53, n o 3, 2004. augusztus, P. 717-724 ( PMID 15255886 , DOI 10.1111 / j.1365-2958.2004.04203.x , olvassa el online )
- (a) Jan Pieter Abrahams Andrew GW Leslie Rene Lutter és John E. Walker , " struktúra 2,8 felbontással F1-ATPáz a szarvasmarha szív mitokondriumok " , Nature , Vol. 370, n ° 6491, 1994. augusztus 25, P. 621-628 ( PMID 8065448 , DOI 10.1038 / 370621a0 , online olvasás )
- (a) John F. Allen , " fotoszintézis ATP Electron, Proton szivattyúk, rotorok, és Poise " , Cell , Vol. 110, n o 3, 2002. augusztus 9, P. 273-276 ( PMID 12176312 , DOI 10.1016 / S0092-8674 (02) 00870-X , online olvasás )
- (a) C. Dahout-Gonzalez, H. Nury, V. Trezeguet, GJ-M. Lauquin, E. Pebay-Peyroula és G. Brandolin , „ A mitokondriális ADP / ATP hordozó molekuláris, funkcionális és patológiai aspektusai ” , Physiology , vol. 21, n o 4, 2005. július 25, P. 242–249 ( PMID 16868313 , DOI 10.1152 / physiol.00005.2006 , online olvasás )
- (in) ST Rao és Michael G. Rossmann , " A szuper-szekunder struktúrák összehasonlítása fehérjékben " , Journal of Molecular Biology , vol. 76, n o 2 1973. május 15, P. 241, IN1, 251-250-256 ( PMID 4737475 , DOI 10.1016 / 0022-2836 (73) 90388-4 , olvassa el online )
- (in) Eric D. Scheeff és Philip E. Bourne , " szerkezeti fejlődését a protein-kináz-Like Szupercsaládba " , PLoS Computational Biology , Vol. 1, N o 5, 2005. október, e49 ( PMID 16244704 , PMCID 1261164 , DOI 10.1371 / journal.pcbi.0010049 , online olvasás )
- (a) Phillip Saylor Chengqian Wang, John T. Hirai és Joseph A. Adams , " A Second Magnézium Ion kritikus ATP kötési értéket a kináz domén a v-fps onkoprotein " , Biochemistry , Vol. 37, n o 36, 1998. szeptember 8, P. 12624-12630 ( PMID 9730835 , DOI 10.1021 / bi9812672 , online olvasás )
- (in) Xiaofeng Lin, Marina K és Ayrapetov Gongqin Sun , " Egy fehérjetirozin-kináz és egy kétértékű fémaktivátor interakciójának entre les aktív helyének jellemzése " , BMC Biochemistry , vol. 6, 2005. november 23, P. 25 ( PMID 16305747 , PMCID 1316873 , DOI 10.1186 / 1471-2091-6-25 , online olvasás )
- (a) Clive R. Bagshaw , " első pillantásra ATP analógok " , Journal of Cell Science , vol. 114, n o Pt 3, 2001. február, P. 459-460 ( PMID 11171313 , online olvasás )
- (a) SM Honigberg, DK Gonda, J. Flory és CM Radding , " A párosítás a folyamatos aktivitás nukleoprotein szálak készült RecA fehérje, egyszálú DNS-t, és az adenozin-5„- (gamma-tio) trifoszfát " , a Journal Biological Chemistry , vol. 260, n o 21, 1985. szeptember 25, P. 11845-11851 ( PMID 3840165 , olvassa el online )
- (en) JA Dantzig, JW Walker, DR Trentham et YE Goldman , " relaxációs izomrostok adenozin 5„- [y-tio] trifoszfát (ATP [y S]), és a lézer fotolízissel ketrecbe zárt ATP [gamma-S] : bizonyíték a nulla erővel rendelkező kereszthidak gyorsan leváló Ca 2+ -függő affinitására ” , Proceedings of the National Academy of Sciences of the United States of America , vol. 85, n o 18, 1988. szeptember, P. 6716-6720 ( PMID 3413119 , PMCID 282.048 , DOI 10,1073 / pnas.85.18.6716 , JSTOR 32451 , Bibcode 1988PNAS ... 85.6716D , olvasható online )
- (in) T. Kraft, SC Yu HJ Kuhn és B. Brenner , " A Ca 2+ hatása gyenge kereszthíd kölcsönhatás az aktinnal adenozin 5 '- [gamma-tio] trifoszfát jelenlétében " , Proceedings of az Amerikai Egyesült Államok Nemzeti Tudományos Akadémiája , t . 89, n o 23, 1992. december, P. 11362-11366 ( PMID 1454820 , PMCID 50550 , DOI 10.1073 / pnas.89.23.11362 , JSTOR 2360707 , Bibcode 1992PNAS ... 8911362K , online olvasás )
- (in) Andrea M. és Joseph M. Resetar Chalovich , " Adenosine 5„- (gamma.-thiotriphosphate.): Egy ATP analógot shoulds óvatosan kell alkalmazni az izom-összehúzódás vizsgálatok " , Biochemistry , Vol. 34, n o 49, 1995. december 12, P. 16039-16045 ( PMID 8519760 , DOI 10.1021 / bi00049a018 , online olvasás )

![{\ displaystyle {\ frac {[\ mathrm {cyt ~ c_ {csökkentett}}]} {[\ mathrm {cyt ~ c_ {oxid}}]}}} = \ bal ({\ frac {[\ mathrm {NADH}] } {[\ mathrm {NAD}] ^ {+}}} \ jobbra) ^ {\ frac {1} {2}} \ balra ({\ frac {[\ mathrm {ADP}] [\ mathrm {P_ {i }}]} {[\ mathrm {ATP}]}} \ jobbra) K _ {\ mathrm {eq}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/89e75ceb7b27981ba88688fe6369101117a55af0)