Perklórsav
| Perklórsav | |||
 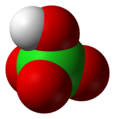 A perklórsav szerkezete. |
|||
| Azonosítás | |||
|---|---|---|---|
| IUPAC név |
Perklórsav hidrogén-perklorát |
||
| N o CAS | |||
| N o ECHA | 100,028,648 | ||
| N o EC | 231-512-4 | ||
| Megjelenés | színtelen, szúrós szagú folyadék | ||
| Kémiai tulajdonságok | |||
| Brute formula |
H Cl O 4 [Az izomerek] |
||
| Moláris tömeg | 100,459 ± 0,003 g / mol H 1%, Cl 35,29%, O 63,71%, |
||
| pKa | ≈ −8 | ||
| Fizikai tulajdonságok | |||
| T ° fúzió | -112 ° C | ||
| T ° forráspontú | (bomlik): 19 ° C | ||
| Oldékonyság | vízben: keverhető | ||
| Térfogat | 1,76 g · cm -3 hogy 22 ° C-on | ||
| Óvintézkedések | |||
| SGH | |||
   Veszély H271, H319, H373, P260, P305 + P351 + P338, P370 + P378, P371 + P380 + P375, H271 : Tûzet vagy robbanást okozhat; erős oxidálószer H319 : Súlyos szemirritációt okoz H373 : Ismételt vagy hosszantartó expozíció után károsíthatja a szerveket (felsorolja az összes érintett szervet, ha ismert) (jelölje meg az expozíciós utat, ha meggyőzően bebizonyosodott, hogy más expozíciós út nem okozza ugyanazt a veszélyt) P260 : Por / füst / gáz / köd / gőzök / permet belélegzése tilos. P305 + P351 + P338 : Ha a szembe jut: Óvatosan öblítse le vízzel néhány percig. Távolítsa el a kontaktlencséket, ha az áldozat viseli őket, és könnyen eltávolíthatók. Öblítse tovább. P370 + P378 : Tűz esetén: Használja a… oltást. P371 + P380 + P375 : Súlyos tűz és nagy mennyiség esetén: ürítse ki a területet. A robbanásveszély miatt távolról oltson tüzet. |
|||
| WHMIS | |||
   C, E, F, C : Oxidáló anyag okok vagy elősegíti az égés a másik anyag felszabadításával oxigén E : Maró anyag veszélyes anyagok szállítása: class 8 F : veszélyesen reaktív anyag válik saját-reaktív hatása alatt sokk Disclosure 1, 0% szerint összetevők nyilvánosságra hozatalának listája |
|||
| NFPA 704 | |||
| 0 3 3 ÖKÖR | |||
| Szállítás | |||
1873 : 50% (tömegszázalékot meghaladó), de legfeljebb 72% savat tartalmazó perklórsav |
|||
| Egység SI és STP hiányában. | |||
A perklórsavat egy kémiai vegyület a általános képletű HClO 4Ahol a atom a klór áll a oxidációs állapotban + VII. Erős oxigénsav, amely erősségében összehasonlítható erős savakkal , például salétromsavval és kénsavval , valamint oxidálószerrel . Különösen perklorátok , elsősorban ammónium-perklorát előállítására használják, amelyet az asztronautikában széles körben alkalmazott szilárd hajtóanyagok , különösen a PCPA előállítására használnak . A perklórsav nagyon maró hatású és könnyen robbanásveszélyes keverékeket képez.
Leírás
Színtelen folyadék, erős sav és erős oxidálószer. Sóit perklorátoknak nevezzük. Ez az egyetlen klórforma, amely stabil a bázikus közeg és a kloridion közötti aránytalanság szempontjából . Dehidratálható nagyon instabil Cl 2 O 7 perklórsavanhidriddé .
Szintézis
A perklorát-ionokat a klorát- ionok elektrokémiai oxidációjával szintetizálják, és a savat a kénsav sóinak hatására nyerik .
Használ
A perklorátok fontos vegyületek a pirotechnikában, mint oxigénhordozók keverékekben. A perklórsav oldatként ellenionként használható, mivel sóinak többsége vízben oldódik, ami korlátozza a kicsapódás problémáját.
Lásd is
Kapcsolódó cikkek
Külső linkek
- fr) INRS lap
- (en) Nemzetközi biztonsági adatlap
- ( fr ) Perklorátok az Egyesült Államok élelmiszer- , környezettudományi és technológiai területén, 2008-02-13. (Egy másik FDA tanulmány átlagokat ad, de nem tartalmazza a nagy kockázatú populációkat)
Bibliográfia
- (en) Schilt, AA, 1979. Perklórsav és perklorátok . GFS Chemicals, Inc., Columbus.
- (en) Kirk-Othmer - A kémiai technológia enciklopédiája, 5. kiadás Repülési. 18. Hoboken: John Wiley és fiai; 2006: 274-284.
- (en) Budavari S (szerk.) - The Merck Index, 13. kiadás NJ: Merck and Co. Inc.; 2001.
- en) Perklórsav. In: HSDB adatbázis. Kanadai Egészségügyi és Biztonsági Központ, felülvizsgálat: 2003.02.14. Elérhető a http://www.tox-net.nlm.nih.gov címen .
- en) Perklórsav. 14. sz. Lap. In: Cheminfo Data Base. Kanadai Egészségügyi és Biztonsági Központ, átdolgozás 2003.03.24.
- en) Tűzvédelmi útmutató veszélyes anyagokhoz. NFPA (National Fire Protection Agency), 13 th ed.
- en) Perklórsav-oldat. BGIA GESTIS-adatbázis a veszélyes anyagokról. Elérhető a http://www.hvbg.de/e/bia/gestis/stoffdb/index címen . html.
- (en) York RG és mtsai. - Patkányoknak ivóvízben orálisan beadott ammónium-perklorát fejlődési neurobevaviorális vizsgálatában megfigyelt hatások finomítása. I. Pajzsmirigy és reproduktív hatások. International Journal of toxicology, 2005; 24 (6): 403-418.
- (en) York RG és mtsai. - Az ammónium-perklorát orális (ivóvíz) fejlődési toxicitási vizsgálata Új-Zéland fehér nyulain. International Journal of Toxicology, 2001; 20 (4): 199-205.
- (en) Thuett KA és mtsai. - A méhen belüli és a laktációs ammónium-perklorát expozíció hatása a pajzsmirigy szövettanára, valamint a pajzsmirigy és nemi hormonokra fejlődő szarvas egerekben (peromyscus maniculatus) a szülés utáni 21. napon keresztül. Journal of Toxicology and Environmental Health A, 2002; 65 (24): 2119-2130.
- (en) Forsberg K, Mansdorf SZ - Gyors választási útmutató a vegyszeres védőruházathoz. New York: John Wiley és fiai, 4. kiadás ; 2002.
- fr) Hajók és tározók - CNAM R 435. ajánlás. Párizs: INRS; 2008.
- (en) Leleu J, Triolet J - Veszélyes kémiai reakciók. Párizs: INRS ED 697; 2003: 15-18.
Hivatkozások
- PERKLORSAV (72% -os MEGOLDÁS) , a kémiai biztonsági nemzetközi program biztonsági adatlapja (i) , 2009. május 9-én megtekintették
- számított molekulatömege a „ atomsúlya a Elements 2007 ” on www.chem.qmul.ac.uk .
- Sigma-Aldrich által létrehozott, 2020. február 2-án megtekintett biztonsági adatlap https://www.sigmaaldrich.com/MSDS/MSDS/DisplayMSDSPage.do?country=FR&language=fr&productNumber=208507&brand=SIAL&PageToGoToURL=https2 sigmaaldrich.com% 2Fcatalog% 2Fproduct% 2Fsial% 2F208507% 3Flang% 3Dfr
- „ Perklórsav ” az adatbázis a vegyi anyagok Reptox a CSST (Quebec szervezet felelős a munkahelyi biztonság és egészségvédelem), elérhető április 25, 2009
