Perjósav
| Perjósav | |
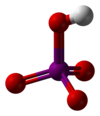 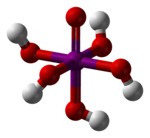 A meta- és ortoperiodikus savak szerkezete. |
|
| Azonosítás | |
|---|---|
| IUPAC név |
periodikus sav hidrogén-perjodát |
| N o CAS | |
| N o ECHA | 100 030 839 |
| N o EC | 233-937-0 |
| PubChem | 25289 |
| Kémiai tulajdonságok | |
| Brute formula |
H 5 I O 6 [izomerek] |
| Moláris tömeg | 227,9406 ± 0,0022 g / mol H 2,21%, I 55,67%, O 42,11%, |
| Fizikai tulajdonságok | |
| T ° fúzió | 122 ° C |
| Óvintézkedések | |
| WHMIS | |
 VS, C : Az oxidáló anyag oxigén felszabadításával okozza vagy elősegíti egy másik anyag égését. A besorolási kritériumok szerint 1,0% -os kibocsátás |
|
| 67/548 / EGK irányelv | |
 VS  O Szimbólumok : C : Maró O : Oxidáló R mondatok : R8 : Éghető anyaggal érintkezve tüzet okozhat . R34 : Égési sérülést okoz. S-mondatok : S26 : Ha szembe jut, bő vízzel azonnal ki kell mosni és orvoshoz kell fordulni. S45 : Baleset vagy rosszullét esetén azonnal orvoshoz kell fordulni (lehetőség szerint mutassa meg a címkét). S36 / 37/39 : Viseljen megfelelő védőruházatot, kesztyűt és szem- / arcvédőt. R mondatok : 8, 34, S-mondatok : 26, 36/37/39, 45, |
|
| Egység SI és STP hiányában. | |
A perjódsav a molekula HIO 4(metaperiodosav) vagy H 5 IO 6(ortoperiodikus sav). A molekula neve nem a „periódus” szóból származik, hanem a „jód” szóból: perjódsav (összehasonlítva a jódsavval vagy a perklórsavval ).
Híg oldatban a perjósav H + és IO 4 - ionok formájában létezik . Nagyobb koncentrációban ortoperjodinsav , H 5 IO 6 képződik. Ezt kristályos formában kaphatjuk meg. Orto-perjódsavval dehidratálhatjuk perjódsav , HIO 4 . A további melegítés diodin-pentoxid (I 2 O 5 ) és oxigén képződéséhez vezet . Nyilvánvalóan az anhidrid- heptoxid-jód nem létezik a természetben, bár szintézissel előállítható.
Lásd is
Hivatkozások
- számított molekulatömege a „ atomsúlya a Elements 2007 ” on www.chem.qmul.ac.uk .
- „ Perjódsavat ” az adatbázis a vegyi termékek Reptox a CSST (Quebec szervezet felelős a munkahelyi biztonság és egészségvédelem), elérhető április 25, 2009