Klór-metán
| Klór-metán | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  A klór-metán szerkezete |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Azonosítás | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| IUPAC név | klór-metán | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Szinonimák |
Metil-klorid- |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100 000 744 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o EC | 200-817-4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 6327 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ChEBI | 36014 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mosolyok |
CCl , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1 / CH3Cl / c1-2 / h1H3 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Megjelenés | színtelen, édeskés szagú gáz | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kémiai tulajdonságok | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brute formula |
C H 3 Cl [izomerek] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Moláris tömeg | 50,488 ± 0,003 g / mol C 23,79 %, H 5,99%, Cl 70,22%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fizikai tulajdonságok | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fúzió | -97,6 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° forráspontú | -24,2 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oldékonyság | 5 g · l -1 ( víz , 25 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
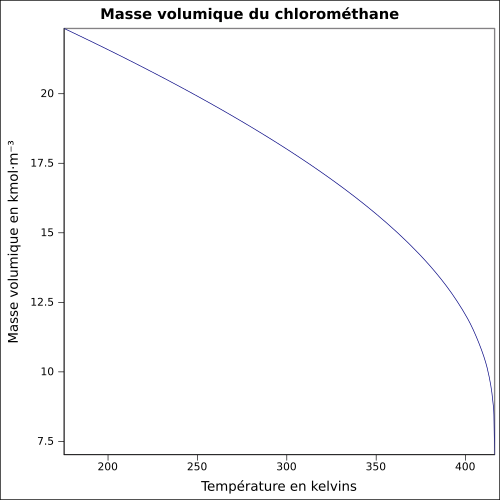
| Térfogat |
2,3065 g · l -1 ( 0 ° C , 1013 mbar )
egyenlet:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Öngyulladási hőmérséklet | 632 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Robbanási határok a levegőben | 7,6 - 19 térfogatszázalék | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Telített gőznyomás |
4,896 bar át 20 ° C-on 6,6 bar át 30 ° C-on 10,9 bar át 50 ° C-on egyenlet:

|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritikus pont | 143 ° C , 66,7 bar , 0,353 kg · l -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hármas pont | -97,71 ° C , 0,00876 bar | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termokémia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 gáz, 1 bar | 234,36 J · K -1 · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 folyadék, 1 bar | 140.08 J · K -1 · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 gáz | -83,68 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 folyadék | -102,4 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ fus H ° | 6,431 kJ · mol -1 - 175,44 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ vap H ° | 20,5 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C o |
81,2 J · K -1 · mol -1 , hogy 298 K
egyenlet:
egyenlet:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PCI | -764,0 kJ · mol -1 (gáz) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronikus tulajdonságok | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 re ionizációs energia | 11,22 ± 0,01 eV (gáz) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Óvintézkedések | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
   Veszély H220, H351, H373, H220 : Fokozottan tűzveszélyes gáz H351 : Feltehetően rákot okoz (jelölje meg az expozíciós utat, ha meggyőzően bebizonyosodik, hogy más expozíciós útvonal nem okoz ugyanolyan veszélyt) H373 : Ismétlődést követően károsíthatja a szerveket (jelölje meg az összes érintett szervet, ha ismert) expozíció vagy tartós expozíció (jelölje meg az expozíciós utat, ha meggyőzően bebizonyosodott, hogy más expozíciós út nem vezet ugyanahhoz a veszélyhez) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 4 2 0 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Szállítás | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
23 : gyúlékony gáz UN-szám : 1063 : METIL-KLORID; vagy HŰTŐGÁZ R 40 Osztály: 2.1 Címke: 2.1 : Gyúlékony gázok (megfelel az F nagybetűvel jelölt csoportoknak); Csomagolás: -  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| IARC osztályozás | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3. csoport: Emberre nézve rákkeltő hatása nem osztályozható | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ökotoxikológia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| DL 50 | 1,8 g · kg -1 (patkány, orális ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LogP | 0,91 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Szagküszöb | alacsony: 10 ppm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Egység SI és STP hiányában. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
A metil-klorid , szintén ismert, mint metil-klorid , Freon 40 vagy R40 , egy kémiai vegyület a általános képletű CH 3 Cl. Ez egy hűtőközeg, amelyet számos szintézishez reagensként is használnak.
Biogenézis és jelenlét a természetben
A halogén-alkánok ( fajok kötést tartalmazó szén - halogén ) képződnek - valószínűleg keresztül különböző biológiai folyamatok - bizonyos gombák, állatok és növények. A CH 3 Cl molekula ezért az élet lehetséges jelzőjeként javasolták, abban az esetben, ha a sziklás exobolygók atmoszférájában észlelik.
Egy enyhén sós növényi Batis maritima termel enzimet -metil-klorid-transzferáz , amely katalizálja a szintézisét CH 3 Cl S-adenozin-L-metionin és a klór. Ezt a fehérjét megtisztítottuk, majd bevittük és géntechnikával expresszáltattuk az E. coli baktériumban . Úgy tűnik, hogy aktív legyen a mikro-gombák , mint például szilvatapló , a vörös algák (pl Endocladia muricata ) vagy növényi fajok válnak lokálisan invazív , Mesembryanthemum crystallinumból , az összes ismert, hogy is termelnek CH 3 Cl., Mivel a per a növény- Arabidopsis thaliana laboratóriumi modell .
Jelenlét az univerzumban
2017-ben a CH 3 Cl molekulaa Naprendszerben és azon kívül is észleltek . Először az interferométer ALMA körül Protostar a napenergia típus IRAS16293-2422 olyan régióban, ahol a bolygók képezheti. Ezután a ROSINA spektrométerrel (a Rosetta szonda fedélzetén ) a 67P / Tchourioumov-Guérassimenko üstökösben .
A CH 3 Cl felfedezéseaz élet (ismert) keletkezését megelőző helyeken azt jelzi, hogy más határozottabb biomarkereket kell használni az élet más bolygókon való jelenlétének megállapításához. Másrészt a szerves halogénatomok az élet keletkezésében szerepet játszó kémia megértésének elemét képezhetik.
Fizikai-kémiai tulajdonságok
Diklorid hidrolizáljuk a vizet magas hőmérsékleten, hogy formában metanol CH 3 OHés hidrogén-klorid- HCl:
CH 3 Cl+ H 2 O→ CH 3 OH+ HCl .Ezt a reakciót lúgos vegyületek katalizálják. A kölcsönös reakció lehetővé teszi a CH 3 Cl előállításátmetanolban hidrogén-klorid buborékoltatásával , cink-klorid ZnCl 2 lehetséges jelenlétébenmint katalizátor jelenlétében , vagy pedig úgy, metanol és hidrogén-kloriddal 350 ° C-on a timföld Al 2 O 3 :
CH 3 OH+ HCI → CH 3 Cl+ H 2 O.Alacsonyabb hőmérsékleten a metil-klorid vízzel hidrátot képez , ami problémát jelent a hűtőrendszerekben.
használat
Diklorid előállítására használjuk a dimetildiklórszilánt Si (CH 3 ) 2 Cl 2a Müller-Rochow szintézissel :
2 CH 3 Cl+ Si → Si (CH 3 ) 2 Cl 2.A szilikonok gyártásának fontos szintetikus útja .
Reagensként használják az alkil -benzolok előállításához használt Wurtz-Fittig reakcióhoz vagy Friedel-Crafts reakcióhoz is . Fontos reagens a metilezéshez, különösen az aminok a kvaterner metil-aminok vagy hidroxilcsoportok képződéséhez, hogy étereket képezzenek .
Gyártás és szintézis
Ez a gáz által termelt klórozásával a metán és klór gáz 400 , hogy 500 ° C-on . A klórozás mechanizmusa a klór disszociációjából származó gyökökön keresztüli gyökös láncreakció. Ez a disszociáció megvalósítható hővel, fotokémiai úton vagy katalizátorokkal. Előnyös a termikus útvonal, amely egymás után következő helyettesítésekhez vezet:
CH 4 + Cl 2 → CH 3 Cl + HCI CH 3 Cl + Cl 2 → CH 2 Cl 2 + HCI CH 2 Cl 2 + Cl 2 → CHCI 3 + HCl CHCI 3 + Cl 2 → CCI 4 + HCIEnnek a reakciósornak az eredménye klór- metán , diklór-metán , kloroform és szén-tetraklorid keveréke . Ezeket a vegyületeket desztillációval elválasztjuk . A reaktorban felesleges mennyiségű metánt használnak, és inert gáz jelenlétében újrahasznosítást alkalmaznak annak elkerülése érdekében, hogy olyan területen dolgozzanak, ahol a metán-klór keverék robbanásveszélyes.
Egy másik szintetikus út az hidroklórozása a metanolt hidrogén-kloriddal. Ezt a reakciót jelenleg előnyben részesítik, mert hidrogén-kloridot fogyaszt, amelyet nehéz melléktermékként kezelni, ahelyett, hogy előállítaná, mint a klórozás esetében. Ezenkívül a szintézis önmagában klór-metán termelését eredményezi, és elkerüli a több klórozott vegyületek termelését.
Megjegyzések és hivatkozások
- számított molekulatömege a „ atomsúlya a Elements 2007 ” on www.chem.qmul.ac.uk .
- METIL-KLORID , a Kémiai Biztonság Nemzetközi Programjának biztonsági adatlapja (i) , konzultálva 2009. május 9-én
- "Metil-klorid" bejegyzés az IFA (a munkavédelemért felelős német testület) GESTIS vegyi adatbázisába ( német , angol ), hozzáférés: 2010. február 2. (JavaScript szükséges)
- (en) Robert H. Perry és Donald W. Green , Perry vegyészmérnökök kézikönyve , USA, McGraw-Hill,1997, 7 -én ed. , 2400 p. ( ISBN 0-07-049841-5 ) , p. 2-50
- (en) "Metil-klorid" , a NIST / WebBook-on , elérhető
- (a) Carl L. yaws, Handbook of Termodinamikai diagramok , Vol. 1., 2. és 3., Huston, Texas, Gulf Pub. Co.,1996( ISBN 0-88415-857-8 , 0-88415-858-6 és 0-88415-859-4 )
- (in) David R. LiDE, Handbook of Chemistry and Physics , Boca Raton, CRC,2008, 89 th ed. , 2736 p. ( ISBN 978-1-4200-6679-1 ) , p. 10-205
- IARC munkacsoportja az embert érintő rákkeltő kockázatok értékelésére , " Evaluations Globales de la Carcinogenicité pour l'Homme, Groupe 3: Unclassables as carcinogenicity to Humans " , http://monographs.iarc.fr , IARC2009. január 16(megtekintés : 2009. augusztus 22. )
- Index szám táblázat 3.1 függelék VI EK rendelet 1272/2008 (december 16, 2008)
- (in) " Metil-klorid " a ChemIDplus- on , elérhető
- " Methyl chloride " a hazmap.nlm.nih.gov címen (hozzáférés : 2009. november 14. )
- "Chloromethane" , az ESIS-en , hozzáférés: 2010. február 2
- Ni X, Hager LP, „ Batis maritima metil-klorid-transzferáz cDNS-klónozása és az enzim tisztítása ”, Proc Natl Acad Sci USA , vol. 95, n o 22,1998, P. 12866-71 ( PMID 9.789.006 , PMCID 23.635 , DOI 10,1073 / pnas.95.22.12866 )
- Ni X, Hager LP, „ A Batis maritima metil-klorid-transzferáz expressziója Escherichia coliban ”, Proc Natl Acad Sci USA , vol. 96, n o 7,1999, P. 3611–5 ( PMID 10097085 , PMCID 22342 , DOI 10.1073 / pnas.96.7.3611 )
- Nagatoshi Y, Nakamura T (2007) "Három halogenid-metil-transzferáz jellemzése Arabidopsis thaliana-ban" . Plant Biotechnol. 24: 503–506. doi: 10.5511 / plantbiotechnology.24.503.
- " A freon-40 első kimutatása csillagközi közegben ALMA-val és Rosettával " , a CNRS-en ,2017. október 2(elérhető : 2017. október 11. ) .
- (en) Edith C. Fayolle, Karin I. Öberg, K. Jes Jørgensen, Kathrin Altwegg, Hannah Calcutt et al. , „ Organohalogének protosztelláris és üstökös detektálása ” , Nature Astronomy , vol. 1,2017, P. 703-708 ( DOI 10.1038 / s41550-017-0237-7 ).
- (en) Manfred Rossberg, Wilhelm Lendle, Gerhard Pfleiderer, Adolf Tögel, Eberhard-Ludwig Dreher, Ernst Langer, Heinz Rassaerts, Peter Kleinschmidt, Heinz Strack, Richard Cook, Uwe Beck, Karl-August Lipper, Theodore R. Torkelson, Eckhard Löser, Klaus K. Beutel, Trevor Mann, klórozott szénhidrogének , Wiley-VCH Verlag GmbH & Co., al. "Ullmann ipari kémiai enciklopédiája",2006. július 15( DOI 10.1002 / 14356007.a06_233.pub2 )