Thymoma
Thymoma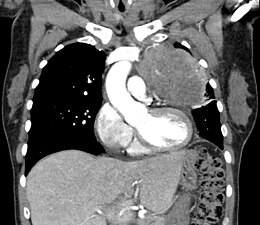 CT-vizsgálat thymomát mutat
CT-vizsgálat thymomát mutat
| Különlegesség | Onkológia |
|---|
| ICD - 10 | D15 |
|---|---|
| CIM - 9 | 164,0 |
| ICD-O | 8580 |
| BetegségekDB | 13067 |
| MedlinePlus | 001086 |
| eGyógyszer | 193809, 427197 és 888536 |
| Háló | D013945 |
A thymoma (a thymusból , az ókori görögül : θυμός , "húsos kinövés" ), vagy a timus epitheliális daganat , a szilárd daganat , amely az immunrendszer intrathoracikus szervének, a thymus rovására fejlődött ki . A timómák általában a felnőtteket érintik. Többféle van, és ezek általában tünetmentesek, de néhány olyan szisztémás betegséghez kapcsolódik, mint a myasthenia gravis ( izomgyengeséggel jellemezhető autoimmun betegség ) vagy a Good szindróma (az immunrendszer kudarca).
A diagnózist általában radiológiai elemzéssel végezzük; a kezelés elsősorban műtéti. Annak ellenére, hogy a priori jóindulatú természete thymomas, hogy a bővülés lehetőségét arra ösztönzi őket, hogy kell kezelni, mint a rák .
A timómák prognózisa a tumor típusától és stádiumától függően változik, de általában jó. A legtöbb timómát valójában korai stádiumban diagnosztizálják, ami lehetővé teszi a teljes gyógyító hatást.
Tábornok
A csecsemőmirigy szerv ismertetett óta ókori Görögország által Galen , aki látta azt a helyet a lélek . A szív és a tüdő között helyezkedik el , és etimológiáját az ókori görögből nyeri : θυμός , azaz "húsos növekedés".
A csecsemőmirigy normális működése
A thymus egy intrathoracalis szerv, amely a thymium rekeszében, az elülső mediastinumban helyezkedik el . Ez a terület a tüdő között, a szív és a nagy erek, például az aorta és ágai előtt helyezkedik el. A csecsemőmirigy két, a felső és az alsó végük kivételével, középen egyesített lebenyből áll, amelyeket tímszarvaknak neveznek. A csecsemőmirigynek van egy felszínes régiója, amelyet „kéregnek” neveznek, és mély régiója, „medulla” -nak. Születésétől a pubertásig növekszik, majd fokozatosan visszafejlődik.
Az immunrendszer szerve , a csecsemőmirigy egyes limfociták , az immunrendszer sejtjeinek érlelésére szakosodott , amelyek felelősek a normál testtől idegen sejtek (például vírus vagy rákos sejtek által érintett sejtek) felismeréséért és megsemmisítéséért. A thymus kéreg főleg ezekből a limfocitákból (más néven timocitákból), valamint néhány hám- és mezenhimális sejtből áll, míg a velő számos hámsejtből és néhány timocitából áll. A hámsejtekből alakulnak ki a timómák.
A betegség történeti felfedezése
Csak a XX . Század elején kezdődött meg a csecsemőmirigy-betegség vizsgálata. A thymás daganatok és az izomgyengeséggel jellemezhető betegség, a myasthenia gravis kapcsolatát már 1901-ben leírta Hermann Oppenheim német neurológus . Ez utóbbi a myasthenia gravis-ban szenvedő beteg boncolása során daganatot fejlesztett ki a thymás maradványok kárára. Ugyanebben az évben Carl Weigert német patológus leírta e daganatok egyikének szövettani jellemzőit. A potenciális metasztatikus karaktert 1905-ben kiemelte Edward Farquhar Buzzard .
1900-ban használta először a „thymoma” kifejezést Friedrich Wilhelm Grandhomme . A kifejezés eredetileg a thymus rekesz összes daganatára vonatkozott, függetlenül azok pontos természetétől. A " kakukkfűből " kivont kakukkfűgyökérből és a jóindulatú daganatoknak tulajdonított -ome utótagból képződött .
Az első thymectomiákat (a csecsemőmirigy eltávolítására szolgáló műtétet) Ernst Ferdinand Sauerbruch német sebész végezte el 1911-ben, nyaki megközelítéssel. 1939-ben Alfred Blalock és csapata közzétette a myasthenia gravis első remisszióját a sternotomia által végzett thymectomia után. Blalock korábban 1936-ban szternotómiával írta le a műtéti technikát.
Járványtan
A timómák ritkák, világszerte évente 100 000 lakosra 0,15 eset fordul elő . Évente körülbelül 250 új eset fordul elő Franciaországban. Ezek azonban az elülső mediastinum leggyakoribb daganatai ( az esetek 50 % -a thymoma). A tímustumorok több mint 90% -a az elülső mediastinumban található (a tüdő közötti, a szív és a nagy erek előtti régió), a többi a nyaki régióban vagy a mediastinum más régióiban található.
A férfiakat és a nőket hasonlóan érintik a timómák. Ha a thymoma myasthenia gravisszal társul, akkor főleg 30 és 40 év közötti felnőttek, és ha nincs myasthenia gravis, akkor inkább a 60 és 70 év közötti korosztályban . Ha a timómák az élet minden életkorát elérhetik, akkor ezek a daganatok nagyon ritkán fordulnak elő olyan gyermekeknél, akiknél a mediastinalis daganatoknak csak mintegy 4% -át teszik ki, nagyrészt limfómák és csírasejt-daganatok dominálják.
Nincs ismert kockázati tényező, különösen genetikai. A timómák családi jellege rendkívül ritka, és kromoszómális transzlokációval társul . Ezenkívül a timómák nem integrálódnak a több különböző rákot társító családi szindrómákkal. Úgy tűnik, hogy nincs olyan vírus-elősegítő tényező sem, amely a méhnyakrák esetében megfigyelhető .
Klinikai megnyilvánulások
Felfedezési mód
A thymoma szisztematikusan végzett mellkasröntgen során fedezhető fel . Az esetek több mint 60% -ában véletlenül fedezik fel.
A legtöbb esetben nem okoz tüneteket. Amikor azonban a daganat kifejlődött és nagy lesz, összenyomja a szomszédos szerveket: így fájdalmat okoz a mellkasban és légzési nehézségeket, vagy akár a felső vena cava szindrómát (a test felső részén található vénák látható tágulata vérrel) engorgement).
Klinikai tünetek
A timómák gyakran tünetmentesek: a betegek egyharmadától - fele nem mutat klinikai tüneteket, a diagnózist véletlenül más okból végzett vizsgálatok során állapítják meg.
Ha tünetek jelentkeznek, az esetek 50% -ában a paraneoplasztikus szindrómák és elsősorban a myasthenia gravis dominálják őket . Az intrathoracikus szervekre gyakorolt tömeges hatással kapcsolatos egyéb tünetek ( köhögés , vena cava superior szindróma, mellkasi fájdalom vagy szorító érzés , nyelési nehézség és légszomj ) a betegek 40% -át érintik. Végül a betegek körülbelül 30% -ánál jelentkeznek olyan általános tünetek, mint a fáradtság vagy a fogyás, amelyek kombinálódhatnak a már felsorolt tünetekkel.
Biológiai jelentés
Nincs specifikus mérhető vérmarker. A timoma jelenlétében azonban meg kell keresni a myasthenia gravis-hoz társuló antitesteket (anti-acetilkolin-receptor és anti-MuSK antitestek).
Képalkotás
Az elvégzett képalkotó vizsgálatok általában először mellkas röntgenfelvételt, majd mellkasi CT vizsgálatot tartalmaznak. Az értékelés során a nyirokcsomók és az áttétek behatolását kell keresni.
Mellkas röntgen
A mellkas röntgensugarával a thymás daganatok 45-80% -a látható. Elölről jól körülhatárolt, néha lebenyezett aspektust mutatnak be, amely a mediastinum egyik oldaláról vetül ki. A profil lehetővé teszi a daganat retrosternális jellegének megerősítését, és ezért annak elhelyezkedését az elülső mediastinumban. Az invázió jelei ritkák és nem feltűnőek, és főként a rekeszizom felemelkedését foglalják magukban , ami a frrenikus ideg inváziójára utal .
Mellkasi szkenner
A mellkasi CT-vizsgálat pontosabb, mint a mellkasröntgen a timómák diagnosztizálásában, a mediastinalis tömegekkel szembeni nagyobb érzékenység miatt . A jódozott kontraszttermék injekciója nem feltétlenül szükséges, de lehetővé teszi a timoma és az érrendszer közötti kapcsolat meghatározását. Ez megfontoláskor lehetővé teszi a műtéti stratégia stádiumát és tisztázását.
A timómák az elülső mediastinum jól meghatározott tömegeként jelennek meg, közel a szívburokhoz és elülső síkban, mint a nagy intrathoracicus erek (felmenő aorta és íve, tüdőartéria, vena cava superior). A tömeg lehet gömb alakú vagy lobulált, de homogén megjelenésű (ritkábban cisztás), amely az injekció beadása után növekszik, és meszesedést tartalmazhat.
A helyi invázió CT-kritériumait meg kell keresni, mert ezek irányítják a kezelést. Másrészt a CT invázió korrelál a prognózissal. A tömeg és az erek, különösen az aorta és a vena cava felső része közötti zsíros határ hiánya a helyi invázió jele. A rekeszizom kupola felemelkedése, akárcsak a mellkas röntgenfelvétele, a frénikus ideg inváziójának jele.
A daganat kontúrjainak szabálytalansága, valamint a meszesedések, nekrózis vagy intratumorális vérzés jelenléte a rossz prognózis jelei korrelálnak az agresszívebb daganatokkal.
- Szkennográfiai szempont
-
Korai stádiumú thymoma klasszikus számítógépes tomográfiai bemutatása (piros kör). Mögött az aorta, a vena cava felső része és a pulmonalis artéria látható metszetben.
-
Injektált CT-vizsgálat a mediastinalis ablakon keresztül, amely kimutatja, hogy a timstin carcinoma behatol a mediastinalis struktúrákba:
1: heterogén tumor, szabálytalan kontúrokkal, hemorrhagiás területeket mutat be;
2: felső vena cava ;
3: brachiocephalicus artériás törzs ;
4: bal subclavia és bal közös carotis artériák;
5: az aorta íve ;
6: mellcsont . -
CT-vizsgálat parenchimális ablakon keresztül, amelyen a tüdőt behatoló tímuszrák látható (emphysema elváltozásokkal) mindkét tüdővel érintkezve (1: jobb tüdő; 2: bal tüdő);
fekete nyilak: invázióval gyanús területek.
A PET-vizsgálatok helye a timómák diagnosztizálásában még mindig vitatott. Ha valóban fennáll a tumor hiperfixációja, tisztázni kell a szerepét a lokoregionális kiterjesztés diagnosztizálásában.
- B1 típusú timoma PET-vizsgálatban
-
Keresztmetszet. A három fotó ugyanarról a vizsgáról készült.
-
Elülső vágás; a daganat a vörös vonalak metszéspontjában van.
-
Nyilas vágás; a daganat a vörös vonalak metszéspontjában van.
MRI
Az MRI- t kevéssé használják a thymoma diagnózisában, de bizonyos esetekben hasznos lehet. Így az a beteg, aki a CT-vizsgálat során nem kaphat injekciót jódozott kontrasztanyagból, részesülhet az MRI-ben a lokoregionális kiterjesztés értékelése érdekében. Az MRI segíthet a másodlagosan cystizált thymoma (folyadéküreggel) megkülönböztetésében a veleszületett mediastinalis cisztától.
A timómák nem mutatnak specifikus jellemzőket az MRI-n. Az MRI-t főleg két szekvenciában elemzik, úgynevezett T1 és T2, amelyek lehetővé teszik a különböző szövetek megkülönböztetését. A T1 szekvenciában a thymoma jele közel van az izmokhoz, vagy sokkal fontosabb, mint a T2 szekvenciában, míg a T2 szekvenciában megközelíti a zsírok szignálját, ami megnehezíti a thymoma széleinek megkülönböztetését a zsír mediastinal közepén. A CT-hez hasonlóan a tumor heterogenitása agresszívebb daganatokkal is társul, de ez egy következetlen és megbízhatatlan jel, amelyet a rutin klinikák nem használnak.
Társult betegségek
A timómák leggyakrabban elszigetelten fordulnak elő. Ezeket azonban paraneoplasztikus szindróma kísérheti . Ez a kifejezés minden olyan rendellenességet felölel, amely bizonyos daganatokkal járhat. Ezek a rendellenességek nem kapcsolódnak közvetlenül a daganathoz, hanem olyan megnyilvánulások, amelyek a rák kialakulásának helyétől távol, a daganat által termelt anyag hatására jelentkeznek. Ezek ritka szindrómák, különösen az intrathoracicus és az emésztőrendszeri rákok kisebbségében fordulnak elő. A paraneoplasztikus szindróma néha kíséri a daganatot evolúciójában: gyakran megelőzi, néha visszafejlődik a kezelésével, gyógyulással eltűnik és visszaesés esetén újra megjelenik. Kezelése a felelős tumor kezeléséből áll. A thymomákban leggyakrabban előforduló paraneoplasztikus szindrómákban a myasthenia gravis dominál .
Myasthenia gravis
A Gravis egy neuromuszkuláris betegség autoimmun . Jellemzője a neuromuszkuláris csomópont károsodása, ami a csontvázcsíkolt izomzat ingadozó gyengeségéhez és a túlzott fáradtsághoz vezet .
A timómában szenvedő betegek 15 és 20% -a között a myasthenia gravis klinikai tünetei is jelentkeznek , és a betegek 25% -ánál vannak anti-acetil-kolin receptor antitestek (anti-ACh-R antitestek), tünetek nélkül. A myasthenia gravis jeleit mutató thymomában szenvedő betegek antitestjei pozitívak lesznek, és az anti-ACh-R antitestekkel társult bármilyen tünetmentes mediastinalis tömeg thymoma. Noha a statisztikai összefüggés összefüggést sugall a két patológia között, a pontos ok-okozati mechanizmus továbbra is vitatott, és számos hipotézist fontolgatnak:
- a timómában található hibás T-limfociták kiválasztása, amelyek felelősek az autoantitest hiperszekréciójáért;
- az autoantigének hibás bemutatása a thymás sejtekben, ami a felismerő T-limfociták nem eliminációjához vezet;
- specifikus csíraközpontok jelenléte a thymás parenchymában, könnyebben termelnek autoantitesteket;
- időseknél a nem specifikus autoimmunitás jelenléte.
Myasthenia gravis esetén mellkasi CT-vizsgálatot kell végezni a timoma keresése érdekében.
A thymoma nem minden típusa társul a myasthenia gravis-szal egyformán, és néhányuk még soha sem társul hozzá.
| Megfigyelt gyakoriság | |
|---|---|
| A típus | 0% |
| AB típus | 6,8% |
| B1 típus | 40% |
| B2 típus | 55,6% |
| B3 típus | 10% |
| Tímuszos karcinómák | 0% |
Good szindróma
A Good-szindróma a timómákhoz kapcsolódó szerzett immunszuppresszió , amelyet először 1954-ben írtak le. Ismételt fertőzésként nyilvánul meg. Noha nincsenek szigorú diagnosztikai kritériumok, a nemzetközi szakértői bizottságok Good szindrómáját külön egységként ismerik el és osztályozzák.
Van hypogammaglobulinaemiát (hiánya vérfehérjék résztvevő az immunrendszert a humorális válasz ) és leukopenia (deficiencia fehérvérsejtek), amely elsősorban B-limfociták és a vezető egy hiány celluláris immunitás (immun védekező mechanizmus bevonásával limfociták). A betegség kialakulásának mechanizmusa nem ismert, de valószínűleg a csontvelőben ered .
A Good-szindróma gyakorisága tanulmányok szerint változó. Egyesek szerint a timogómában szenvedő betegek 6-11% -ában van jelen hipogammaglobulinémia , és a hypogammaglobulinemiában szenvedő felnőttek körülbelül 10% -ában thymoma is van. Az eddigi legnagyobb tímustumor-kohorsz azonban a hipogammaglobulinémia kevesebb mint 1% -ának gyakoriságáról számol be.
Egyéb paraneoplasztikus szindrómák
Egyéb tünetek közé tartozik az erythroblastopenia , a Morvan-szindróma , az encephalitis és a myositis . Jelenlétüknek thymoma kereséséhez kell vezetnie, és a tünetek általában javulnak a kezeléssel. Ritkábban figyelhető meg olyan betegségek, mint a szisztémás lupus erythematosus , a reumás ízületi gyulladás , a Sjögren-szindróma vagy a fekélyes vastagbélgyulladás . Vitatott ezeknek a betegségeknek az ok-okozati összefüggése, mivel a thymoma nélküli embereknél meglehetősen gyakori betegség, és nagyon ritka azoknál.
Diagnosztikai
Diagnosztikai stratégia
Leggyakrabban a klinikailag radiológiai diagnózis elegendő, tipikusan a thymás rekeszben kialakult kicsi és jól körülhatárolt csomó esetén. Szükség lehet azonban a biopsziával végzett határozott diagnózisra (szövetminta felvétele mikroszkópos elemzés céljából) a kezelés megkezdése előtt, amennyiben jelentős helyi invázió legalábbis kezdetben lehetetlenné teszi a műtéti megközelítést. A biopsziára akkor is szükség van, ha erős kétség merül fel a timoma és a limfóma közötti diagnózisban, amelynek kezelése akkor nagyon eltérő lenne.
Szükség esetén a biopszia többféleképpen is elvégezhető. A műtéti biopsziák (főleg mediastinotomiával ) lehetővé teszik a diagnózis felállítását az esetek 90% -ában, de általános érzéstelenítést igényelnek. A szkennerrel végzett tűbiopszia nem igényel általános érzéstelenítést és kevésbé invazív, de csak az esetek 60% -ában teszi lehetővé a diagnózist. A technika megválasztása az egyes hozzáférési utak daganatának hozzáférhetősége és a beteg általános állapota szerint történik.
Differenciáldiagnózisok
Más diagnózisokat fel lehet idézni a tímusz rekeszét elfoglaló tumor előtt. Ezek lehetnek jóindulatú daganatok, például egy méhen kívüli golyva (a pajzsmirigy rendellenesen a mellkasban, nem pedig a nyakban helyezkedik el), a mellékpajzsmirigy adenoma, amely szintén méhen kívüli, de egyben lipoma vagy ' teratoma is . Érrendszeri eredet is lehetséges ( aneurysma ). Más esetekben rosszindulatú daganatok lehetnek, amelyek nem tímuszszövetből származnak, például szarkómák és szeminómák , vagy rosszindulatú vérbetegségek , például limfómák .
Kóros anatómia
Történelmi
Történelmileg a timómák szövettani osztályozása kihívást jelent a patológusok számára az azonosítás szempontjából.
Így James Ewing amerikai patológus 1916-ban azt írta, hogy „a daganatok egyetlen csoportja sem állta ki az értelmezést és osztályozást, valamint a csecsemőmirigyét. A felmerült problémák közül különösen azokra gondolunk, amelyek bonyolítják ennek a mirigynek az embriológiai és szövettani vizsgálatát, és amelyekhez viszonylagos szűkösségük és jelentős változatosságuk, valamint a betegség általános patológiájának hiányos ismeretei járulnak hozzá. thymus. "
A nemzetközi thymás malignitás érdekcsoportot (ITMIG) 2010-ben hozták létre azzal a céllal, hogy koordinálják a timómák tanulmányozását, diagnosztikai és terápiás ajánlásait.
Szövettani osztályozás
A szövettan a biológiai szövetek vizsgálata . A daganatok összefüggésében a szövetek felépítésének azonosítására összpontosít, de az általuk expresszált különféle receptorokra is, a daganatok azonosítása és osztályozása érdekében. Meghozza a bizonyosság diagnózisát és lehetővé teszi a kezelés orientálását.
A timómák fő típusaiA timómák a tímusz hámsejtjeiből fejlődnek ki, ezért globális elnevezésük „tímusz hámdaganatok”. A más típusú sejtekből kifejlesztett tímusz rekesz tumorok nem thymomák. Tehát a csecsemőmirigybe eljutó limfómákat nem szabad úgy tekinteni, mint amelyek a timómákhoz tartoznak, csakúgy, mint az elülső mediastinumban elhelyezkedő és nem natív thymus sejtekből kifejlődött daganatokat ( magányos rostos daganat , lipoma, liposarcoma, ivarsejtdaganatok .
A tímusz hámdaganatait a WHO 2003-ban frissített osztályozása szerint, majd 2015-ben tímómákként (A, AB, B1, B2 vagy B3 típus) és tímuszrákokként osztályozzák. A tímuszos neuroendokrin daganatok még egy nagyon ritka ( a tímustumorok kevesebb mint 5% -a és kevesebb, mint 200 jelentett eset ) 1972-ben leírt entitás. Az ITMIG csoport 2014-ben közzétett nemzetközi konszenzusa meghatározza azokat a kritériumokat, amelyek lehetővé teszik a szövettani altípusok.
SzövettanA WHO szövettani besorolása a timókat a beteg sejtek alakja alapján azonosítja, A típusra (ovális vagy orsó) és B típusra (dendritikus vagy epithelioid) osztva. A különböző B típusokat a timociták és az atipikus sejtek aránya különbözteti meg a limfociták mennyiségéhez viszonyítva; A B1 típusok limfocitákban gazdagabbak, a B3 típusok pedig szegényebbek. Az A és B1 típusú jellemzőkkel rendelkező timómákról azt mondják, hogy AB típusúak. A tímuszos karcinómák viszont a karcinómák általános szövettani jellemzőit mutatják .
A különböző alakzatok osztályozásához főbb és kisebb szempontok vonatkoznak.
| A típus | AB típus | B1 típus | B2 típus | B3 típus | Tímuszos karcinómák | |
|---|---|---|---|---|---|---|
| A hámsejtek alakja | fusiform | fusiform / sokszög | sokszögű | sokszögű | sokszögű | |
| Sejtes atypia | minimális | minimális | minimális | gyenge | mérsékelt | fontos |
| A limfociták mennyisége | ritka | közvetítők | bőséges | közvetítők | ritka | nagyon ritka |
A B2 típusúak a leggyakoribb timómák, a teljes mennyiség 25–28% -ával , a B1 típus pedig a legritkább ( 10–12% ). A szövettani típusok megoszlása az életkor függvényében változik (az A és AB típusok gyakoribbak az 55 évesnél idősebb betegeknél), de nem szerint.
Az A és AB típusú timómák lokálisan ritkábban invazívak, e daganatok 90% -a korai stádiumban van. Másrészt a B1 , B2 és B3 típusok lokálisan előrehaladottabbak (ezen daganatok 62% -a III . Stádiumú ).
A földrajzi eloszlásban eltérések vannak, az A és B2 típusok az Ázsiában ritkábban fordulnak elő, mint Európában és Észak-Amerikában, ellentétben az AB és B3 típusokkal . Másrészt a B1 timómák harmonikusan oszlanak meg e régiók között. Az afrikai kontinensről azonban nincs adat.
A timoma minden típusa változóan expresszál bizonyos antigéneket . Az azonosítás immunfestésével lehetővé teszi, hogy meghatározza a daganat típusa, a szövettani megjelenése önmagában, hogy néha nem elegendő.
Az anti- citokeratin antitestek egyértelműen megjelölik a timómákat, de nem teszik lehetővé a medulláris és a kortikális hámsejtek megbízható differenciálódását. A citokeratinokat elsősorban az A és B típus differenciáldiagnózisában használják.
A myasthenia gravishoz társuló timómák erősebben expresszálják a CD57 antigént. A CD5 antigén expressziója korlátozott érdeklődésű, mivel a timómák és a thymás karcinómák minden formájával kifejezhető.
| A típus | AB típus | B típus | Tímuszos karcinómák | |
|---|---|---|---|---|
| CD20 | pozitív | pozitív | negatív | negatív |
| Kalretinin | negatív | negatív | negatív | az esetek 30% -ában pozitív |
| Vimentin | pozitív | pozitív | negatív | negatív |
| Mesothelin | negatív | negatív | negatív | az esetek 30% -ában pozitív |
| CD57 | pozitív | pozitív | pozitív | negatív |
Stádium
Az onkológiában a stádium a daganatok szabványosított osztályozása helyi, regionális és távolsági kiterjedésük szerint. A leggyakrabban alkalmazott thymoma stádium nem TNM típusú, mint a szilárd daganatok többségében. A timómák nagy morfológiai változékonysága miatt a stádiumozás, hasonlóan a szövettani osztályozáshoz, az orvosi közösségben vitatott és folytatandó vita, és több stádiumot alkalmaztak egyszerre az egész világon.
Az első kísérlet a tímuszos daganatok osztályozására az evolúció szakaszaiban 1978-ból származik: Nils P. Bergh-nek és csapatának köszönhető. Három fázist hoz létre, a tumor helyi inváziójának szintjétől függően. Ezt a rendszert a következő évben a massachusettsi általános kórház csapata kissé módosította . Ezt a két besorolást kritizálják a szomszédos szervek inváziójának pontatlansága és az intratorakális vagy távoli terjesztés miatt.
Akira Masaoka japán sebész 1981-ben dolgozta ki a nevét viselő osztályozást, amelyet ezután széles körben használnak. Ez a szomszédos struktúrák invázióján és nem a daganat méretén alapuló osztályozás az első, amelynek stádiuma összefügg a túléléssel.
A Masaoka osztályozást 1994-ben úgy alakították át, hogy Masaoka-Koga osztályozássá váljon, amelyet ma a világon a leggyakrabban használnak, bár számos ponton bírálták, különös tekintettel a klinikai szempont és a mikroszkopikus aspektus összefüggésére, valamint a kétértelműség miatt. . Végül a Masaoka osztályozást nem lehet alkalmazni a thymás karcinómákra.
- Masaoka-Koga stadionok
-
Stage I
Encapsulated daganat. -
II
. Szakasz A szomszédos zsír inváziója. -
III. Szakasz
A szomszédos szervek folyamatos inváziója. -
Stage IV egy
pleurális vagy szívburok terjesztését.
E probléma orvoslására 1991-ben javasolták a TNM típus besorolását, főként a timus carcinomákra. Újabb tanulmányok azonban érvénytelenítik a tímuszrák prognosztikai jellegét. Ezért ezekre a daganatokra új osztályozást vezettek be 1994-ben.
2005-ben javaslatot tettek a thymomák új TNM osztályozására, figyelembe véve az 1991-es osztályozás tág körvonalát, de tovább meghatározva bizonyos elemeket, különösen a műtéti reszekció minőségét. Ez a besorolás validálás alatt maradt, és soha nem használták széles körben a kezelés irányítására.
2014-ben az ITMIG csoport és az International Association for Study of Lung Cancer (IASLC) új TNM osztályozást vezetett be. Első alkalommal és egy nemzetközi nyilvántartás létrehozásának köszönhetően a világ minden tájáról nagyszámú beteg irat tanulmányozható, amely részletesebb statisztikai elemzést tesz lehetővé. Valójában Bergh (1978) besorolása 43 beteg vizsgálatából származik , a Massachusettsi Általános Kórház 103 beteg vizsgálatából ; 93. Masaoka és 79 Koga . Az 1991. évi TNM osztályozás 107 betegen alapult . Ennek az alacsony betegszámnak a fő oka a timómák ritkasága, és ez a régi osztályozások határa. A timómák valójában nagy klinikai és szövettani variabilitást mutatnak, ami tükröződik ezen osztályozások bizonyos szempontjainak részleges elégtelenségében. Ezen okok miatt nemzetközileg nem vezettek be osztályozást, minden tanult társadalom saját ajánlásait adta ki azon osztályozás alapján, amelyről úgy érezte, hogy a legjobban megfelel a betegpopulációjának.
A használt adatbázis létrehozása a besorolása ITMIG összeállítja feljegyzések 1808-betegek 105 központok világszerte, és a meghatározást tartalmazza a 8 th kiadás a TNM besorolás a rosszindulatú daganatok , így ez egy nemzetközi benchmark értéket.
Kezelés
Az ITMIG csoport jelentése szerint világszerte a betegek 47,1% -át egyedül műtéttel kezelik. A műtéttel kombinált sugárterápiát a betegek 26,7% -ának ajánlják; A betegek 6,5% -a kap műtétet és kemoterápiát, végül 18,4% részesül műtétet, sugárterápiát és kemoterápiát ötvöző kezelésben. A timómákat jóindulatú daganatoknak tekintik, progressziójuk lassú, általában tünetmentes. A helyi invázió és a regionális áttétek (mellhártya és szívburok) lehetősége miatt azonban rosszindulatú daganatokra van szükségük, ezért a korai stádiumtól kezdve radikális gyógyító kezelést igényelnek.
Sebészet
JelzésekA timómák elsődleges kezelése a teljes műtéti reszekció, különösen a korai szakaszban. Mellkas műtéten esik át .
Bár a műtéti kezelésnek a lehető legteljesebb reszekcióra kell irányulnia, a tumor térfogatcsökkentő műtét ( debulking ) érdeke vitatott a thymomák esetében, amelyek lokálisan túl előrehaladottak és amelyeket lehetetlen teljesen eltávolítani. Egyes szerzők úgy vélik, hogy a hiányos reszekció, amelyet sugárterápián és kemoterápián alapuló adjuváns kezelés követ, jobb túlélést tesz lehetővé, mint a tisztán orvosi kezelés. Azonban a legtöbb vizsgálatban a túlélési növekedés kicsi, és csak két tanulmány mutat szignifikáns növekedést. Lehetséges, hogy a debulking és az adjuváns terápia előnye csak középtávon figyelhető meg, és hosszú távon eltűnik. Újabb tanulmányok viszont nem mutatnak szignifikáns növekedést a túlélésben a debulking után , inkább csak radiokemoterápiás kezelést javasolnak.
Annak érdekében, hogy felszámolja a módszertani torzításokat kapcsolódik a betegek kis száma ezekben a vizsgálatokban, a meta-analízis a 13 tanulmány , összesen 314 betegnél hajtottuk végre 2015-ben A szerzők szerint debulking javíthatja a prognózist, de fenntartásokkal az alkalmazott vizsgálatok módszertanához, a betegek kis számához és az elvégzett adjuváns kezelések nagy heterogenitásához. Egy másik fenntartás a nagy erek inváziójára és a pleurális áttétek jelenlétére vonatkozik, amelyeknek nem tűnik előnyös a kiszerelés .
Sebészeti technikákKét fő megközelítést alkalmaznak: szternotómiát ("transz-sternalis thymectomia") és videotorakoszkópiát ("video-segített timektómia", amely robot segítségével segíthet). Más, minimálisan invazív megközelítéseket is leírnak, különösen a méhnyak útján vagy - különösen gyermekeknél - mediastinoscopy segítségével . A „minimálisan invazív” kifejezés minden olyan technikát jelöl, amely nem tartalmazza a szternotómiát vagy a bordák elválasztását.
Az első útvonalat a timoma jellemzői szerint választják meg. Nincs randomizált, a két technikát összehasonlító vizsgálat ; csak a posteriori összehasonlítások állnak rendelkezésre 2016-ban. A transzsternalis megközelítés régóta maradt referencia megközelítés; Ma is felismerjük a tímuszrész kitettségének kiváló minőségét, amelyet lehetővé tesz annak teljes mélyedése érdekében. A kevésbé invazív technikák kifejlesztése azonban lehetővé tette a beavatkozás szövődményeinek és nehézségeinek csökkentését, miközben a reszekció hasonló minősége megmaradt. Videóval támogatott megközelítés ajánlott kicsi, korai stádiumú thymomák esetén, ezért lehetővé teszi a kórházi tartózkodás hosszának, a műtét utáni fájdalom és a jobb esztétikai eredmények csökkentését. Meg kell azonban jegyezni, hogy a videoszisztémás műtéten áteső betegeket pontosan a thymoma kevésbé előrehaladott jellege alapján választják ki. A posztoperatív szövődmények alacsonyabb aránya tehát egyszerűen annak tudható be, hogy ezek olyan daganatok, amelyeket technikailag könnyebb eltávolítani, a technika különös előnye nélkül.
- Először használt útvonalak
-
Középvonal sternotomia metszés transz-sternalis thymectomiához.
-
A trocarok nyílásainak bemetszése egy videós asszisztált thymectomiához bal megközelítéssel.
-
Cervicotomia metszés transz-cervicalis thymectomiához.
Technikailag mindegyik megközelítésnek vannak előnyei és hátrányai. A transz-sternalis megközelítést egy medián sternotomia végzi , a heg a szegycsont teljes magasságában fut. Ez feltárja a szegycsont fertőzésének kockázatát , és az egész mellhártyaüreg nem könnyen hozzáférhető. Másrészről, könnyen kiterjeszthető a metszés a nyakig, cervicothoracalis daganat esetén, és kivágást kell végrehajtani, amelynek el kell távolítania a szomszédos szerveket: pneumonectomia vagy pulmonalis lobectomia, valamint a mediastinum nagy erének gesztusa optimálisan nem lehetséges, mint először ezen az úton.
A videotorakoszkópos út és a robot út nagyon hasonló, a robot által segített műtét a videoműtét technológiai kiterjesztése, ahol az operátor egyszerűen szabadságfokokat nyer a műszerek manipulálásában, amelyet az intervenciós helyiségben található konzolról végeznek. A csecsemőmirigy helyett a mellcsonton keresztül az egyik mellhártyaüreg közelíti meg. A videotorakoszkópos megközelítés ezért egyhólyagos szellőzést igényel a megfelelő munkaterület felszabadítása érdekében (különben a levegővel felfújt tüdő elfoglalja az egész mellhártyaüreget, és megakadályozza a műszerek átjutását). Az egyetlen tüdő szellőzését szelektív intubáció teszi lehetővé az érzéstelenítés során. Ezen túlmenően, a befúvási alacsony nyomású CO 2 megkönnyítheti az expozíciót és a szerkezetek boncolását azáltal, hogy befejezi a tüdő eltávolítását a munkaterülettől.
Bármi legyen is a választott megközelítés, a radikális thymectomia beavatkozásának végén a thymus rekesznek üresnek kell lennie a maradék zsírtól.
A reszekció mértékeJelenleg vita folyik a kis thymomák esetében egy egyszerű thymomectomia (a thymás csomó eltávolítása) helyett egy radikális thymectomia (a thymus rekesz teljes mélyedése) elvégzésének lehetőségéről a képalkotás agresszivitásának kritériumai nélkül. A myasthenia gravis nélküli betegeknél, akiknek a timoma kicsi, önmagában a timomectomia tűnik elfogadhatónak, azonos 5 éves túléléssel. Hiányoznak azonban a hosszú távú adatok.
Bizonyos esetekben nyirokcsomó-boncolást is el kell végezni. A lokálisan előrehaladott daganatok, valamint a thymás karcinómák a nyirokcsomó-invázió forrásai: ezért a műtétnek tartalmaznia kell legalább a jobb paratrachealis és az elülső mediastinum boncolását. Ez egy olyan gesztus, amelyet videokirurgiai megközelítéssel nehézkesen lehet elérni, de a szternotómiával nem, ami az első megközelítés az ilyen típusú agresszívebb daganatok esetében. A boncolás érdeke elsősorban a lehető legmegbízhatóbb szakasz megszerzése, amely lehetővé teszi a posztoperatív kezelés irányítását. A szomszédos szervek összefüggő inváziója esetén ajánlott a daganat és a betolakodott szervek monoblokk reszekcióját végrehajtani.
A társult myasthenia gravis perioperatív kezeléseNincs nemzetközi egyetértés a myasthenia gravis perioperatív kezelésében a thymoma miatt műtött betegeknél. A témáról azonban rengeteg orvosi szakirodalom létezik, amely lehetővé teszi a különböző tanult társadalmak számára ajánlások megfogalmazását.
A miaszténikus krízis posztoperatív rizikófaktorait azonosították, amelyek magukban foglalják az anti-acetilkolin receptor antitestek jelenlétét, a B1, B2 vagy B3 típusú hisztológiákat és a hiányos reszekciót. Preoperatív myasthenia gravisban szenvedő betegeknél a myasthenia gravis visszaesése a műtét után két évvel is lehetséges; ezeknél a betegeknél a preoperatív légzési elégtelenség a myasthenia gravis kiújulásának kockázati tényezője. A műtéti stressz azonban önmagában kockázati tényező a miaszténikus krízisben.
Antikolinészteráz gyógyszereket ( különösen piridosztigmint ) gyakran adnak háttérkezelésnek a műtét előtt. Másrészt mellékhatásaik, például hányás és szívritmuszavar miatt, a műtét reggelén leállították őket. A gyógyulásnak, általában a második posztoperatív nap után, tünetekre kell irányulnia és fokozatosnak kell lennie.
Az orális kortikoszteroidok (különösen a prednizolon ) szintén gyakran a fenntartó terápia részét képezik myasthenia gravis-ban szenvedő betegeknél. A kortikoszteroid terápiához kapcsolódó műtét utáni szövődmények fokozott kockázata (elsősorban gyógyulási nehézségek) miatt mérsékelt myasthenia gravis esetén a kezelést több héttel a műtét előtt le lehet állítani. Ha az antikolinészteráz-kezelés önmagában nem elegendő a tünetek kezelésére, akkor átmenetileg más típusú kezelések is végrehajthatók, például a plazmaferezis , amely elvben a tünetektől függetlenül is elvégezhető. Azoknál a betegeknél, akik műtét előtt hosszú ideig kortikoszteroidokat kaptak, a kezelést korán el kell kezdeni. Operatív posztoperatív akut myasthenikus krízis esetén óvintézkedésekkel rövid, nagy dózisú intravénás kortikoszteroid terápia végezhető.
Súlyos myasthenia gravis esetén a plazmaferezis több szakasza ( általában 3-5 ) elvégezhető a műtét előtt. A hatékonyság körülbelül egy hét alatt figyelhető meg, és 1-3 hónapig tart .
Operáció után súlyos myasthenicus krízis hiányában immunglobulinokkal történő kezelés nem ajánlott .
Multimodális kezelés
A thymomák alacsony gyakorisága miatt kevés randomizált vizsgálat áll rendelkezésre vagy megvalósítható, ami korlátozza a kezelési módszerekről rendelkezésre álló adatokat, és elsősorban az úgynevezett adjuváns kezelés indikációit.
Az adjuváns terápia kemoterápia vagy sugárterápia, amelyet műtét után végeznek a kiújulás kockázatának csökkentése érdekében, míg a neoadjuváns terápia a műtét előtt történik, hogy növelje a daganat reszekcióképességét. Különböző tanult társadalmak vezetési ajánlásokat fogalmaztak meg, amelyek változhatnak. Ezeket a következő táblázat foglalja össze:
| Sebészet | Sugárterápia | Kemoterápia | |
|---|---|---|---|
| I. szakasz | igen, egyedül | nem | nem |
| II. Szakasz | Igen | tárgyalt neoadjuváns, amelyet a helyi kiújulás magas kockázatainak kell fenntartani | nem |
| III. Szakasz | Igen |
kemoterápiával társított neoadjuváns a daganat méretének csökkentése érdekében, ha kétség merül fel a reszekcióval kapcsolatban; adjuváns , hiányos reszekció esetén |
adjuváns, hiányos reszekció esetén |
| IVa szakasz | igen, ha teljes reszekció lehetséges | kemoterápiával párosítva, ha műtét nem lehetséges | neoadjuváns |
| Szakasz IVb | nem | nem | igen, egyedül |
Míg a timómák egészében még előrehaladott stádiumban is meglehetősen kemoszenzitívek, a jelenlegi tudományos adatok nem támasztják alá önmagában a kemoterápiával végzett adjuváns kezelést. A korai szakaszban ( Masaoka I és II ) a műtét továbbra is a szokásos kezelés, és hiányos reszekció esetén kiegészíthető adjuváns sugárterápiával. A fejlettebb szakaszokban ( Masaoka III és Iva, valamint timus carcinoma) és neoadjuváns módon adjuváns radiokemoterápia ajánlott, önmagában a kemoterápia nem teszi lehetővé a túlélés növekedését.
A javasolt kemoterápiák gyakran ciszplatinon alapulnak , amely gátolja a replikációt és a rákos sejtek preferenciális sejtpusztulását váltja ki .
A thymomák esetében nem áll rendelkezésre célzott terápia .
Franciaországban van egy speciális hálózat, amelyet RYTHMIC-nek hívnak, és amelyet az INCa hozott létre, és amelynek feladata nemzeti referenciarendszer létrehozása az ellátásról, ugyanakkor kéthavonta országos multidiszciplináris konzultációs értekezlet (RCP) irányítása, a betegek tájékoztatása és a kutatás felügyelete.
A helyi kiújulás speciális esete
A timómák megismétlődésének aránya az első műtéti kezelés után 10 és 29% között van , és a kiújulás gyakran több évvel a műtét után következik be. A lokális kiújulások a teljes műtéti reszekció után is a kiújulási módok 5% -át teszik ki, és főleg a III. Vagy IV .
A visszatérő thymomák kezelése világos konszenzus nélkül vita tárgyát képezi. A helyi kiújulások kezelése ismét műtéti lehet, vagy sugárterápián vagy kemoterápián alapulhat. A műtét állhat az elváltozások egyszerű reszekciójából, vagy kombinálható intraoperatív kemoterápiával a hipertermikus intrapleurális kemoterápia (CHIT) részeként. A 2014-ben elvégzett és 11 tanulmányra kiterjedő metaanalízis kedvezőbb hosszú távú prognózissal zárult le újraoperáció esetén, annak ellenére, hogy a reszekció gyakran hiányos volt. A randomizált vizsgálatok hiányához és a betegség ritkaságához kapcsolódó módszertani fenntartások azonban kifejeződnek. Amikor további műtét nem lehetséges, általában önmagában kemoterápiát javasolnak.
Előrejelzés és nyomon követés
Prognosztikai tényezők
Abban az időben a diagnózis, a betegek közölt 40% -ában egy I. stádiumú daganat Masaoaka, 25% egy szakaszban II vagy III , 10% egy szakaszban IVa, és csak 1-2% a szakaszban IVb .
A fő prognosztikai tényező a lokális kiterjesztés a diagnózis idején, majd az életkor és a műtéti reszekció minősége. A szövettani diagnózist illetően a thymás karcinómák rosszabb prognózissal rendelkeznek, mint más típusú thymomák. A masaoka stádium és a szövettani természet két független prognosztikai tényező. A myasthenia gravis vagy a paraneoplasztikus szindróma jelenléte nem befolyásolja a prognózist. Kiújulás esetén a másodlagosan megjelenő elváltozások száma prognosztikai tényező.
Ismétlődés és nyomon követés
A kiújulások körülbelül 90% -a pleurális áttétek formájában jelentkezik; a myasthenia gravis megjelenése vagy újbóli megjelenése megismétlődésre utalhat. Bizonyos szövettani típusoknál nagyobb a kockázat a kiújulás kockázatának a kezelés után, az A és AB típusok az esetek 1-2% -ában visszatérnek , szemben a B1, B2 és B3 típusok 2-7% -ával , a túlélésben nincs különbség ezen altípusok között. A diagnózis időpontja szintén megjósolja a kiújulást.
A kiújulások gyakran késői jellege miatt egyesek a kezdeti kezelés után 10 évig tartó rendszeres ellenőrzést javasolnak annak korai felismerése és kezelése érdekében. Az ajánlott nyomon követés éves mellkasi CT-vizsgálatból áll, néhány a magas biológiai markerek monitorozásával is a diagnózis idején.
Prognózis
A műtéti reszekció utáni 5 éves túlélés még a betegség előrehaladott stádiumában szenvedő betegek számára is jó.
A 15 éves általános túlélés kiváló a korai szakaszban. A fejlettebb stádiumokban alacsonyabb, de ezek a betegek a helyi invázió miatt nem mindig tudtak profitálni az optimális műtétből. A hosszú távú túlélés az 1980-as évek óta növekszik , a korábbi diagnózis és az új műtéti technikáknak köszönhetően a teljes tumoreltávolítás elérése érdekében. A halál oka a betegek kapcsolódik thymoma a 19-58% -ában függően a sorozat, hogy egy operatív komplikáció , 2 és 19% -ában, a fejlesztés a myasthenia gravis a 16. és 27.% -ában, és a Az esetek 8–47 % -a a timómával vagy annak kezelésével nem összefüggő okokat okoz. E számadatok heterogenitása megmutatja, hogy a kezelések hogyan fejlődtek a XX . Század második fele óta , megnehezítve a betegek homogén kohorszainak hosszú távú nyomon követését. Ráadásul, amint azt a nemzetközi osztályozás létrehozásának nehézségei leírtak fentebb kifejtették, ezek gyakran kicsi, meglehetősen heterogén betegcsoportok.
A kiújulás nélküli túlélés talán jobb eszköz a kezelések hatékonyságának mérésére, mert mentes a timómával és kezelésével nem összefüggő halálokoktól. Az alábbi táblázat összehasonlítja a teljes túléléssel.
| 15 éves teljes túlélés | 10 éves kiújulásmentes túlélés | |
|---|---|---|
| I. szakasz | 78% | 92% |
| II. Szakasz | 73% | 87% |
| III. Szakasz | 30% | 60% |
| IV. Szakasz | 8% | 35% |
Megjegyzések és hivatkozások
Megjegyzések
- Az etimológiáról a következő Wikiszótár cikkekben olvashat : θυμός , thymus , -ome és thymoma .
- hámsejtek és a mezenchimasejtek azok a sejtek, amelyek a testszövetek két fő típusát alkotják, az epitheliát és a kötőszövetet .
- " A daganatok egyetlen csoportja sem állt ellen sikeresebben az értelmezési és osztályozási kísérleteknek, mint a csecsemőmirigyé. Az érintett problémák közé tartoznak azok, amelyek bonyolítják a mirigy embriológiai és szövettani vizsgálatát, míg további nehézségek adódnak a daganatok összehasonlító ritkaságából és jelentős változatosságából, valamint a csecsemőmirigy általános patológiájának kissé tökéletlen ismeretéből. "
- TNM-osztályozások három kritériumon alapulnak: daganatméret (T), nyirokcsomó-érintettség (N), valamint metasztázisok jelenléte és elhelyezkedése (M).
- extrapulmonalis áttétek nagyon ritkák.
Hivatkozások
-
(in) Mr. Nishino, SKAshiku, ON Kocher, RL Thürer PM Boisselle és H. Hatabu, " A Thymus: átfogó felülvizsgálatát " , RadioGraphics , vol. 26, n o 22006. március-április, P. 335–48 ( DOI 10.1148 / rg.262045213 , online olvasás , hozzáférés : 2016. április 5. ).

-
(in) Vincent Geenen , " A csecsemőmirigy 2013-ban: egy" vestigialis "szervtől az immunológiai ön-tolerancia és autoimmunitásig " , Proceedings of the Royal Belgian Academy of Medicine., Brüsszel, Belgium Royal Academy of Medicine, vol. 3,2014, P. 171-193 ( ISSN 2034-7626 , online olvasás [PDF] ).
 Ugyanazon szerző és ugyanazon témában, de franciául: a cikk összefoglalása , konferencia 2013-ban a youtube-on .
Ugyanazon szerző és ugyanazon témában, de franciául: a cikk összefoglalása , konferencia 2013-ban a youtube-on .
- A. de Mascarel, M. Parrens, JF. Goussot és H. Bégueret, „ Az anterior mediastinum tumorai - Thymus epithelialis tumorok ” , a Respir.com oldalon ,2002. április 26(megtekintve 2016. május 29-én )
- „ Mi a thymus rák? " On Canadian Cancer Society (hozzáférés: 2016. április 26. ) .
- " Le Thymus " , a Canadian Cancer Society-től (hozzáférés : 2016. április 26. ) .
-
(in) P. Tosi, R. Kraft, P. Luzi, Mr. Cintorino, G. Fankhauser MW Hess és H. Cottier, " az emberi csecsemõmirigy invúziós mintázatai. I A kérgi terület nagysága az életkor függvényében. ” , Klinikai és kísérleti immunológia , vol. 47, n o 21982. február, P. 497-504 ( PMID 7075032 , online olvasás , hozzáférés : 2016. április 10. ).

- Fujii 2011 .
-
(en) Marius Raica, Anca Maria Cimpean és Domenico Ribatti, „ Myasthenia gravis és a csecsemőmirigy. Történelmi áttekintés ” , Klinikai és kísérleti orvoslás , Springer Science + Business Media, vol. 8, n o 22008. június, P. 61-64 ( ISSN 1591-8890 , DOI 10.1007 / s10238-008-0158-y , online olvasás ).

- (De) C. Weigert, " Pathologisch-Anatomischer Beitrag zur Erb'schen Krankheit (Myasthenia gravis) " , Neurologisches Centralblatt , n o 20,1901, P. 597-601.
- Detterbeck & Parsons 2004 .
-
(in) H. Reid és R. Marcus, " thymoma. 5 esetről szóló jelentéssel ” , British Journal of Surgery , vol. 36., n o 143.,1949. január, P. 271-279 ( DOI 10.1002 / bjs.1800361430 , online olvasás , hozzáférés : 2016. április 5. ).

- " A daganatok nomenklatúrája " , a Campus d'Anatomie Pathologique - Francia Pathológus Kollégium (CoPath) (megtekintve : 2016. április 25. ) .
-
(in) Alfred Blalock, MF Mason, HJ Morgan és SS Riven, " A régió myasthenia gravis és tímustumorai - Jelentés egy dobozról a qui Was tumor eltávolításakor " , Annals of Surgery , vol. 110, n o 4,1939. október, P. 544-561 ( PMCID PMC1391425 , online olvasás , hozzáférés : 2016. április 10 ).

- Srirajaskanthan et al 2008 .
- (en) Annikka Weissferdt és Cesar A. Moran, „A thymás epitheliális neoplazmák stádiuma: Thymoma és thymic carcinoma ” , Patológia - kutatás és gyakorlat , Elsevier BV, vol. 211, n o 1,2015. január, P. 2–11 ( ISSN 0344-0338 , DOI 10.1016 / j.prp.2014.06.007 , online olvasás ).
- " Thymomas: a CHU de Lyon jelölt INCA " , a Réseau Chu ,2012. március 8(megtekintve : 2016. május 29. ) .
- " Betegek " a Network thymus tumorok és a rák (ritmikai) (hozzáférhető a 1 st június 2016 ) .
- " timómasejteket " szóló Orpha , frissített március 2011 (megajándékozzuk 1 -jén június 2016 ) .
-
(en) Annabelle L. Fonseca, Doruk E. Ozgediz, Emily R. Christison-Lagay, Frank C. Detterbeck és Michael G. Caty: „ Gyermek thymomák: két eset jelentése és az irodalom átfogó áttekintése ” , Pediatr Surg Int , Springer Science + Business Media, vol. 30, n o 3,2013. december 10, P. 275-286 ( ISSN 0179-0358 , DOI 10.1007 / s00383-013-3438-x , online olvasás ).

-
(in) J. és K. Jaggers Balsara, " Mediastinalis tömegek gyermekeknél " , Szemináriumok a mellkasi és szív- és érrendszeri sebészetben , Elsevier, vol. 16, n o 3,2004 ősze, P. 201-208 ( PMID 15619186 , online olvasás , hozzáférés : 2016. április 10. ).

- " A thymus tumorok kockázati tényezői ", a Canadian Cancer Society részéről (hozzáférés : 2016. április 26. ) .
- (in) Frederick Nicodemus, Sandrine Geffroy, Massimo Conti, Bruno Delobel, Valerie Soenen, Nathalie Grardel Henri Porte, Marie-Christine Copin, Jean-Luc Lai és Joris Andrieux, " A timoma és autoimmun betegségek előfordulása az alkotmányos transzlokációval (14; 20) (q24,1; p12,3) ” , Gének kromoszóma. Cancer , Wiley-Blackwell, vol. 44, n o 22005. október, P. 154-160 ( ISSN 1045-2257 , DOI 10.1002 / gcc.20225 , online olvasás ).
-
(en) Roland Penzel, Josef Hoegel, Waltraud Schmitz, Hendrik Blaeker, Alicia Morresi-Hauf, Sebastian Pieper, Erich Hecker, Gunhild Mechtersheimer, Herwart F. Otto és Ralf Rieker J., " Clusters kromoszómális egyensúlyhiány thymus epiteliális tumorok társítva a WHO osztályozásához és a Masaoka szerinti állomásrendszerhez ” , International Journal of Cancer , Wiley-Blackwell, vol. 105, n o 4,2003. április 18, P. 494-498 ( ISSN 0020-7136 , DOI 10.1002 / ijc.11101 , online olvasás ).

-
(in) Xinxin Zhang Tao Wang, Wei Wang Yibing Ding Lixing Zhou Qiuyan Chen Xiang Gao Yongzheng Wu, Yuna Mei Yu Jin, Qian Gao és Long Yi " családi emlőrák Van-e és a timómában utal-e rák szindrómára? Családi perspektíva ” , Gene , Elsevier BV, vol. 573, n o 22015. december, P. 333-337 ( ISSN 0378-1119 , DOI 10.13039 / 501100002949 , online olvasás ).

-
(in) Biao Liu, Qiu Rao, Yun Zhu, Bo Yu, Hai-Yan Zhu és Xiao-jun Zhou, " a mediastinum metaplasztikus timoma " , American Journal of Clinical Pathology , Oxford University Press (OUP), vol. 137, n o 22012. február, P. 261-269 ( ISSN 0002-9173 , DOI 10.1309 / ajcp0t1jfylmphmi , online olvasás ).

-
(in) Manuel López Cano, Jose M Ponseti-Bosch, Eloi Espin-Basany Jose L Sanchez-Garcia és Armengol, Manuel Carrasco, " A thymoma-Associated myasthenia gravis kimenetelének klinikai és kóros előrejelzői " , The Thoracic Surgery Annals , Elsevier BV, vol. 76, n o 5,2003. november, P. 1643-1649 ( ISSN 0003-4975 , DOI 10.1016 / s0003-4975 (03) 01139-1 , online olvasás ).

-
(en) Yoshitaka Fujii , „ A csecsemőmirigy, a thymoma és a myasthenia gravis ” , Surgery Today , Springer, vol. 43, n o 5,2013 május, P. 461-466 ( DOI 10.1007 / s00595-012-0318-2 , online olvasás , hozzáférés : 2016. április 10. ).

- Marom 2010 .
-
(en) Carlos S. Restrepo, Meenakshi Pandit, Isabel C. Rojas, Miguel A. Villamil, Hernan Gordillo, Diego Lemos, Luciano Mastrogiovanni és Lisa Diethelm: „ A csecsemőmirigy kiterjedt elváltozásainak képalkotó megállapításai ” , Aktuális problémák in Diagnostic Radiology , Elsevier BV, vol. 34, n o 1,2005. január, P. 22–34 ( ISSN 0363-0188 , DOI 10.1067 / j.cpradiol.2004.10.001 , online olvasás ).

-
(in) Erin Casey, Patrick J. Kiel és Patrick J. Loehrer, " a betegek klinikai ellátása thymoma " , Hematológiai \ / Oncology Clinics of North America , Elsevier, vol. 22, n o 3,2008. június, P. 457-473 ( ISSN 0889-8588 , DOI 10.1016 / j.hoc.2008.03.010 , online olvasás ).

- Wright 2008 .
-
(in) Noriyuki Tomiyama, Nestor L. Müller, Samantha J. Ellis, Joanne R. Cleverley Meinoshin Okumura, Shinichiro Miyoshi, Masahiko Kusumoto, Takeshi Johkoh, Shigeyuki Yoshida, Naoki Mihara, Osamu Honda, Takenori Kozuka Seiki és Hironobu „ Invazív és noninvazív thymoma: megkülönböztető CT jellemzők ” , Journal of computed assisted tomography , Lippincott Williams & Wilkins, Inc., vol. 25, n o 3,2001. május-június, P. 388-393 ( PMID 11351188 , online olvasás , hozzáférés : 2016. április 17. ).

-
(in) Elena Scagliori Laura Evangelista Analori Panunzio, Fiorella Calabrese, Nasarena Nannini, Roberta Polverosi és Fabio Pomerri, " A számítógépes tomográfia (CT) és a pozitronemissziós tomográfia (PET) / CT konfliktusos vagy kiegészítő szerepe a thymás rák értékelésében és thymoma: tapasztalataink és irodalmi áttekintésünk ” , Thoracic Cancer , Wiley-Blackwell, vol. 6, n o 4,2015. július, P. 433-442 ( DOI 10.1111 / 1759-7714.12197 , online olvasás , hozzáférés : 2016. április 18. ).

- (en) Meinoshin Okumura, Shinichiro Miyoshi, Yoshitaka Fujii , Yukiyasu Takeuchi, Hiroyuki Shiono, Masayoshi Inoue, Kenjirou Fukuhara, Yoshihisa Kadota, Hisashi Tateyama, Tadaaki Eimoto és Hikaru Matsaluda osztályozása Funkció és jelentőség és Hikaru Matsaluda, " az emberi tímiás hám neoplazmáiról " , The American Journal of Surgical Pathology , Ovid Technologies (Wolters Kluwer Health), vol. 25, n o 1,2001. január, P. 103-110 ( ISSN 0147-5185 , DOI 10.1097 / 00000478-200101000-00012 , online olvasás ).
- (in) RA Jó, " Agammaglobulinaemia - a természet provokatív kísérlete " , Bulletin of the University of Minnesota , vol. 26,1954, P. 1-19.
-
(en) Mark Henry Joven, Melvin P. Palalay és Charlie Y Sonido, „ Esettanulmány és irodalmi áttekintés a Good-szindrómáról, a timómákkal társított szerzett immunhiány egyik formájáról. ” , Hawai'i Journal of Medicine & Public Health , University Clinical, Education & Research Associates (UCERA), vol. 72, n o 22013 február, P. 56-62 ( ISSN 2165-8218 , PMID 23467629 , online olvasás , hozzáférés : 2016. április 18 ).

- (in) Fred S. Rosen, Martha Eibl, Chaim Roifman, Alain Fischer, John Volanakis, Fernando Aiuti Luigi Notarangelo, Tadamitsu Kishimoto, Igor B. Resnick, Lennart Hammarstrom Reinhard Seger, Helen Chapel, Max D. Cooper, Raif S. Geha, Robert A. Good, Thomas A. Waldmann és Ralph JP Wedgwood, „ IUIS tudományos bizottság elsődleges immunhiányos betegségekről szóló jelentése ” , Klinikai és kísérleti immunológia , Wiley-Blackwell, vol. 118, n o S1,1999. október, P. 1-28 ( ISSN 0009-9104 , DOI 10.1046 / j.1365-2249.1999.00109.x , online olvasható ).
- (in) P. Kelleher: " Mi a Good szindróma? Immunológiai rendellenességek timómában szenvedő betegeknél ” , Journal of Clinical Pathology , BMJ, vol. 56, n o 1,1 st január 2003, P. 12-16 ( ISSN 0021-9746 , DOI 10.1136 / jcp.56.1.12 , online olvasás ).
- (en) James Huang, Usman Ahmad, Alberto Antonicelli, Ann Christine Catlin, Wentao Fang, Daniel Gomez, Patrick Loehrer, Marco Lucchi, Edith Marom, Andrew Nicholson, Enrico Ruffini, William Travis, Paul Van Schil, Heather Wakelee, Xiaopan Yao és Frank Detterbeck, „ A nemzetközi thymicus malignitás érdekcsoport nemzetközi adatbázisának fejlesztése: példátlan erőforrás egy ritka daganatos csoport tanulmányozásához ” , Journal of Thoracic Oncology , Elsevier BV, vol. 9, n o 10,2014. október, P. 1573-1578 ( ISSN 1556-0864 , DOI 10.1097 / jto.0000000000000269 , online olvasás ).
- (in) Amelia eevee és Eric Lancaster, " Paraneoplasztikus zavaroktól szenvedő betegek thymoma " , Journal of Thoracic Oncology , Elsevier, vol. 9, n o 9,2014. szeptember, S143-S147 ( ISSN 1556-0864 , DOI 10.1097 / jto.000000000000000300 , olvassa el online ).
- (in) David Blumberg, Jeffrey L. Port, Benny Weksler, Ruby Delgado, Juan Rosai, Manjit S. Bains, Robert J. Ginsberg, Nael Martini, Patricia McCormack, Valerie Rusch és Micahel E. Burt, „ Thymoma : A túlélést előrejelző tényezők többváltozós elemzése ” , The Annals of Thoracic Surgery , Elsevier BV, vol. 60, n o 4,1995. október, P. 908-914 ( ISSN 0003-4975 , DOI 10.1016 / 0003-4975 (95) 00669-c , online olvasás ).
- (in) Katrina H. Moore, Paul R. McKenzie, Catherine W. Kennedy és Brian C. McCaughan, " thymoma: trendek az idő múlásával " , The Annals of Thoracic Surgery , Elsevier BV, vol. 72, n o 1,2001. július, P. 203-207 ( ISSN 0003-4975 , DOI 10.1016 / s0003-4975 (01) 02633-9 , online olvasás ).
- (a) James Ewing , daganatos betegségek: egy értekezést a tumorok , Philadelphia; London, WBSaunders,1922, 2 nd ed. ( 1 st ed. 1916), 1053 o. ( online olvasható ) , fej. XLVI („A csecsemőmirigy és a daganatok”) , p. 912.
- (in) Frank Detterbeck és Robert Korst, " The International Thymic Malignancy Interest Group Thymic Initiative: A thymic malignitások korszerű vizsgálata " , Szemináriumok a mellkasi és szív- és érrendszeri műtétekben , Elsevier BV, vol. 26, n o 4,2014, P. 317-322 ( ISSN 1043-0679 , DOI 10.1053 / j.semtcvs.2015.02.002 , online előadás ).
- (in) Michael A. den Bakker, Alexander Marx, Kiyoshi Mukai és Philipp Ströbel, " A mediastinum mezenkimális tumorai - I. rész " , Virchows Archiv , Springer Science + Business Media, Vol. 467, N o 5,2015. szeptember 10, P. 487-500 ( ISSN 0945-6317 , DOI 10.1007 / s00428-015-1830-8 , online olvasás ).
- Marx és mtsai 2015 .
- (in) Travis WD, Brambilla, E., Burke AP, Marx és A. Nicholson AG, a WHO osztályozása a tüdő, a pleura, a csecsemőmirigy és a szív daganataiban. Negyedik kiadás , Lyon, Nemzetközi Rákkutató Ügynökség,2015, 412 p. ( ISBN 978-92-832-2436-5 , online olvasás ).
- " A thymus rosszindulatú daganatai " , a Canadian Cancer Society-től (hozzáférés : 2016. április 26. ) .
- (in) Juan Rosai és Enrique Higa, " mediastinalis endokrin daganatok, valószínűleg csecsemőmirigy eredetű kapcsolatos carcinoid tumor. 8 eset klinikopatológiai vizsgálata ” , Cancer , American Cancer Society, vol. 29, n o 4,1972. április, P. 1061-1074 ( ISSN 1097-0142 , online olvasás , konzultáció 2016. április 25-én ).
- (in) Meinoshin Okumura, Hiroyuki Shiono, Masato Minami Masayoshi Inoue, Tomoki Utsumi, Yoshihisa Kadota és Yoshiki Sawa, " A thymás epitheliális daganatok klinikai és patológiai aspektusai " , Általános mellkasi és szív- és érrendszeri műtét , Springer Science + Business Media, Vol. 56, n o 1,2008. január, P. 10-16 ( ISSN 1863-6705 , DOI 10.1007 / s11748-007-0177-8 , online olvasás ).
- (en) Cleo-Aron Weis, Xiaopan Yao, Yanhong Deng, Frank C. Detterbeck, Mirella Marino, Andrew G. Nicholson, James Huang, Philipp Ströbel, Alberto Antonicelli és Alexander Marx: „ A thymoma hatása Histotype on Prognosis in a Worldwide Database ” , Journal of Thoracic Oncology , Elsevier BV, vol. 10, n o 22015. február, P. 367-372 ( ISSN 1556-0864 , DOI 10.1097 / jto.0000000000000393 , online olvasás ).
- (en) Borislav A. Alexiev, Cinthia B. Drachenberg és Allen P. Burke, „ Thymomas: citológiai és immunhisztokémiai vizsgálat, különös tekintettel a limfoid és neuroendokrin markerekre ” , Diagnostic Pathology , BioMed Central Ltd., vol. 11,2007. május, P. 2-13 ( ISSN 1746-1596 , DOI 10.1186 / 1746-1596-2-13 , online olvasás , hozzáférés : 2016. április 25. ).
- „ Staging ” , a Canadian Cancer Society-től (hozzáférés : 2016. május 13. ) .
- (in) Akira Masaoka, " Thymoma staging system " , Journal of Thoracic Oncology , Elsevier BV, vol. 5, n o 10,2010. október, S304-S312 ( ISSN 1556-0864 , DOI 10.1097 / jto.0b013e3181f20c05 , olvassa el online ).
- (en) Sandra Tomaszek, Dennis A. Wigle, Shaf Keshavjee és Stefan Fischer, „ Thymomas: Review of Current Clinical Practice ” , The Annals of Thoracic Surgery , Elsevier BV, vol. 87, n o 6,2009. június, P. 1973-1980 ( ISSN 0003-4975 , DOI 10.1016 / j.athoracsur.2008.12.095 , online olvasás ).
- (en) Pier Luigi Filosso, Enrico Ruffini, Paolo Olivo Lausi, Marco Lucchi, Alberto Oliaro és Frank Detterbeck, „ Történelmi perspektívák: A thymás hámdaganatok stádiumrendszerének evolúciója ” , Lung Cancer , Elsevier BV, vol. . 83, n o 22014 február, P. 126-132 ( ISSN 0169-5002 , DOI 10.1016 / j.lungcan.2013.09.013 , online olvasás ).
- (en) NP Bergh, P. Gatzinsky, S. Larsson, P. Lundin és B. Ridell, „ A csecsemőmirigy és a csecsemőmirigy régió tumorai: I. Thymomák klinikopatológiai vizsgálata ” , A mellkasi sebészet Annals , Elsevier BV, vol. 25, n o 21978. február, P. 91-98 ( ISSN 0003-4975 , DOI 10.1016 / s0003-4975 (10) 63498-4 , online olvasás ).
- (in) Earle W. Wilkins és Benjamin Castleman, " thymoma: Folyamatos felmérés a Massachusettsi Általános Kórházban " , The Annals of Thoracic Surgery , Elsevier BV, vol. 28, n o 3,1979. szeptember, P. 252–256 ( ISSN 0003-4975 , DOI 10.1016 / s0003-4975 (10) 63114-1 , online olvasás ).
- (en) Akira Masaoka, Yasumasa Monden, Kazuya Nakahara és Tsuneo Tanioka, „A timómák nyomon követése, különös tekintettel a klinikai stádiumokra ” , Cancer , American Cancer Society, vol. 48, n o 11,1 st december 1981, P. 2485-2492 ( ISSN 1097-0142 , online olvasás , konzultáció 2016. április 25-én ).
- Koga és mtsai 1994 .
- (in) Frank C. Detterbeck, Andrew G. Nicholson, Kazuya Kondo, Paul Van Schil és Cesar Moran, " The Masaoka-Koga Internship Classification for Thymic Malignancies: Clarification and Definition of Definitions " , Journal of Thoracic Oncology , Elsevier BV, repülési. 6, n o 7,2011. július, S1710-S1716 ( ISSN 1556-0864 , DOI 10.1097 / jto.0b013e31821e8cff , olvassa el online ).
- (in) Cesar A. Moran, Garrett Walsh, Saul Suster és Larry Kaiser, " Thymomas II " , American Journal of Clinical Pathology , Oxford University Press (OUP), vol. 137, n o 3,2012. március, P. 451-461 ( ISSN 0002-9173 , DOI 10.1309 / ajcp36alguzwosea , online olvasás ).
- (a) Colin B. Begg, Laura D. Cramer, ES Venkatraman és Juan Rosai, " Összehasonlítva a tumor és a besorolási rendszerek: esettanulmány és felülvizsgálatot a kérdések, segítségével thymoma egy modell " , Statistics in Medicine , vol . 19, n o 15,2000. augusztus, P. 1997-2014 ( ISSN 1097-0258 , online olvasás , konzultáció 2016. április 25-én ).
- (en) Ryosuke Tsuchiya, Kenji Koga, Yoshihiro Matsuno, Kiyoshi Mukai és Yukio Shimosato, „ Thymic carcinoma: javaslat patológiás TNM-re és stádiumra ” , Pathology International , Japán Patológiai Társaság és John Wiley & Sons Australia, Ltd , vol. 44, n o 7,1994. július, P. 502-512 ( ISSN 1440-1827 , online olvasás , konzultáció 2016. április 25-én ).
- (in) Annikka Weissferdt és Cesar A. Moran, " Thymic Carcinoma, 1. rész: A 65 eset klinikopatológiai és immunhisztokémiai vizsgálata " , American Journal of Clinical Pathology , Oxford University Press, Vol. 138, n o 1,2012. július, P. 103–114 ( DOI 10.1309 / AJCP88FZTWANLRCB , online olvasás ).
- Kondo és mtsai 2014 .
- (en) Yosuke Yamakawa, Akira Masaoka, Takahiko Hashimoto, Hiroshi Niwa, Tsutomu Mizuno, Yoshitaka Fujii és Kazuya Nakahara, „ A thymoma kísérleti tumor - csomópont - metasztázis osztályozása ” , Cancer , American Cancer Society, vol. 68, n o 9,1991. november, P. 1984-1987 ( ISSN 1097-0142 , online olvasás , konzultáció 2016. április 25-én ).
- (in) Amedeo Vittorio Bedininek Stefano Michele Andreani Luca Tavecchio Alessandra Fabbri Roberto Giardini, Tiziana Camerini, Rosaria Bufalino, Alberto Morabito és Juan Rosai, " Javaslat a Novel rendszer az átmeneti thymus epithelialis tumorokat " , The Annals of Thoracic Surgery , Elsevier BV, vol. 80, n o 6,2005. december, P. 1994-2000 ( ISSN 0003-4975 , DOI 10.1016 / j.athoracsur.2005.07.019 , online olvasás ).
- Detterbeck és mtsai 2014 .
- (in) Richard F. Riedel és William R. Burfeind, Jr., " thymoma: Megjelenés jóindulatú, rosszindulatú potenciál " , The Oncologist , Alphamed Press, vol. 11, n o 8,1 st szeptember 2006, P. 887-894 ( ISSN 1083-7159 , DOI 10.1634 / teonkológus.11-8-887 , olvassa el online ).
- (in) Guiliano Maggi Caterina Casadio Antonio Cavallo Roberto Cianci Massimo Molinatti és Enrico Ruffini, " timoma : 241 műtött eset eredményei " , The Annals of Thoracic Surgery , Elsevier BV, vol. 51, n o 1,1991. január, P. 152-156 ( ISSN 0003-4975 , DOI 10.1016 / 0003-4975 (91) 90478-9 ).
- (in) K. Nakahara K. Ohno J. Hashimoto, H. Maeda, S. Miyoshi, Sakurai M, Kawashima Monden Y és Y, " thymoma: eredmények teljes reszekcióval és adjuváns posztoperatív besugárzással 141 egymást követő betegnél " , The Journal of Thoracic and Cardiovascular Surgery , Elsevier, vol. 95, n o 6,1988. június, P. 1041-1047 ( ISSN 0022-5223 , PMID 3374155 , online olvasás , hozzáférés : 2016. április 25. ).
- (in) Federico Venuta, Erino A Rendina, Edoardo O Pescarmona, Tiziano De Giacomo, Maria Luce vegna, Paola Fazi, Isac Flaishman, Enrico Guarino és Costante Ricci, " A timoma multimodalitásának kezelése: távlati tanulmány " , The Thoracic Annals Sebészet , Elsevier BV, vol. 64, n o 6,1997 december, P. 1585-1592 ( ISSN 0003-4975 , DOI 10.1016 / s0003-4975 (97) 00629-2 , online olvasás ).
- (en) Saina Attaran, David McCormack, John Pilling és Karen Harrison-Phipps: „A timoma mely szakaszai részesülnek adjuváns kemoterápiában a thymectomia utáni időszakban? ” , Interaktív szív- és érrendszeri és mellkasi sebészet , Oxford University Press (OUP), vol. 15, n o 22012. május 2, P. 273-275 ( ISSN 1569-9293 , DOI 10,1093 / icvts / ivs133 , olvasható online ).
- (in) Mr. Hamaji F. Kojima, Mr. Omasa, Sozu T., T. Sato, F. Chen, Mr. Sonobe és H. dátum, " A meta-analízis debulking műtét versus sebészi biopszia rezekálható thymomás ” , European Journal of Cardio-Thoracic Surgery , Oxford University Press (OUP), vol. 47, n o 4,2014. július 11, P. 602-607 ( ISSN 1010-7940 , DOI 10.1093 / ejcts / ezu277 , online olvasás ).
- (en) Jens Rueckert, Marc Swierzy, Harun Badakhshi, Andreas Meisel és Mahmoud Ismail, „ Robotikus asszisztált thymectomia: műtéti eljárás és eredmények ” , The Journal of Thoracic and Cardiovascular Surgery , Thieme, vol. 63, n o 3,2015. április, P. 194-200 ( ISSN 0171-6425 , DOI 10.1055 / s-0035-1549007 , online olvasás , hozzáférés : 2016. április 25. ).
- (in) Alper Toker, " A minimálisan invazív thymoma reszekció szabványosított meghatározása és politikája " , Annals of Cardiothoracic Surgery , AME Publishing Company, vol. 4, n o 6,2015. november, P. 535-539 ( ISSN 2225-319X , PMCID 4.669.255 , DOI 10,3978 / j.issn.2225-319X.2015.10.02 , olvasható online , elérhető április 25, 2016 ).
- (in) Joseph B. Shrager, " Extended Transcervical Thymectomy: The Ultimate Minimally Invasive Approach " , The Annals of Thoracic Surgery , Elsevier BV, vol. 89, n o 6,2010. június, S2128-S2134 ( ISSN 0003-4975 , DOI 10.1016 / j.athoracsur.2010.02.099 , online olvasás ).
- (in) Marcin Zieliński, J Jaros Kuzdzał és Artur Szlubowski, " Transcervicalis-subxiphoid-videothoracoscopic" maximális "thymectomy - Műszaki operatív és korai eredmények " , The Annals of Thoracic Surgery , Elsevier BV, vol. 78, n o 22004. augusztus, P. 404-409 ( ISSN 0003-4975 , DOI 10.1016 / j.athoracsur.2004.02.021 , online olvasás ).
- (-ban) N. Kitagawa, Mr. Shinkai H. Take, K. Mochizuki, F. Asano, H. Usui, H. Miyagi, T. Kido, N. Kurauchi, H. és S. Yamashita Osaka, " Mediastinoscopic extended thymectomia myasthenia gravisos gyermekbetegeknél ” , Journal of Pediatric Surgery , Elsevier Inc., vol. 50, n o 4,2015. április, P. 528-530 ( ISSN 0022-3468 , PMID 25840056 , online olvasás , hozzáférés : 2016. április 25. ).
- Hess és mtsai 2016 .
- Maurizi et al 2015 .
- (en) I. Zahid, S. Sharif, T. Routledge és M. Scarci, „ Videóval támogatott thoracoscopos műtét vagy transzsternális thymectomia a myasthenia gravis kezelésében? ” , Interaktív szív- és érrendszeri és mellkasi sebészet , Oxford University Press (OUP), vol. 12, n o 1,2010. október 13, P. 40–46 ( ISSN 1569-9293 , DOI 10.1510 / icvts.2010.251041 , online olvasás ).
- (in) Pio Maniscalco Nicola Tamburini Francesco Quarantotto William Grossi Elena Garelli és Giorgio Cavallesco, " A korai stádiumú thymoma hosszú távú eredménye: Thoracoscopic és Open Approaches összehasonlítása " , The Thoracic and Cardiovascular Surgeon , Thieme Publishing Group járat. 63, n o 03,2015. január 28, P. 201-205 ( ISSN 0171-6425 , DOI 10.1055 / s-0034-1396594 , online olvasás , hozzáférés : 2016. április 25. ).
- (in) René Horsleben Petersen, " Videó által támogatott torakoszkópos thymectomia 5 mm-es portokkal és szén-dioxid-befúvással " , Annals of Cardiothoracic Surgery , AME Publishing Group repülés. 5, n o 1,2016. január, P. 51–55 ( ISSN 2225-319X , DOI 10.3978 / j.issn.2255-319X.2016.01.02 , online olvasás , konzultáció 2016. április 25-én ).
- (in) Kazuo Nakagawa, Kohei Yokoi, Jun Nakajima Fumihiro Tanaka Yoshimasa Maniwa, Makoto Suzuki, Takeshi Nagayasu és Hisao Asamura, " Megfelelő-e a thymomectomia egyedül az I. stádiumú (T1N0M0) timómához? A hajlam-pontszám elemzés eredményei ” , The Annals of Thoracic Surgery , Elsevier BV, vol. 101, n o 22016. február, P. 520-526 ( ISSN 0003-4975 , DOI 10.1016 / j.athoracsur.2015.07.084 , olvasható online ).
- (in) Faiz Y Bhora, David J Chen, Frank C. Detterbeck Hisao Asamura Conrad Falkson Pier Luigi Filosso Giuseppe Giaccone, James Huang, Jhingook Kim, Kazuya Kondo, Marco Lucchi, Mirella Marino Edith M Marom, Andrew G Nicholson, Meinoshin Okumura , Enrico Ruffini és Paul Van Schil , „ Az ITMIG \ / IASLC tímikus hámtumorok stádiumprojektje: javasolt nyirokcsomótérkép a tímuszos hámdaganatok számára a TNM rosszindulatú daganatok osztályozásának következő kiadásában ” , Journal of Thoracic Oncology , Elsevier BV , vol. 9, n o 9,2014. szeptember, S88-S96 ( ISSN 1556-0864 , DOI 10.1097 / jto.0000000000000293 , online olvasás ).
- (in) Andrea Viti Bertolaccini Luca és Alberto Terzi: " Mi a nyirokcsomó-áttétek és a lymphadenectomia szerepe a tímuszos karcinómák és karcinoidok műtéti kezelésében és prognózisában? ” , Interact CardioVasc Thorac Surg , Oxford University Press (OUP), vol. 19, n o 6,2014. szeptember 4, P. 1054-1058 ( ISSN 1569-9293 , DOI 10.1093 / icvts / ivu281 , online olvasás ).
- (in) Benny Weksler Arjun Pennathur, Jennifer L. Sullivan és Katie S. Nason: "A csomómintavétel reszekciója magában foglalja a thymoma kellékeket " , The Journal of Thoracic and Cardiovascular Surgery , Elsevier BV, vol. 149, n o 3,2015. március, P. 737-742 ( ISSN 0022-5223 , DOI 10.1016 / j.jtcvs.2014.11.054 , online olvasás ).
- Kadota és mtsai 2015 .
- (en) GO Skeie, S. Apostolski, A. Evoli, NE Gilhus, I. Illa, L. Harms, D. Hilton-Jones, A. Melms, J. Verschuuren és HW Horge, „ Útmutató autoimmun neuromuszkuláris transzmissziós rendellenességek kezelésére ” , European Journal of Neurology , Wiley-Blackwell, vol. 17, n o 7,2010. február 23, P. 893-902 ( ISSN 1351-5101 , DOI 10.1111 / j.1468-1331.2010.03019.x , online olvasható ).
- (in) Yoshito Yamada, Shigetoshi Yoshida Takekazu Iwata, Hidemi Suzuki, Tetsuzo Tagawa, Teruaki Mizobuchi Naoki Kawaguchi és Ichiro Yoshino, " kialakulásának kockázati tényezői Postthymectomy myasthenia timómasejteket betegek " , az Annals of mellkassebészet , Elsevier, repülés. 99, n o 3,2015. március, P. 1013-1019 ( ISSN 0003-4975 , DOI 10.1016 / j.athoracsur.2014.10.068 , olvasható online ).
- (en) KH Choi, TS Nam, SH Lee és MK Kim, „A preoperatív tüdőfunkció szorosan összefügg a thymectomia utáni myasthenikus válsággal ” , Neurology India , vol. 62, n o 22014. március-április, P. 164–168 ( online olvasás , konzultáció 2016. április 25-én ).
- (in) Ds fiatalabb és N. Raksadawan, " Medical terápiák myasthenia gravis " , Chest Surgery Clinics of North America , WB Saunders Co., Vol. 11, n o 22001. május, P. 329-336 ( ISSN 1547-4127 , PMID 11413759 , online olvasás , hozzáférés : 2016. április 25. ).
- (in) Peter E. Krucylak és Keith S. Naunheim, " Myasthenia gravisos betegek preoperatív előkészítése és érzéstelenítése " , Szemináriumok a mellkasi és szív- és érrendszeri műtétekben , Elsevier BV, vol. 11, n o 1,1999. január, P. 47–53 ( ISSN 1043-0679 , DOI 10.1016 / s1043-0679 (99) 70019-5 , online olvasás ).
- (en) Shunsuke Endo, Tsutomu Yamaguchi, Noriko Saito, Shinichi Otani, Tsuyoshi Hasegawa, Yukio Sato és Yasunori Sohara, „ Tapasztalat a thymectomia programozott szteroid kezelésével nonthymomatous myasthenia gravis-ban ” , BV Annals of Thoracvieric Surgery köt. 77, n o 5,2004. május, P. 1745-1750 ( ISSN 0003-4975 , DOI 10.1016 / j.athoracsur.2003.10.039 , online olvasás ).
- (in) Edward Arsura, Norman G. Brunner, Tatsuji Namba és David Grob, " Nagy dózisú intravénás metilprednizolon Myasthenia Gravisban " , Archívum neurológiai , American Medical Association (AMA), vol. 42, n o 12,1 st december 1985, P. 1149-1153 ( ISSN 0003-9942 , DOI 10,1001 / archneur.1985.04060110031011 , olvasható online ).
- Wei 2013 .
- (in) RJ Kelly, I. Petrini A. Rajan, Y. Wang és G. Giaccone, " Thymás rosszindulatú daganatok : a klinikai irányítástól a célzott terápiákig " , Journal of Clinical Oncology , American Society of Clinical Oncology (ASCO), lopás. 29, n o 36,2011. november 21, P. 4820-4827 ( ISSN 0732-183X , DOI 10.1200 / jco.2011.36.0487 , online olvasás )
- „ Thymic Tumors and Cancer Network ” (hozzáférés : 2016. április 25. ) .
- (en) Masatsugu Hamaji, Syed Osman Ali és Bryan M. Burt, „ A meta-analízis Sebészeti Versus nonsurgical kezelése Ismétlődő thymoma ” , The Annals of Thoracic Surgery , Elsevier, vol. 98, n o 22014. augusztus, P. 748-755 ( ISSN 0003-4975 , DOI 10.1016 / j.athoracsur.2014.04.028 , online olvasás ).
- (en) Masayuki Haniuda, Ryoichi Kondo, Hiroki Numanami, Akiko Makiuchi, Emi Machida és Jun Amano, „ Thymoma visszatérése: klinikopatológiai jellemzők, újbóli működés és kimenetel ” , Journal of Surgical Oncology , Wiley-Blackwell , vol. 78, n o 3,2001, P. 183-188 ( ISSN 0022-4790 , DOI 10.1002 / jso.1146 , online olvasás ).
- (in) Alberto Sandri Giacomo Cusumano, Filippo Lococo Marco Alifano Pierluigi Granone Stefano Margaritora Alfredo Cesario, Alberto Oliaro Pierluigi Filosso, Jean-François Regnard és Enrico Ruffini, " A visszatérő thymoma hosszú távú eredményeinek utókezelése: multicentrikus elemzés " , Journal of Thoracic Oncology , Elsevier BV, vol. 9, n o 12,2014. december, P. 1796-1804 ( ISSN 1556-0864 , DOI 10.1097 / jto.0000000000000370 , online olvasás ).
- (in) Mark Shapiro és Robert J. Korst , " sebészi megközelítés a timusz epiteliális tumorok IVA Gyakorlat " , Frontiers in Oncology , Vol. 3,2014( ISSN 2234-943X , PMID 24459636 , PMCID PMC3891210 , DOI 10.3389 / fonc.2013.00332 , online olvasás , hozzáférés : 2017. július 9 )
- (in) Motoki Yano Hidefumi Sasaki Satoru Moriyama, Yu Hikosaka Keisuke Yokota Akira Masaoka és Yoshitaka Fujii , " A visszatérő elváltozások száma prognosztikai tényező a visszatérő thymomában " , Interact Cardiovasc Thorac Surg , Oxford University Press (OUP), vol. 13, n o 1,1 st június 2011, P. 21–24 ( ISSN 1569-9293 , DOI 10.1510 / icvts.2010.264036 , online olvasás ).
- " Ha a thymus rák terjed " , a Canadian Cancer Society-től (hozzáférés : 2016. április 26. ) .
- (in) Paul M. Claiborne, Clara S. Fowler és Ara A. Vaporciyan, " A mellkas rosszindulatú daganatos megbetegedéseinek nyomon követése " , Thoracic Surgery Clinics , Elsevier BV, vol. 22, n o 1,2012. február, P. 123-131 ( ISSN 1547-4127 , DOI 10.1016 / j.thorsurg.2011.08.011 , olvasható online ).
- (en) Jean-François Regnard, Pierre Magdeleinat Christian Dromer Elizabeth Dulmet, Vincent Montpreville, Jean-François Levi és Philippe Levasseur: " Prognosztikai tényezők és hosszú távú eredmények thymoma utáni reszekció: 307 beteg sorozata " , The Journal of Mellkasi és szív- és érrendszeri sebészet , Elsevier BV, vol. 112, n o 21996 augusztus, P. 376-384 ( ISSN 0022-5223 , PMID 8751506 , DOI 10.1016 / S0022-5223 (96) 70265-9 , online olvasás , hozzáférés : 2016. április 25 ).
Fő felhasznált tudományos cikkek
Általános cikkek-
(in) Frank C Detterbeck és Alden M Parsons, " Thymus tumorok " ["thymus tumorok"], The Annals of Thoracic Surgery , Elsevier BV, vol. 77, n o 5,2004. május, P. 1860-1869 ( ISSN 0003-4975 , DOI 10.1016 / j.athoracsur.2003.10.001 , online olvasás ).

-
(in) R. Srirajaskanthan, C. Toubanakis, Mr. Caplin Dusmet és ME, " A thymus tumorok áttekintése " ["A thymás tumorok áttekintése"], Lung Cancer , Elsevier BV, vol. 60, n o 1,2008. április, P. 4-13 ( ISSN 0169-5002 , DOI 10.1016 / j.lungcan.2008.01.014 , online olvasás ).

-
(in) Cameron D. Wright, " A thymomák kezelése " ["Support thymoma"], Critical Reviews in Oncology / Hematology , Elsevier BV, vol. 65, n o 22008. február, P. 109-120 ( ISSN 1040-8428 , DOI 10.1016 / j.critrevonc.2007.04.005 , online olvasás ).

-
(en) Frank C. Detterbeck, Kelly Stratton, Dorothy Giroux, Hisao Asamura, John Crowley, Conrad Falkson, Pier Luigi Filosso, Aletta A. Frazier, Giuseppe Giaccone, James Huang, Jhingook Kim, Kazuya Kondo, Marco Lucchi, Mirella Marino, Edith M. Marom, Andrew G. Nicholson, Meinoshin Okumura, Enrico Ruffini és Paul Van Schil , „ Az IASLC / ITMIG Thymic Epithelial Tumors Staging Project: Javaslat bizonyítékokon alapuló szakaszos osztályozási rendszerre a TNM jövőbeli (8.) kiadásához A rosszindulatú daganatok osztályozása ” [[IASLC / ITMIG Thymic Epithelial Tumor Staging Project: javaslat evidence-based Staging Classification for the Aston TNM Classification of Malignus Tumors”], Journal of Thoracic Oncology , Elsevier BV, járat. 9, n o 9,2014. szeptember, S65-S72 ( ISSN 1556-0864 , DOI 10.1097 / jto.0000000000000290 , online olvasás ).

-
(en) Kenji Koga, Yoshihiro Matsuno, Masayuki Noguchi, Kiyoshi Mukai, Hisao Asamura, Tomoyuki Goya és Yukio Shimosato, „ A 79 thymoma áttekintése: A stádiumrendszer módosítása és a konvencionális invazív és non-invazív timómára történő felosztás átértékelése ” [“ 79 thymoma áttekintése: a stádiumrendszer módosítása és a hagyományos szétválasztás invazív és non-invazív thymomákká történő újbóli értékelése. »], Pathology International , Wiley-Blackwell, vol. 44, n o 5,2008. december 12, P. 359-367 ( ISSN 1320-5463 , DOI 10.1111 / j.1440-1827.1994.tb02936.x , online olvasható ).

-
(en) Kazuya Kondo, Paul Van Schil, Frank C. Detterbeck, Meinoshin Okumura, Kelly Stratton, Dorothy Giroux, Hisao Asamura, John Crowley, Conrad Falkson, Pier Luigi Filosso, Giuseppe Giaccone, James Huang, Jhingook Kim, Marco Lucchi, Mirella Marino, Edith M Marom, Andrew G. Nicholson és Enrico Ruffini, „ Az IASLC / ITMIG Thymic Epithelial Tumors Staging Project: Javaslatok az N és M komponensekre a TNM rosszindulatú daganatok osztályozásának következő (8.) kiadásához ” [„Projet of IASLC / ITMIG Thymic Epithelial Tumor Staging: Javaslatok az N és M komponensekre a TNM rosszindulatú daganatok osztályozásának nyolcadik kiadásához ”], Journal of Thoracic Oncology , Elsevier BV, vol. 9, n o 9,2014. szeptember, S81- S87 ( ISSN 1556-0864 , DOI 10.1097 / jto.0000000000000291 , online olvasás ).

-
(en) Edith M. Marom, „ Imaging Thymoma ” , Journal of Thoracic Oncology , Elsevier BV, vol. 5, n o 10,2010. október, S296-S303 ( ISSN 1556-0864 , DOI 10.1097 / jto.0b013e3181f209ca , olvassa el online ).

-
(en) Alexander Marx, Philipp Ströbel, Sunil S. Badve, Lara Chalabreysse, John KC Chan, Gang Chen, Laurence de Leval, Frank Detterbeck, Nicolas Girard, Jim Huang, Michael O. Kurrer, Libero Lauriola, Mirella Marino, Yoshihiro Matsuno , Thierry Jo Molina, Kiyoshi Mukai, Andrew G. Nicholson, Daisuke Nonaka, Ralf Rieker, Juan Rosai, Enrico Ruffini és William D. Travis, „ ITMIG Consensus Statement on the Use of the WHO Histological Classification of Thymoma and Thymic Carcinoma: Refined Definitions , szövettani kritériumok és " [" ITMIG konszenzusos nyilatkozata a WHO thymoma és thymic carcinoma osztályozásának használatáról: definíciók, szövettani kritériumok és felülvizsgált deklaráció "], Journal of Thoracic Oncology , Elsevier BV, vol. 9, n o 5,2014. május, P. 596-611 ( ISSN 1556-0864 , DOI 10.1097 / jto.0000000000000154 , online olvasás ).

-
(en) Yoshitaka Fujii , „ A thymoma kezelésének közzétett irányelvei ” , mellkasi sebészeti klinikák , Elsevier BV, vol. 21, n o 1,2011. február, P. 125–129 ( ISSN 1547-4127 , DOI 10.1016 / j.thorsurg.2010.08.002 , online olvasás ).

- " RITMIKUS hálózati adattár - tímusz hámdaganatok " , a tímuszos daganatok és a rákhálózatról ,2020(megtekintés : 2020. április 15. ) .
-
(en) Nicholas R. Hess, Inderpal S. Sarkaria, Arjun Pennathur, Ryan M. Levy, Neil A. Christie, James D. Luketich: „ Minimálisan invazív versus nyílt thymectomia: a műtéti technikák, a betegek demográfiájának és a perioperatív szisztematikus áttekintése eredmények ” [„ Minimálisan invazív vagy nyílt thymectomia: a műtéti technikák, a betegek demográfiai és perioperatív eredményeinek szisztematikus áttekintése ”], Annals of Cardiothoracic Surgery , vol. 5, n o 1,2016. január, P. 1–9 ( DOI 10.3978 / j.issn.2255-319X.2016.01.01 , online olvasás ).

-
(en) Yoshihisa Kadota, Hirotoshi Horio, Takeshi Mori, Noriyoshi Sawabata, Taichiro Goto, Shinichi Yamashita, Takeshi Nagayasu és Akinori Iwasaki: „ Perioperative management in myasthenia gravis: a japán társulási rendszer szisztematikus felülvizsgálatának és javaslatának újbóli közzététele mellkasi sebészethez ” ], Általános mellkasi és szív- és érrendszeri sebészet , Springer, vol. 63, n o 4,2015. április, P. 201–215 ( DOI 10.1007 / s11748-015-0518-y , online olvasás ).

-
en) Giulio Maurizi, Antonio D'Andrilli, Lorenzo Sommella, Federico Venuta és Erino A. Rendina, „ Transsternal Thymectomy ” , The Journal of Thoracic and Cardiovascular Surgery , Thieme, vol. 63, n o 3,2015. április, P. 178–186 ( DOI 10.1055 / s-0034-1396083 , online olvasás ) .

-
(in) Mao Ling Wei Kang Deying, Lijia Gu Meng Qiu Liao Zhengyin és Yanming Mu " Kemoterápia előrehaladott tímiás karcinóma és timóma felnőtteknél " ["Kemoterápiás tímiás karcinómák és lokálisan előrehaladott tímózis felnőtteknél"], Cochrane szisztematikus áttekintések adatbázisa , Wiley -Blackwell,2013. augusztus 23( DOI 10.1002 / 14651858.cd008588.pub2 , olvassa el online ).

Külső linkek
- „ Thymic Tumors and Cancer Network (RYTHMIC) ” (hozzáférés : 2016. április 26. ) .
- „ Thymoma ” , az Orphaneten , frissítve: 2011. március (megtekintés : 2016. április 26. ) .
- „ Mi a thymus rák? " On Canadian Cancer Society (hozzáférés: 2016. április 26. ) .
- " A thymus és a thymomák epitheliális daganatai " , a betegtájékoztató lap, az Institute Institute Monisteouris- on , frissítve:1 st április 2016(megtekintve 2016. április 26-án ) .
- " Thymectomia " , a Myasthéniques Isolés et Solidaires egyesületről ,2013. július 6(megtekintve 2016. május 30-án ) .
- Hatósági nyilvántartások :