Fehérje aggregáció
A fehérjék aggregációja (vagy aggregációs / agglomerációs fehérje ) egy olyan biológiai jelenség, amelyben a fehérjék gyengén hajtogatott aggregátumai (vagyis felhalmozódnak és csoportosulnak), tehát intra-, mint sejten kívül. Ezek a fehérje aggregátumok gyakran összefüggnek a betegséggel . Valójában a fehérje-aggregátumok sokféle betegségben szerepet játszanak, amelyeket amiloidózisnak neveznek , beleértve az ALS-t , az Alzheimer- és a Parkinson- kórokat és a prionbetegségeket .
Szintézisük után a fehérjéknek szokásuk egy adott háromdimenziós konformációba hajtódni, amely termodinamikailag a számukra a legkedvezőbb: natív állapotuk . Ezt a hajtogatási folyamatot a hidrofób hatás vezérli , amely a fehérje hidrofób részeinek azon tendenciája, hogy megpróbálják megvédeni magukat a sejt hidrofil környezetétől a fehérje belsejében történő lyukasztással. Tehát a fehérje külseje tipikusan hidrofil, míg a belseje tipikusan hidrofób.
A fehérjeszerkezeteket nem kovalens kötések és két ciszteinmaradékot összekötő diszulfidkötések stabilizálják . A nem kovalens kölcsönhatások közé tartoznak az ionos kötések és a gyenge van der Waals kölcsönhatások . Az ionos kölcsönhatások az anion és a kation között alakulnak ki, és sóhidakat képeznek, amelyek segítenek a fehérje stabilizálásában. A Van der Waals kölcsönhatások közé tartoznak a nempoláris kölcsönhatások ( londoni erők ) és a poláris kölcsönhatások ( hidrogénkötések , intermolekuláris erők ). Ezek fontos szerepet játszanak a fehérjék szekunder struktúrájában , például alfa-spirál vagy béta lap kialakításában , valamint harmadlagos szerkezetükben . A kölcsönhatások közötti aminosav -maradék egy adott fehérje nagyon fontos a végső szerkezetét, hogy fehérje.
Ha a nem kovalens interakciókban változások vannak, amik az aminosav-szekvencia változásából következhetnek be, akkor valószínűleg a fehérje rosszul vagy egyáltalán nem hajtogat. Ebben a típusú helyzetben, ha a sejt nem segít a fehérjéknek ezt a hajtogatási hibát kijavítani vagy elpusztítani, össze tudnak tömörülni, és ebben a folyamatban a fehérjék kitett hidrofób részei kölcsönhatásba léphetnek a kitett hidrofób részekkel. fehérjék. A fehérje-aggregátumok három fő típusa képződhet: amorf aggregátumok, oligomerek és amiloid fibrillák .
Okoz
A fehérjék összesítése több okból is megvalósulhat. Négy osztályba sorolhatók ezek az okok, amelyeket az alábbiakban részletezünk.
Mutációk
A mutációk előforduló szekvenciában a DNS lehet vagy nem befolyásolja az aminosavszekvenciát a fehérje. Ha a szekvencia érintett, egy másik aminosav megváltoztathatja az oldalláncok közötti kölcsönhatásokat , ami befolyásolja a fehérje hajtogatását. Ez a fehérje hidrofób régióinak kitettségéhez vezethet, amelyek ugyanazzal a rosszul összehajtott vagy kibontott fehérjével, vagy egy másik fehérjével aggregálódnak.
A magukat a fehérjéket érintő mutációk mellett a fehérje-aggregációt közvetett módon a fehérjékben olyan szabályozási utak során előforduló mutációk is kiválthatják, mint például a hajtogatási útvonal ( chaperonok ) vagy az ubiquitin-proteasoma útvonal ( ubiquitin-ligázok ). A kaperonok elősegítik a fehérjék felhajtását, biztonságos környezetet biztosítva számukra. Az ubiquitin ligázok megcélozzák a fehérjéket, amelyeket az ubiquitin módosításával kell lebontani .
Hibák a fehérjeszintézis során
A fehérje aggregációt a transzkripció vagy a transzláció során felmerülő problémák okozhatják . A transzkripció során a DNS-t átmásolják az mRNS-be , egy pre-mRNS- szálat képezve, amely poszt-transzkripciós módosításokon megy keresztül, hogy mRNS - t képezzen. A transzláció során a riboszómák és az RNS-ek segítenek az mRNS-szekvencia aminosav-szekvenciává történő átalakításában. Ha a két lépés bármelyikében hibák lépnek fel, amelyek helytelen mRNS-szálat vagy aminosav-szekvenciát eredményeznek, ez a fehérje hibás hajtogatásához vezet, ami fehérje-aggregációhoz vezet.
Környezeti stressz
A környezeti stresszek, mint például a szélsőséges hőmérséklet vagy pH , vagy az oxidatív stressz , szintén fehérje aggregációhoz vezethetnek. Az ilyen típusú stressz által okozott betegségre példa a krioglobulinémia .
A szélsőséges hőmérsékletek gyengíthetik és destabilizálhatják az aminosavmaradékok közötti nem kovalens kötéseket. Az adott fehérje pH-tartományán kívül eső PH-k megváltoztathatják az aminosavak protonációs állapotát , ami növelheti vagy csökkentheti a nem kovalens kölcsönhatásokat. A fehérje kevésbé stabil kötődéséhez és ezért nem hajtogatásához is vezethet.
Az oxidatív stresszt olyan gyökök okozhatják, mint az ROS . Ezek az instabil gyökök megtámadhatják az aminosavakat, ami oldalláncok (például aromás oldalláncok vagy metionin oldalláncok ) oxidációjához és / vagy a polipeptidkötések hasításához vezet. Ez befolyásolhatja azokat a nem kovalens kötéseket, amelyek a fehérjét megfelelő formában tartják, ami a fehérje destabilizálódását okozhatja, és ezáltal megakadályozhatja a fehérje összecsukódását.
Öregedés
A sejtek olyan mechanizmusokkal rendelkeznek, amelyek képesek újratekerni vagy lebontani a fehérje aggregátumokat. A sejtek öregedésével azonban ezek a kontrollmechanizmusok kevésbé hatékonyak, és a sejt kevésbé képes átvenni ezeket az aggregátumokat.
Az a hipotézis, miszerint a fehérje aggregáció az öregedés következményes folyamata, most tesztelhető, mert a késleltetett öregedés bizonyos modelljei kidolgozás alatt állnak. Ha a fehérje-aggregátumok fejlődése az öregedéstől független folyamat lenne, akkor ennek az öregedésnek a lassítása nem lenne hatással a proteotoxicitás időbeli változására. Ha azonban az öregedés a proteotoxicitás elleni védőmechanizmusok aktivitásának csökkenésével járna, a lassított öregedés modelljei mutatnák az aggregáció és a proteotoxicitás csökkenését. Annak érdekében, hogy megoldja ezt a problémát, több toxicitási vizsgálatokat végeztünk a fonalféreg C. elegans . Ezek a vizsgálatok kimutatták, hogy az inzulin / IGF jelátviteli aktivitás csökkentése, amely egy jól ismert öregedési szabályozási út, véd a neurodegenerációval járó toxikus fehérje-aggregáció ellen. Ennek a megközelítésnek az érvényességét kipróbálták és megerősítették emlősökben , mivel csökkentette az IGF-1 jelátviteli út védett , Alzheimer-kórban szenvedő vizsgálati egerek aktivitását a betegséggel kapcsolatos viselkedés és károsodások megjelenése miatt.
Az aggregátumok helye
Számos tanulmány kimutatta, hogy a fehérje aggregációra adott sejtes válaszok jól szabályozottak és szervezettek. A fehérje aggregátumok a sejt meghatározott területein helyezkednek el, és a kutatások ezekre a területekre összpontosítottak prokariótákban ( E. coli ) és eukariótákban ( élesztő , emlős sejtek).
Baktériumokban
A baktériumok aggregátumai aszimmetrikusan találhatók a sejt egyik pólusánál , az " idősebb pólusnál ". A sejtosztódást követően a több elülső pólust tartalmazó leánysejt megszerzi a fehérje aggregátumot, és lassabban növekszik, mint a leánysejt az aggregátum nélkül. Ez a természetes szelekció mechanizmusát képezi a baktériumok populációjában a fehérje aggregátumok csökkentésére.
Élesztőkben
Az élesztősejtek legtöbb fehérje aggregátumának hajtogatási hibáját chaperonok javítják. Egyes aggregátumok hajtáshibája azonban nem korrigálható, például az oxidatív stressz által károsított fehérjék vagy a lebontásra szánt fehérjék. Ehelyett átirányítható egy két rekesz: a JUxtaNuclear minőség-ellenőrző rekesz ( JUNQ ), közel a nukleáris membrán, és az oldhatatlan fehérje Betét vagy IPOD angolul), közel a vacuole az élesztő sejtekben. A fehérje aggregátumok akkor kerülnek a JUNQ-ba, amikor azokat mindenütt felszámolják és lebontásra szánják, míg az összetapadt és oldhatatlan fehérjék hosszabb tárolás céljából az IPOD-ba kerülnek. Az eredmények azt mutatták, hogy az ezen a helyen található fehérjék autofágia útján eltávolíthatók . Ez a két lehetőség úgy működik együtt, hogy a fehérjék hajlamosak az IPOD felé menni, amikor a proteaszóma út túlterhelt.
Emlős sejtekben
Az emlőssejtekben ezeket a fehérje-aggregátumokat "agresomáknak" nevezik, és akkor képződnek, amikor a sejt beteg. Ez azért történik, mert az aggregátumok általában akkor képződnek, amikor heterológ fehérjék vannak jelen a sejtben, ami akkor fordulhat elő, amikor a sejt mutálódik. Az ubiquitin ligáz E3 képes felismerni a rosszul összehajtott fehérjéket és ubiquitinizálni őket. HDAC6 azután kötődnek ubiquitin és a motor fehérje dyneinproteineket szállítani a „címkézett” aggregátumok a centrosoma . Odaérve összeállnak egy olyan szférában, amely körülveszi a centroszómát. Chaperonákat és proteázómákat biztosítanak, és aktiválják az autofágia működését.
Az adalékanyagok eltávolítása
A sejtekben két fő "minőség-ellenőrzési" rendszer működik, amelyek felelősek a fehérje-aggregátumok eltávolításáért. A rosszul összehajtott fehérjéket a bi-chaperone-rendszer, az ubiquitin-proteasome rendszer vagy az autofágia képes lebontani.
Neo-hajtogatás
A bi-chaperone rendszer a Hsp70 (DnaK-DnaJ-GrpE E. coliban és Ssa1-Ydj1 / Sis1-Sse1 / Fe1 élesztõben) és a Hsp100 ( E. coli ClpB és élesztõben Hsp104) chaperonákat használja fel és neo hajtogatja a fehérjéket.
A Hsp70 kölcsönhatásba lép a fehérje aggregátumokkal és toborozza a Hsp100-at. A Hsp70 stabilizálja az aktivált Hsp100-at. Hsp100 van aromás pórus hurkok használt menetvágó aktivitás kibogozni egyetlen polipeptidek. Ez a szálképző tevékenység megindítható az N-terminálison , a C-terminálon vagy a polipeptid közepén . A polipeptid a Hsp100 által transzlokáción megy keresztül egy sor lépésben, amelyek mindegyike ATP-t fogyaszt . A polipeptid önmagában vagy hősokkfehérjék ( hősokkfehérjék ) segítségével nem hajtódik össze, majd neo-hajtogatható .
Lebomlás
A rosszul összehajtott fehérjéket az ubiquitin-proteaszóma rendszer távolíthatja el. Ez egy E1-E2-E3 útvonalból áll, amely ubikvitinizálja a fehérjéket, hogy lebontásra szánja őket. Az eukariótákban a fehérjéket a 26S proteaszóma lebontja. Emlős sejtekben az E3 ligáz és a Hsp70-interakcióban lévő karboxi-terminális fehérje a Hsp70-hez kötött fehérjéket célozza meg. Élesztőben az E3 Doa10 és Hrd1 ligázok hasonló funkciókkal rendelkeznek az endoplazmatikus retikulum fehérjéin :

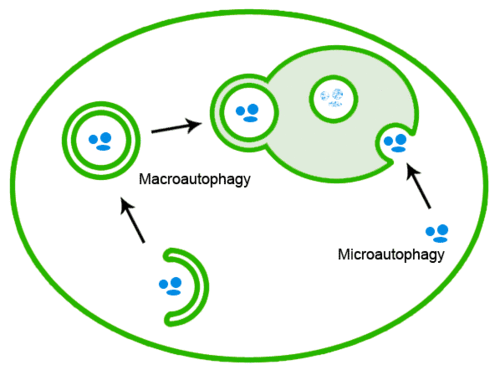
A rosszul összehajtott fehérjéket autofágia is eltávolíthatja, amelynek során a fehérje aggregátumok a lizoszómába kerülnek :
Toxicitás
Bár úgy gondolták, hogy az érett fehérje aggregátumok önmagában mérgezőek, a legfrissebb eredmények szerint valójában az éretlen fehérje aggregátumok a legmérgezőbbek. Ezen aggregátumok hidrofób csoportjai kölcsönhatásba léphetnek és károsíthatják a sejt más komponenseit. A hipotézisek szerint a fehérje-aggregátumok toxicitása összefügg a sejtkomponensek megkötésének mechanizmusaival, az ROS keletkezésével, a membrán specifikus receptoraihoz való kötődéssel vagy a membránok megszakadásával. Egy genetikai teszt megállapította, hogy a nagyobb molekulatömegű fajok felelősek a membrán permeabilitásáért. Ismeretes, hogy a fehérje aggregátumok in vitro destabilizálhatják a mesterséges lipid kettős rétegeket, ami membrán permeabilizációhoz vezet.
Lásd is
Megjegyzések
- (fr) Ez a cikk részben vagy egészben az angol Wikipedia " Fehérje-aggregáció " című cikkéből származik ( lásd a szerzők felsorolását ) .
Hivatkozások
- Adriano Aguzzi és Tracy O'Connor , „ Fehérje-aggregációs betegségek: patogenitás és terápiás perspektívák ”, Nature Review. Drug Discovery , vol. 9, n o 3,2010. március, P. 237-248 ( ISSN 1474-1784 , PMID 20.190.788 , DOI 10.1038 / nrd3050 , olvasható online , elérhető október 30, 2017 )
- Fernanda G. De Felice , Marcelo NN Vieira , M. Nazareth L. Meirelles és Ludmilla A. Morozova-Roche , „ Amyloid aggregátumok képződése humán lizozimból és betegséggel összefüggő variánsaiból hidrosztatikus nyomás segítségével ”, FASEB folyóirat: hivatalos kiadvány az Amerikai Kísérletbiológiai Társaságok Szövetsége , vol. 18, n o 10,2004. július, P. 1099-1101 ( ISSN 1530-6860 , PMID 15.155.566 , DOI 10,1096 / fj.03-1072fje , olvasható online , elérhető október 30, 2017 )
- Rudolph E. Tanzi és Lars Bertram , „ Az Alzheimer-kór amiloid hipotézisének húsz éve: genetikai perspektíva ”, Cell , vol. 120, n o 4,2005. február 25, P. 545–555 ( ISSN 0092-8674 , PMID 15734686 , DOI 10.1016 / j.cell.2005.02.008 , online olvasás , hozzáférés : 2017. október 30. )
- MJ Gething és J. Sambrook , „A fehérje összecsukódik a cellában ”, Nature , vol. 355, n o 63551992. január 02, P. 33-45 ( ISSN 0028-0836 , PMID 1731198 , DOI 10.1038 / 355033a0 , olvasható online , elérhető október 30, 2017 )
- (in) David L. Cox és Michael Nelson , Lehninger Principles of Biochemistry , New York, WH Freeman,2013( ISBN 978-1-4292-3414-6 ) , p. 143
- Sarah J Shoesmith Berke és Henry L Paulson , „A fehérje aggregációja és az ubiquitin proteaszóma útja: az UPPer kezének megszerzése a neurodegenerációban ”, Current Opinion in Genetics & Development , vol. 13, n o 3,1 st június 2003, P. 253–261 ( DOI 10.1016 / S0959-437X (03) 00053-4 , online olvasás , hozzáférés : 2017. október 30 )
- (in) Robert F. Weaver, Molecular Biology , New York, McGraw-Hill,2012( ISBN 978-0-07-352532-7 ) , p. 122-156; 523-600
- Jens Tyedmers , Axel Mogk és Bernd Bukau , „ Cellular stratégiák ellenőrző fehérje aggregáció ”, Nature Reviews. Molecular Cell Biology , vol. 11, n o 11,2010. november, P. 777–788 ( ISSN 1471-0080 , PMID 20944667 , DOI 10.1038 / nrm2993 , online olvasás , hozzáférés : 2017. október 30. )
- (in) ER Stadtman és RL Levine , " A szabad aminosavak és aminosavmaradékok szabad gyökök által közvetített oxidációja a fehérjékben " , Aminosavak , vol. 25 nincsenek csontok 3-4,1 st december 2003, P. 207–218 ( ISSN 0939-4451 és 1438-2199 , DOI 10.1007 / s00726-003-0011-2 , online olvasás , hozzáférés : 2017. október 30. )
- James F. Morley , Heather R. Brignull , Jill J. Weyers és Richard I. Morimoto , „ A poliglutamin-expanziós fehérje-aggregáció és a sejtek toxicitásának küszöbértéke dinamikus, és az öregedés befolyásolja a Caenorhabditis elegans-ban ”, Proceedings of the National Academy of Sciences of the United States of America , vol. 99, n o 16,2002. augusztus 6, P. 10417–10422 ( ISSN 0027-8424 , PMID 12122205 , DOI 10.1073 / pnas.152161099 , online olvasás , hozzáférés : 2017. október 30. )
- Natalia G. Bednarska , Joost Schymkowitz , Frederic Rousseau és Johan Van Eldere , „ Protein aggregation in baktériumok: a vékony határ a funkcionalitás és a toxicitás között ”, Microbiology (Reading, England) , vol. 159, n o Pt 9,2013 szeptember, P. 1795–1806 ( ISSN 1465-2080 , PMID 23894132 , DOI 10.1099 / mic.0.069575-0 , online olvasás , hozzáférés : 2017. október 30. )
- Mari Takalo , Antero Salminen , Hilkka Soinien és Mikko Hiltunen , „ Protein aggregáció és lebomlási mechanizmusai a neurodegeneratív betegségek ”, American Journal of neurodegeneratív betegség , vol. 2, n o 1,2013, P. 1–14 ( ISSN 2165-591X , PMID 23516262 , PMCID PMC3601466 , online olvasás , hozzáférés : 2017. október 30. )
- (in) Rafael Garcia-Mata , Ya-Sheng Gao és Elizabeth Sztul , " Hassles with With Gathering the Garbage: Aggravating Aggresomes " , Traffic , vol. 3, n o 6,1 st június 2002, P. 388-396 ( ISSN 1600-0854 , DOI 10,1034 / j.1600-0854.2002.30602.x , olvasható online , elérhető október 30, 2017 )
- (in) Niels Gregersen, Lars Bolund és Peter Bross , "A fehérje hibás hajtogatása , aggregációja és a betegség romlása " , Molecular Biotechnology , vol. 31, n o 21 st október 2005, P. 141–150 ( ISSN 1073-6085 és 1559-0305 , DOI 10.1385 / MB: 31: 2: 141 , online olvasás , hozzáférés: 2017. október 30. )
- Axel Mogk , Eva Kummer és Bernd Bukau , „ A Hsp70 és Hsp100 chaperone gépek együttműködése a fehérje szétbontásában ”, Frontiers in Molecular Biosciences , vol. 2,2015, P. 22 ( ISSN 2296-889X , PMID 26042222 , PMCID PMC4436881 , DOI 10.3389 / fmolb.2015.00022 , online olvasás , hozzáférés : 2017. október 30. )
- Krzysztof Liberek , Agnieszka Lewandowska és Szymon Zietkiewicz , „ Chaperones in control of protein disaggregation ”, The EMBO journal , vol. 27, n o 22008. január 23, P. 328–335 ( ISSN 1460-2075 , PMID 18216875 , PMCID PMC2234349 , DOI 10.1038 / sj.emboj.7601970 , online olvasás , hozzáférés : 2017. október 30. )
- Bryan Chen , Marco Retzlaff , Thomas Roos és Judith Frydman , „ A fehérje minőségének ellenőrzésének celluláris stratégiái ”, Cold Spring Harbour Perspectives in Biology , vol. 3, N o 8,1 st augusztus 2011, a004374 ( ISSN 1943-0264 , PMID 21746797 , PMCID PMC3140689 , DOI 10.1101 / cshperspect.a004374 , online olvasás , hozzáférés : 2017. október 30. )
- YJ Zhu , H. Lin és R. Lal : „A friss és nemfibrilláris amiloid béta fehérje (1–40) gyors sejtdegenerációt indukál idős humán fibroblasztokban: bizonyíték az AbetaP-csatorna által közvetített celluláris toxicitásra ”, FASEB folyóirat: hivatalos kiadvány az Amerikai Kísérletbiológiai Társaságok Szövetsége , vol. 14, n o 9,2000. június, P. 1244–1254 ( ISSN 0892-6638 , PMID 10834946 , online olvasás , hozzáférés : 2017. október 30. )
- C. Nilsberth , A. Westlind-Danielsson , CB Eckman és Mr. Condron : " Az Arctic APP mutáció (E693G) fokozott Abeta protofibril képződéssel okozza az Alzheimer-kórt " Nature Neuroscience , vol. 4, n o 9,2001. szeptember, P. 887–893 ( ISSN 1097-6256 , PMID 11528419 , DOI 10.1038 / nn0901-887 , online olvasás , hozzáférés : 2017. október 30. )
- (a) Claudio Soto , " kihajtása a szerepe a protein misfoldingot a neurodegeneratív betegségek " , Nature Reviews Neuroscience , Vol. 4, n o 1,2003. január, P. 49-60 ( ISSN 1471-003X , DOI 10.1038 / nrn1007 , olvasható online , elérhető október 30, 2017 )
- Patrick Flagmeier , Suman De , David C. Wirthensohn és Steven F. Lee , „ A protein aggregátumok által indukált lipid vezikulákba történő Ca (2+) beáramlás ultraibens érzékeny mérése ”, Angewandte Chemie (International Ed. In English) , vol. 56, n o 27,2017. június 26, P. 7750–7754 ( ISSN 1521-3773 , PMID 28474754 , PMCID PMC5615231 , DOI 10.1002 / anie.201700966 , online olvasás , hozzáférés : 2017. október 30. )
Külső linkek
- (hu) Folding @ Home segítség a fehérje hajtogatásának dekódolásában.
- (hu) Rosetta @ Home Segít a fehérje szerkezetek és komplexek előrejelzésében.