Jód-metán
| Jód-metán | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 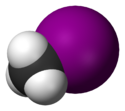 A jodometán szerkezete |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Azonosítás | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| IUPAC név | metil-jodid | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Szinonimák |
Metil-monojód-metán |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100000745 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o EC | 200-819-5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mosolyok |
CI , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1 / CH3I / c1-2 / h1H3 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Megjelenés | jellegzetes szagú színtelen folyadék. fény és nedvesség hatására megbarnul. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kémiai tulajdonságok | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brute formula |
C H 3 I [izomerek] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Moláris tömeg | 141,939 ± 0,001 g / mol C 8,46%, H 2,13%, I 89,41%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dipoláris pillanat | 1,59 D | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fizikai tulajdonságok | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fúzió | -66,5 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° forráspontú | 42,5 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oldékonyság | vízben 20 ° C-on : 14 g · l -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oldhatósági paraméter δ | 9,9 cal 1/2 · cm -3/2 ( 25 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Térfogat | 2,3 g · cm -3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Öngyulladási hőmérséklet | Olvadáspont: 352 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Robbanási határok a levegőben | 8,5 - 66% | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Telített gőznyomás | át 20 ° C-on : 50 kPa , 24.09 psi át 55 ° C-on |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritikus pont | 65,9 bar , 254,85 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termokémia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C o |
egyenlet:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronikus tulajdonságok | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 re ionizációs energia | 9.538 eV (gáz) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Optikai tulajdonságok | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Törésmutató | 1,5304 ( 20 ° C , D) 1,5293 ( 21 ° C , D) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Óvintézkedések | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Veszély H301, H312, H315, H331, H335, H351, H301 : Lenyelve mérgező H312 : Bőrrel érintkezve H315 : Izgatja a bőrt H331 : Belélegezve mérgező H335 : irritálhatja a légzőrendszert H351 : Feltehetően rákot okoz (meg kell jelölni az expozíciós útvonalat, ha azt hivatalosan bizonyított, hogy más expozíciós útvonal azonos veszélyhez vezet) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Besorolatlan termékEnnek a terméknek az osztályozását még nem hitelesítette a Toxicological Directory Service 0.1% -os közzététele az összetevők közzétételi listája szerint |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Szállítás | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
2644 : METIL-JODID |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| IARC osztályozás | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3. csoport : Emberre nézve rákkeltő hatása nem osztályozható | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ökotoxikológia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LogP | 1,51-1,69 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Egység SI és STP hiányában. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
A jód-metán , vagy más néven metil-jodidot , egy kémiai képletű vegyület CH 3 I, néha megjegyezte MeI. Ez egy halogén-alkánban , származó metán , ahol az egyik hidrogénatomot atomok szubsztituálva lett egy jód -atom . Ez formájában színtelen, sűrű, illékony folyadék egy éteri szag, amely úgy egy lilás arcbőr fény hatására jelenléte miatt a I 2 dióda.. A jód-metán általánosan használt szerves szintézis , mint a metilcsoport donor , a reakciók az úgynevezett metilezések . Ez természetesen kibocsátott, kis mennyiségben rizst .
A jód-metán hidrolizál 270 ° C , ezáltal kialakítjuk a hidrogén-jodid , a szén-monoxid és szén-dioxid .
Használ
transzferáz
Jód-metánt főleg a metilációs más vegyületek, a S N 2 típusú reakciókat . Könnyen megtámadta térbelileg nukieoíiiek és jodid jó nukleofil .
Ez lehet például használni a metilezése karbonsavak (átalakítása karboxil metanoát ) vagy fenolok (képződése methoxybenzenes):

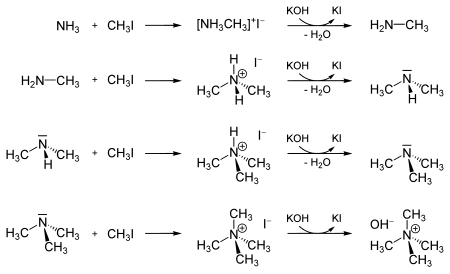
Azt is fel lehet használni a metilezése ammónia és az azokból származó aminok iodoammonium. Ez a reakció folytatódik, amíg a kialakulását a tetrametilammónium-hidroxid.
Jód-metánt is prekurzora metilmagnézium-jodid vagy „MeMgI”, egy Grignard-reagens gyakran használják a szerves szintézis . A MeMgI meglehetősen könnyen képződik, ezért gyakran használják példaként ezen reagensek előállításának tanításához. Használata MeMgI Azonban azt felváltotta a használata metil .
A Monsanto-eljárás során a MeI metanol és hidrogén-jodid reakciójával in situ képződik . Ezután ródium jelenlétében szén-monoxiddal reagálva etanil-jodidot képez , amely ecetsav prekurzor ( hidrolízissel nyert ). A világon előállított ecetsav nagy részét ezzel a módszerrel állítják elő.
Egyéb
Emellett a használatát, mint metilezőszerrel, néhány javaslatot használni jód, mint egy gombaölő , gyomirtó , rovarirtó , féregirtó vagy akár tűzoltó . Ezt fel lehet használni, mint egy talajfertőtlenítő helyett brómmetán (amelyek használata már betiltották a Montreali Jegyzőkönyv ) és mikroszkópos tulajdonságai kapcsolódó törésmutatója.
Gyártás és szintézis
Jód-metánt is szintetizálhatjuk exoterm reakció, a reakció a jód metanol jelenlétében foszfor . A diidode ezután transzformáljuk in situ át foszfor-trijodidot . Ebből következik, egy nukleofil szubsztitúciós metanol:
Egy másik módszer az, hogy reagáljon a dimetil-szulfát és kálium-jodid jelenlétében a kalcium-karbonát :
Ezután a jód-metánt nátrium-tioszulfáttal végzett mosás után desztillálással nyerhetjük a jódfelesleg eltávolítása céljából.
A jód-metánt nukleáris baleseteknél is elő lehet állítani, ha szerves vegyületeket "fúziós jóddal" reagáltatnak.
Jodometán választása metilezőszerként
A jodometán kiváló metilezőszer, de van néhány hátránya. Amellett, hogy mérgező ; összehasonlítva más halogén-metán ( különösen a klór-metán ) annak ekvivalens tömege nagyobb: egy mol Mel súlya majdnem háromszor annyi, mint egy mól MeCI. Azonban a klór-gáz (például a bróm-metán ), ami használatuk finomabb, mint jód, amely folyadék. A klór-metán sokkal gyengébb metilezőszer, mint a MeI, de a legtöbb reakcióban elegendő.
A jodidok általában sokkal drágábbak, mint klorid- vagy bromid-ekvivalenseik, de a megfizethető jodometán nem. Kereskedelmi méretekben a dimetil-szulfát előnyös, bár mérgező, mert olcsó és folyékony is.
A reakciók során a nukleofil szubsztitúció az indulás a kilépő csoport, I - vezethet oldalán reakciókat , mert ez egy erős nukleofil . Végül, a magas reakcióképessége miatt a MeI veszélyesebb a vele foglalkozó személyzet számára, mint brómozott és klórozott ekvivalense.
Toxicitási és biológiai hatásai
A jód-metánt egy DL 50 által orális adagolás a 76 mg · kg -1 a patkányok, és a májban, ez gyorsan átalakul S-metil- glutation . Az Egyesült Államokban, jód tekinthető potenciálisan rákkeltő szerinti besorolása EüM (en) , NTP és az EPA . A IARC sorolja azt a 3. csoport ( „osztályozhatatlan kell tartalmazniuk a karcinogenitás az emberekre”).
A jodometán gőzök belégzése károsíthatja a tüdőt, a májat, a vesét és az idegrendszert. Hányingert, szédülést, köhögést és hányást okoz. Hosszantartó érintkezés a bőrrel égési sérülést okoz. Massive inhalációs okozhat tüdőödémát .
Megjegyzések és hivatkozások
- (fr) Ez a cikk részben vagy egészben az angol Wikipedia " Metil-jodid " című cikkéből származik ( lásd a szerzők felsorolását ) .
- METIL-JODID , a Kémiai Biztonság Nemzetközi Programjának biztonsági lapja (i) , konzultáció 2009. május 9-én.
- számított molekulatömege a „ atomsúlya a Elements 2007 ” on www.chem.qmul.ac.uk .
- (a) Nicholas P. Chopey, Handbook of Chemical Engineering Számítások , McGraw-Hill,2004, 3 e . , 800 p. ( ISBN 978-0-07-136262-7 ) , p. 1.43.
- (in) " Különböző gázok tulajdonságai " a flexwareinc.com webhelyen (hozzáférés: 2010. április 12. ) .
- (a) Carl L. yaws, Handbook of termodinamikai diagramok: szervetlen vegyületek és Elements , Vol. 1., 2. és 3., Huston, Texas, Gulf Pub. Co.,1996, 384 p. ( ISBN 0-88415-857-8 , 0-88415-858-6 és 0-88415-859-4 ).
- (in) David R. LiDE, Handbook of Chemistry and Physics , Boca Raton, CRC,2008, 89 th ed. , 2736 p. ( ISBN 978-1-4200-6679-1 ) , p. 10-205.
- IARC munkacsoportja az embert érintő rákkeltő kockázatok értékelésére , " Evaluations Globales de la Carcinogenicité pour l'Homme, Groupe 3 : Unclassables as to carcinogenicity to Humans " , http://monographs.iarc.fr , IARC,2009. január 16(megtekintés : 2009. augusztus 22. ) .
- Index szám a 3.1 táblázat a mellékletben VI Az EK-rendelet n o 1272/2008 (16 2008 decemberében).
- „ Jódmetánt ” az adatbázis a vegyi termékek Reptox a CSST (Quebec szervezet felelős a munkahelyi biztonság és egészségvédelem), elérhető április 25, 2009.
- (en) KR Redeker, NY Wang, JC Alacsony, A. McMillan, SC Tyler és RJ Cicerone, „ kibocsátás Metil halogén- és metán a rizs rizsföldeken ” , Science , vol. 290,2000, P. 966–969 ( PMID 11062125 , DOI 10.1126 / science.290.5493.966 ).
- (a) CS King, WW Hartman: metil-jodid . In: Organic Synthesis , 1943, 2, S. 399 ( cikk ).
- (a) Johnson, K., " Metabolism jódmetánt a patkány " , Biochem J. , Vol. 98,1966, P. 38–43.
Bibliográfia
- Adams, RE, Browning Jr, WE, Cottrell, WB és Parker, GW (1965) A metil-jodid felszabadulása és adszorpciója a HFIR maximális hiteles balesetében (ORNL-TM-1291 sz . ) . Oak Ridge Nemzeti Labor Oak Ridge Nemzeti Lab. , Tenn.





