Levegő
| Levegő | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Azonosítás | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ATC kód | V03 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kémiai tulajdonságok | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Moláris tömeg | 28,965 g / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fizikai tulajdonságok | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fúzió | -216,2 ° C ( 1 atm ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° forráspontú | -194,3 ° C ( 1 atm , 874,0 kg / m 3 ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oldékonyság | 0,0292 térfogat / térfogat (víz, 0 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
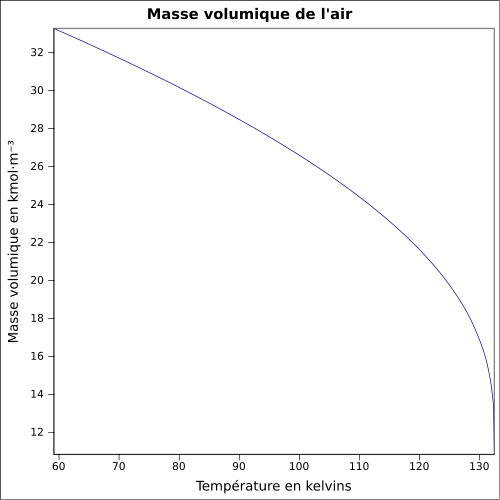
| Térfogat |
1,2 kg / m 3 ( 21,1 ° C , 1 atm )
egyenlet:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Telített gőznyomás |
egyenlet:
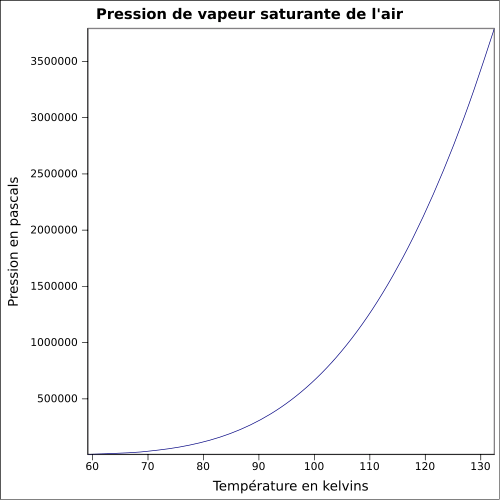
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritikus pont | -140,6 ° C , 3771 kPa , 351 kg / m 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hővezető | 0,023 4 W m −1 K −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termokémia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
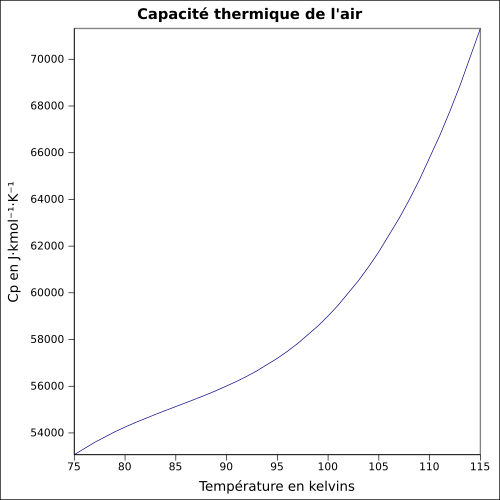
| C o |
egyenlet:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Optikai tulajdonságok | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Törésmutató | 1 00026825 ( 100 kPa , száraz levegő 450 ppm CO 2 -val ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Egység SI és STP hiányában. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
A levegő keveréke gázok alkotó légkörben a Föld . Normál esetben színtelen, láthatatlan és szagtalan.
Fogalmazás
A talaj közelében lévő száraz levegő homogén gázelegy. Körülbelül mólfrakcióból vagy térfogatból áll:
Azt is tartalmaz nyomokban a 0.000072% dihidrogén (0,72 ppmv ), hanem az ózon , valamint egy minimális jelenlétében radon . Tartalmazhat kén-dioxidot , nitrogén-oxidokat , finom szuszpendált anyagokat aeroszol formában , port és mikroorganizmusokat is.
Legtöbbször a Föld környezetében a levegő nedves, mert vízgőzt tartalmaz . A talaj közelében a vízgőz mennyisége nagyon változó. Ez az éghajlati viszonyoktól és különösen a hőmérséklettől függ. A levegőben lévő vízgőz parciális nyomását korlátozza telített gőznyomása, amely a hőmérséklettől függően nagyon változik:
| Levegő hőmérséklet | -10 ° C | 0 ° C | 10 ° C | 20 ° C | 30 ° C | 40 ° C |
| % vízgőz
1013 hPa légnyomás esetén |
0–0,2% | 0–0,6% | 0–1,2% | 0–2,4% | 0–4,2% | 0–7,6% |
A levegőben jelen lévő vízgőz százalékos arányát a páratartalom mértékével mérjük , ez az időjárás-előrejelzések fontos eleme. A hidrometria leírására több mennyiség is tartozik: abszolút páratartalom , amely megfelel a vízgőz tömegének a levegő térfogatára; és a relatív páratartalom , amely a vízgőz parciális nyomásának a telített gőznyomáshoz viszonyított százalékos aránya .
A szén-dioxid szintje idővel változik. Egyrészt körülbelül 6,5 ppmv ( p ection p ar m illion in v olume) amplitúdó éves változáson megy keresztül . Másrészt az átlagos éves ráta évente 1,2-1,4 ppmv-vel növekszik. Mintegy 384 ppmv (0,0384%) 2008 közepén volt 278 ppmv előtt ipari forradalom , 315 ppmv 1958, 330 ppmv 1974 és 353 ppmv 1990-ben ez az üvegházhatást okozó gázok üvegház fontos szerepet játszik a globális felmelegedés a Föld .
A metán egy másik gázfő üvegház, amelynek sebessége idővel növekszik: 800 mm 3 / m 3 (0,8 ppmv ) az ipar előtti korszakban, 1585 mm 3 / m 3 1985, 1663 mm 3 / m 3 1992-ben és 1 676 mm 3 / m 3 1996-ban.
Körülbelül 80 km tengerszint feletti magasságig a száraz levegő összetétele nagyon homogén, a levegő összetételének egyetlen jelentős változása a vízgőztartalomé.
Levegő összetétele
|
|
||||||||||||||||||||||||||||||||||||||||||||
A tömegarányok úgy értékelhetők, hogy a térfogatarányokat megszorozzuk a figyelembe vett gáz moláris tömegének és a levegő moláris tömegének, azaz 28,976 g mol-- 1 arányának , például CO 2 esetén.. Ez az arány nem elhanyagolható, mivel 44 / 28,976 = 1,5185 egyenlő , ezért a CO 2 tömegtartalmalevegőben 415 × 1,5185 = 630 ppmm .
Térfogat
Mivel a levegő összenyomható gáz, sűrűsége ( kg / m 3 -ben ) a nyomás, a hőmérséklet és a páratartalom függvénye.
Száraz levegő normál légköri nyomáson ( 1013,25 hPa ):
Általában úgy 1,293 kg / m 3 , hogy 0 ° C-on és 1,204 kg / m 3 , hogy 20- ° C .
Ezt generalizált ( ideális gáz képlet ) a: (a T a Kelvinben és P a pascalban szerinti SI egyezmények). A hőmérséklet θ Celsius fokban, a hőmérséklet T kelvinben hozzáadásával kapott 273,15, hogy θ : T (K) = θ (° C) + 273,15 .
Globális felmelegedési potenciál
A globális felmelegedési potenciál (GWP angolul : GWP: Globális felmelegedési potenciál ) vagy ezzel egyenértékű CO 2lehetővé teszi az egyes üvegházhatású gázok „károsságának” mérését .
Az alábbi táblázat a levegőben található fő üvegházhatású gázok GWP-értékét adja meg:
| PRG | 1 (hivatkozás) | 8 | 23. | 310 | 1300-tól 1400-ig | 6 200-tól 7 100-ig | 6500 | 22,800 |
| gáz | szén-dioxid | vízpára | metán | dinitrogén-oxid (N 2 O) | klór-difluor-metán (HCFC) | diklór-difluor-metán (CFC) | szén-tetrafluorid (CF 4 ) | kén-hexafluorid (SF 6 ). |
Törésmutató
A levegő törésmutatójának kifejezése "standard körülmények között":
azzal , ahol a hullámhossz nanométerben kifejezve (nm), ahol az a kölcsönös a hullámhossz mikrométer.Száraz, 0,03% szén-dioxidot tartalmazó levegőre vonatkozik, 101 325 Pa (760 milliméter higany) nyomáson és 288,15 kelvin ( 15 ° C ) hőmérsékleten .
N- t kapunk különböző hőmérsékleten vagy nyomáson, az alábbi két kifejezés egyikének használatával:
val vel:
- T , hőmérséklet kelvinben kifejezve ;
- p , nyomás passzban;
- T s , 288,15 K ;
- p s , 101,325 Pa ;
- n s , a fent megadott levegő törésmutatója,
vagy:
val vel:
- T , hőmérséklet Celsius-fokban ;
- T s , 15 ° C ;
- p , nyomás Hgmm-ben ;
- p s , 760 Hgmm ;
- , 0,00366 K- 1 ;
- , (1,049 - 0,015 T ) × 10 -6 Hgmm -1 ;
- 8,13 × 10 -7 Hgmm -1 ;
- n s , a fent megadott levegő törésmutatója.
Termofizikai tulajdonságok
Frank M. White által közzétett táblázatokból, Heat and Mass transfer , Addison-Wesley, 1988.
val vel:
- T , hőmérséklet Kelvinben ;
- ρ , sűrűség ;
- μ , dinamikus viszkozitás ;
- ν , kinematikai viszkozitás ;
- C p , fajlagos hő állandó nyomáson ;
- λ , hővezetőképesség ;
- a , termikus diffúzió ;
- Pr , Prandtl szám .
| T | ρ | μ | v | C o | λ | nál nél | Pr |
|---|---|---|---|---|---|---|---|
| K | kg m −3 | kg m −1 s −1 | m 2 s −1 | J kg −1 K −1 | W m −1 K −1 | m 2 s −1 | - |
| 250 | 1.413 | 1,60 × 10 −5 | 0,949 × 10 −5 | 1,005 | 0,0223 | 1,32 × 10 −5 | 0,722 |
| 300 | 1.177 | 1,85 × 10 −5 | 1,57 × 10 −5 | 1,006 | 0,0262 | 2,22 × 10 −5 | 0,708 |
| 350 | 0,998 | 2,08 × 10 −5 | 2,08 × 10 −5 | 1,009 | 0,0300 | 2,98 × 10 −5 | 0,697 |
| 400 | 0.883 | 2,29 × 10 −5 | 2,59 × 10 −5 | 1,014 | 0,0337 | 3,76 × 10 −5 | 0,689 |
| 450 | 0.783 | 2,48 × 10 −5 | 2,89 × 10 −5 | 1,021 | 0,0371 | 4,22 × 10 −5 | 0,683 |
| 500 | 0,705 | 2,67 × 10 −5 | 3,69 × 10 −5 | 1,030 | 0,0404 | 5,57 × 10 −5 | 0,680 |
| 550 | 0.642 | 2,85 × 10 −5 | 4,43 × 10 −5 | 1,039 | 0,0436 | 6,53 × 10 −5 | 0,680 |
| 600 | 0,588 | 3,02 × 10 −5 | 5,13 × 10 −5 | 1,055 | 0,0466 | 7,51 × 10 −5 | 0,680 |
| 650 | 0,543 | 3,18 × 10 −5 | 5,85 × 10 −5 | 1,063 | 0,0495 | 8,58 × 10 −5 | 0.682 |
| 700 | 0,503 | 3,33 × 10 −5 | 6,63 × 10 −5 | 1,075 | 0,0523 | 9,67 × 10 −5 | 0,684 |
| 750 | 0.471 | 3,48 × 10 −5 | 7,39 × 10 −5 | 1,086 | 0,0551 | 10,8 × 10 −5 | 0.686 |
| 800 | 0.441 | 3,63 × 10 −5 | 8,23 × 10 −5 | 1,098 | 0,0578 | 12,0 × 10 −5 | 0,689 |
| 850 | 0,415 | 3,77 × 10 −5 | 9,07 × 10 −5 | 1 110 | 0,0603 | 13,1 × 10 −5 | 0,692 |
| 900 | 0,392 | 3,90 × 10 −5 | 9,93 × 10 −5 | 1,121 | 0,0628 | 14,3 × 10 −5 | 0,696 |
| 950 | 0,372 | 4,02 × 10 −5 | 10,8 × 10 −5 | 1,132 | 0,0653 | 15,5 × 10 −5 | 0,699 |
| 1000 | 0,352 | 4,15 × 10 −5 | 11,8 × 10 −5 | 1,142 | 0,0675 | 16,8 × 10 −5 | 0,702 |
| 1,100 | 0,320 | 4,40 × 10 −5 | 13,7 × 10 −5 | 1,161 | 0,0723 | 19,5 × 10 −5 | 0,706 |
| 1200 | 0,295 | 4,63 × 10 −5 | 15,7 × 10 −5 | 1,179 | 0,0763 | 22,0 × 10 −5 | 0,714 |
| 1,300 | 0,271 | 4,85 × 10 −5 | 17,9 × 10 −5 | 1,197 | 0,0803 | 24,8 × 10 −5 | 0,722 |
A hőmérséklet és a levegő hővezetési tényezője közötti kapcsolat 100 K és 1600 K közötti hőmérsékleten érvényes :
vagy:
- : a hőmérséklet K-ban kifejezve
- : hővezető képesség W m −1 K −1
A levegő dinamikus viszkozitása és a hőmérséklet viszonya:
vagy:
- : hőmérséklet K-ban
- : dinamikus viszkozitás kg m −1 s −1
A levegő kinematikus viszkozitása és a hőmérséklet közötti kapcsolat a következő:
vagy:
- : hőmérséklet K-ban
- : kinematikai viszkozitás m 2 / s-ban
A WPI (en) információ szerint a fajlagos levegő hő és a hőmérséklet közötti kapcsolat a következő:
vagy:
- : hőmérséklet K-ban
- : fajlagos hő J kg −1 K −1
Nyomás
Mivel a csökkenés levegő nyomása a magasság , szükséges, hogy nyomás a kabinok repülőgépek és más légi jármű . A gyakorlatban a kabinokban alkalmazott nyomás nagyobb, mint a külső nyomás, bár kisebb, mint a talajszint nyomása.
A sűrített levegőt a búvárkodás során is használják .
Cseppfolyósítás
A levegő különböző gázokból áll, amelyek megfelelő lehűlés esetén végül folyékony állapotba , majd szilárd állapotba kerülnek . Például az oxigén -218 ° C hőmérsékleten szilárdtá válik , a nitrogén -195 ° C-on cseppfolyósodik . A hőmérséklet -270 ° C (körülbelül 3 K ), az összes gáz kivéve hélium ezután a szilárd és így kapjuk az „fagyott levegő”.
A levegőt nem lehetett cseppfolyósítani, mielőtt ismertek azok a kritikus nyomások és hőmérsékletek, amelyek ismerik azokat az elméleti határokat, amelyeken túl egy vegyület csak gázállapotban létezhet. Mivel a levegő keverék, ezeknek az értékeknek nincs szigorú jelentése, de valójában –140 ° C feletti hőmérsékleten a levegő már nem cseppfolyósítható.
A levegő alkatrészeinek forrási hőmérséklete
| Vezetéknév | Képlet | Hőfok |
|---|---|---|
| Dinitrogén | 2. sz | -195,79 ° C , folyékony nitrogén |
| Dioxigen | O 2 | –183 ° C , folyékony oxigén |
| Argon | Ar | -185,85 ° C |
| Szén-dioxid | CO 2 | -56,6 ° C át 5,12 atm |
| Neon | Született | -246,053 ° C |
| Hélium | Hé | -268,93 ° C , folyékony hélium |
| Nitrogén-monoxid | NEM | -151,8 ° C |
| Kripton | Kr | -154,34 ° C |
| Metán | CH 4 | -161,52 ° C |
| Dihidrogén | H 2 | -252,76 ° C , folyékony hidrogén |
| Dinitrogén-oxid | N 2 O | -88,5 ° C |
| Xenon | Xe | -108,09 ° C |
| Nitrogén-dioxid | NO 2 | 21,2 ° C |
| Ózon | O 3 | -111,9 ° C |
| Radon | Rn | -61,7 ° C |
Az első csepp folyékony levegőt szinte egyidejűleg, Louis Paul Cailletet és Raoul-Pierre Pictet kapta meg 1877-ben , hirtelen tágulással 300 és 1 atmoszféra között.
A 1894 , a holland fizikus Heike Kamerlingh Onnes fejlesztette ki az első cseppfolyós levegő telepítést. Az elkövetkező 40 évben a francia, nagy-britanniai, németországi és oroszországi kutatók számos fejlesztést hajtottak végre a folyamaton.
Sir James Dewar első cseppfolyós hidrogén a 1898 és Heike Kamerlingh Onnes hélium, a legnehezebb gáz felenged, a 1908 .
Függetlenül Carl von Linde , Georges Claude kifejlesztett 1902 egy ipari folyamat cseppfolyósító levegőt.
Szimbolikus
- Nem tudományterületen a levegő egyike annak a négy elemnek (a tűzzel , a vízzel és a földdel együtt ), amelyeket egykor az anyagoknak tekintettek (és egyes kultúrákban még mindig figyelembe vettek), amelyek az egész életen át alapulnak. Ő a Lélek szimbóluma.
- A levegőt gyakran más különféle fogalmakkal is társítják, például a tarot fedélzeti kardcsaládhoz .
Megjegyzések és hivatkozások
Megjegyzések
- Ez a száraz levegő moláris tömege.
Hivatkozások
- " Air " , az olivier.fournet.free.fr webhelyen (megtekintve : 2010. március 4. )
- (en) Sűrítettgáz-társulás, Sűrített gázok kézikönyve , Springer,1999, 4 th ed. , 702 p. ( ISBN 0-412-78230-8 , online olvasás ) , p. 234
- (en) Robert H. Perry és Donald W. Green , Perry vegyészmérnökök kézikönyve , USA, McGraw-Hill,1997, 7 -én ed. , 2400 p. ( ISBN 0-07-049841-5 ) , p. 2-50
- (a) Philip E. Ciddor, " Törésmutató levegő: új egyenletek a látható és a közeli infravörös " , Applied Optics , Vol. 35, n o 9,1996, P. 1566-1573 ( DOI 10.1364 / AO.35.001566 )
- (in) A legújabb globális CO2 a noaa.gov oldalon, hozzáférés 2021. április 21.
- (in) A Keeling Curve , a keelingcurve.ucsd.edu webhely, 2015. április 23.
- CO 2 koncentráció a föld légkörében
- CO 2 koncentráció Mauna Loán (Hawaii), NOAA.
- A metán koncentrációja Mauna Loán (Hawaii), NOAA.
- A gyakorlatban az erősen szárított levegő még mindig tartalmaz vízgőz nyomokat.
- Adatforrás: Szén-dioxid: (en) NASA - Earth Fact Sheet , 2007. január. Metán: IPCC TAR; 6.1 táblázat, 1998 (en) Az IPCC harmadik értékelési jelentése: "Climate Change 2001" , GRID-Arendal 2003-ban. A NASA összértéke 17 ppmv volt a 100% -ból, és a CO 2itt 15 ppmv-vel nőtt . Normalizálni, N 2 csökkenteni kell 25 ppmv és az O 2 7 ppmv .
- " Légtörési index " , az olivier.fournet.free.fr webhelyen (megtekintve : 2010. március 4. )
- vegyipari szakemberek
- Vegyipari szakemberek , nem találhatók 2013. augusztus 11
- Ez a dokumentum a WPI webhelyéről , a wpi.edu webhelyről
Lásd is
Kapcsolódó cikkek
- Légsűrűség
- Légtömeg
- Pszichrometria
- Párás levegő
- Légszennyezés és cikkei a következő kategóriából: Légszennyezés
- Levegő minősége