Nukleáris gyógyszer
Nukleáris gyógyszer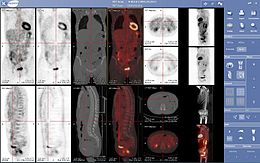
| Alosztálya | Gyógyszer |
|---|---|
| Gyakorolta | Nukleáris orvos ( in ) |
A nukleáris medicina magában foglalja az összes orvosi alkalmazásai radioaktivitás a gyógyszert .
Közigazgatásilag nem lezárt radioaktív források használatáról beszélünk.
A pácienst ( intravénás injekcióval , lenyeléssel , inhalációval stb.) Radiofarmakonok adják be ; ezek lehetnek izolált radionuklidok (például a jód a pajzsmirigy számára ), vagy vektorból és radionuklidból állhatnak. Egy "vektor" molekula, amely az emberi anyagcsere része, vonzódni fog egy célszervhez, vagy nyomon követi a szervezet működését. A hozzákapcsolt radionuklid-nyomjelző ionizáló sugárzást bocsát ki, amely detektálható (képalkotás vagy szcintigráfia), vagy felhasználható a sejtek elpusztítására (belső vektorizált sugárterápia). Ez a módszer nagyon érzékeny és lehetővé teszi a diagnózist vagy a kezelést.
A különböző alkalmazási területek a következők:
- funkcionális in vivo képalkotás, amely radioaktív nyomjelző beadásából áll a beteg számára, lehetővé téve annak külső detektálását. Ezek szcintigráfiák (gammasugarak kibocsátása) vagy pozitronemissziós tomográfia (PET);
- a metabolikus sugárkezelés, amely jóindulatú betegségeket (hipertireózis, policitémia vera ...) és rosszindulatú betegségeket (pajzsmirigyrák, prosztatarák áttétek ...) kezel
- in vitro biológiai diagnózis: radioimmunológia ;
A nukleáris orvoslás egy átfogó orvosi szakterület, amely egyszerre diagnosztikai ( in vivo és in vitro ) és terápiás.
Történelem
Frédéric és Irène Joliot-Curie mesterségesen előállított radioaktív izotópok (radionuklidok) 1934-es felfedezése jelentette ennek az új orvosi tudományágnak a megjelenését.
A radioizotópok első alkalmazása terápiás volt. 1936-ban a foszfort 32 alkalmazták leukémia kezelésére . 1938-ban John Livingoodnak és Glenn Seaborgnak sikerült kifejlesztenie a jód termelését. 1941-ben radioaktív jódot adtak a pajzsmirigy-túlműködésben szenvedő betegeknek .
1946-ban Samuel Seidlin, Leonidas Marinelli és Eleanor Oshry kimutatták, hogy a pajzsmirigyrákban szenvedő betegek összes metasztázisa megsemmisülhet a 131. jóddal végzett kezelést követően. Ez a kezelés a mai napig a leghatékonyabb módszer a rák esetében.
Az első gamma kamerát 1957-ben fejlesztette ki Hal Anger, és ez lehetővé tette egy teljes felület radioaktivitásának mérését egyszerre.
Henri Wagner 1963-ban radioaktívan megjelölt albumin aggregátumok felhasználásával elkészítette az első tüdőképeket. 1978-ban David Goldenberg jelölt antitesteket használt az emberi tumorok képalkotására. A szcintigráfia 1962-ben jelent meg David Kuhl vezetésével .
1971-ben a nukleáris orvostudományt az American Medical Association orvosi szakterületként ismerte el.
Jelenleg Franciaországban a nukleáris orvoslás elismert orvosi szakterület.
Diagnosztikai
Általános elv
A nukleáris gyógyászatban a beteg intravénás úton, orálisan vagy inhalálva kap radioaktív gyógyszert a vizsgálatot vagy az elvégzendő terápiát követően.
A szcintigráfiában (nukleáris gyógyászati képalkotás) a képeket (diagnosztizálás céljából) külső detektorok (gamma-kamerák) segítségével állítják elő, amelyek az ionizáló sugárzás arányos detektorai (fotonkibocsátók), és lehetővé teszik a kép előállítását, de a mennyiségi meghatározásokat is. Ez a folyamat különbözik a röntgendiagnosztikától , ahol a sugárzás külső és a testen áthaladva képet alkot. A nukleáris képalkotás lehetővé teszi a szervezet működésének megfigyelését, miközben a radiológia (és különösen a röntgen szkenner) információt nyújt a szerkezetről. Ez funkcionális képalkotás, szemben az anatómiai képalkotással.
Jelenleg a gamma-kamerák egyre inkább szkennerekkel vagy MRI-kkel párosulnak, amelyek lehetővé teszik a fúziós képek előállítását, strukturális információkat és fiziológiai vagy metabolikus információkat adva egyetlen vizsgálat során.
Felfedezhetjük a metabolizmusok nagy részét: a máj-epe, a pajzsmirigy, a szellőzés és a tüdő perfúziója, a vese és a vizeletfa szerkezete és működése, a csont anyagcseréje (törések, áttétek keresése, algoneurodystrophia), az agy anyagcseréje, a cső emésztőrendszer (különösen a gyomor kiürülése), a bal kamra működése, a bal kamra miokardiális szövetének működése ... A szcintigráfiák közelmúltbeli pozitronkibocsátóinak hozzájárulása tovább növelte a diagnosztikai lehetőségeket.
A nukleáris orvoslás számszerűsítésre alkalmas. Valójában a vizsgálat során a radioaktivitás mérésének eredménye arányos a térfogattal vagy a funkcionális aktivitással.
Egyes technikák lehetővé teszik a dinamikus rekonstrukciót (mozgást) a különböző időpontokban ( szív , vese) készített képek egymásra helyezésével .
Jelenleg két szcintigráfiai technikát alkalmaznak:
- egyfoton emissziós tomográfia (TEMP)
- pozitronemissziós tomográfia (PET)
Azonban nem szüntették meg teljesen a sík, dinamikus szcintigráfiát.
Szcintigráfia
A szcintigráfia elve abban áll, hogy a betegnek nagyon kis mennyiségű radiofarmakonot adnak be. A radiofarmakon által kibocsátott foton sugárzást, egy szervben koncentrálódva vagy egy funkció nyomon követését gamma kamera érzékeli. A szcintigráfia során gamma-sugarakat kibocsátó radioizotópot tartalmazó radiofarmakonokat használnak .
A célrészhez rögzítve a gyógyszerészeti rádió gammasugarakat bocsát ki, amelyeket egy szcintillációs kamera észlel, amelyet általában gamma-kamerának hívnak . Ezt az információt ezután egy számítógép rekonstruáló algoritmus segítségével dolgozza fel, hogy megkapja a megcélzott testrész 2D vagy 3D képét.
Különösen a következő kutatások különböztethetők meg:
- A miokardiális szcintigráfia lehetővé teszi a szívizom perfúziójának, vagyis a szívizomba , különösen a bal kamrába érkező véráramlás tanulmányozását (lehetővé teszi az angina vagy a szívinfarktus következményeinek diagnosztizálását).
- A szívkamrák szcintigráfiája, amely lehetővé teszi a kamrai ejekciós frakció (különösen a bal) mérését, amely fontos paraméter bizonyos kardiotoxikus kemoterápiás kezelések nyomon követésében.
- A szcintigráfia Pulmonary lehetővé teszi a képalkotó szellőzés funkcióinak és a tüdő perfúziójának diagnosztizálását a tüdőembólia szempontjából. Jelenleg ez a diagnózis referencia-módszere, különösen terhes nőknél.
- A csont-scan , hogy szemléltesse a növekedés a csont. Törések ( Silverman-szindróma vagy ütött gyermekek, röntgenfelvételen észrevétlen törések stb.), Neuroalgo-dystrophia vagy osteophil rákos megbetegedések (emlő, vese, pajzsmirigy, prosztata, tüdő) egyetlen vizsgálatában javallt. )
- A dinamikus vese szcintigráfia lehetővé teszi egy nyomjelző vese általi felvételének és kiürítésének tanulmányozását. A DMSA szcintigráfia lehetővé teszi a fertőzés utáni következmények vagy hegek vizualizálását.
- Agy szcintigráfiával elemzik az infúzió eloszlását az agyban. Bizonyos degeneratív betegségek (Alzheimer-kór, frontotemporális dementiák) esetén azonban a perfúziós rendellenességek az agy meghatározott területeit érintik, ami lehetővé teszi a diagnózis orientálását. A Datscan szcintigráfiával a Parkinson-szindrómák diagnosztizálására is lehetőség nyílik.
- A pajzsmirigy szcintigráfiáját a hyperthyreosis különböző formáinak megkülönböztetésére is használják (Graves-kór, alaposított golyva, forró csomók, toxikus csomók stb.)
- Emésztőrendszeri szcintigráfiát végeznek a gyomor kiürülésének felmérésére (különösen a cukorbetegség értékelésében).
- Hepatobiliaris szcintigráfiát végeznek az epeutazás vizsgálatára.
Vannak más lehetséges vizsgálatok (nyirok, bizonyos neuro-endokrin daganatok stb.)
TEMPAz egyfoton emissziós tomográfia (SPECT) egy szcintigráfián alapuló funkcionális képalkotó technika. A gamma kamera 180 vagy 360 fokkal elfordul a beteg körül, hogy képeket készítsen. Rekonstrukciós algoritmus segítségével a számítógép rekonstruálja a szervben lévő radionuklidok háromdimenziós eloszlásának képeit. A SPECT-nek kollimátorra van szüksége a célszervre vagy funkcióra merőleges fotonok kiválasztásához. Ezt a kollimátort hozzá kell igazítani a radionuklidok által kibocsátott fotonok energiájához (nagy energiájú kollimátor például a 131-es jódhoz). Ez a folyamat nagy mennyiségű foton elvesztését indukálja, és megmagyarázza a képek relatív rossz minőségét. A fotonikus jel érzékenysége azonban olyan, hogy ez a típusú képalkotás nagyon hatékony.
HÁZI KEDVENCA pozitronemissziós tomográfia (PET) egy szcintigráfia, amely pozitronkibocsátó radionukliddal (béta +) jelzett radiofarmakon beadását jelenti a betegnek. Miután kibocsátott és után egy rövid út a sorrendben a milliméter, a pozitron fog megsemmisíteni egy középső elektron előidéző kibocsátása két gamma foton a 511 keV ellenkező irányban (180 °). Ezeknek a fotonoknak a detektálása véletlenszerűen és PET kamera segítségével történik; amely lehetővé teszi az emisszió helyzetének és a nyomjelző koncentrációjának az egyes pontokban történő meghatározását. Az egybeeséseket rekonstrukciós algoritmus segítségével tomográfiai képekké alakítják, és így rekonstruálják a szerv 3D képét.
A leggyakoribb nyomjelzők a nagyon rövid felezési idővel rendelkező radionuklidok, amelyek glükózmolekulákhoz kapcsolódnak, és amelyek a legtöbb cukrot fogyasztó szövetekhez kötődnek, különösen a rákos sejtekhez. A fluor ( 18 F) jelenleg a legszélesebb körben alkalmazott pozitron-kibocsátó. De vannak más használható radionuklidok is, például 15 O, 13 N és 11 C. Ezen elemek nagyon rövid felezési ideje azt jelenti, hogy csak akkor használhatók, ha egy termelési ciklotron a létesítmény közelében van.
A PET-t eredetileg neurológiára (epilepsziát, Parkinson- vagy Alzheimer-kórt okozó agykárosodások felderítésére) és kardiológiára (a szívizmok rendellenességeinek kimutatására) fejlesztették ki; jelenleg a PET-et elsősorban onkológiára fejlesztik.
Páros képalkotásJelenleg a legtöbb gamma-kamera (TEMP vagy PET) röntgenszkennerhez (vagy a jövőben MRI-hez) kapcsolódik, amely lehetővé teszi a szkenner által nyújtott strukturális információk és a szcintigráfia által szolgáltatott metabolikus vagy fiziológiai információk összekapcsolását, vagy inkább egyesítését. .
Szcintigráfia Franciaországban
Franciaországban 2013-ban valamivel több mint 460 gamma kamera és mintegy 118 PET-CT vizsgálat volt 220 nukleáris gyógyászati központban.
Évente több mint egymillió szcintigráfiát és közel 250 000 PET-vizsgálatot végeznek Franciaországban a Nukleáris Orvosi Központokban (2013-as SFMN-adatok).
Összehasonlítás más diagnosztikai módszerekkel
A képalkotás a nukleáris gyógyászatban funkcionális képalkotás, amely nem ugyanazt az eredményt adja, mint az egyszerű anatómiai képalkotás. De a vizsgálat nem helyettesíti a felvételeket és az MRI-t , csak bizonyos esetekben egészíti ki őket (agydaganatok, megismétlődés gyanúja stb. Esetén). A PET-vizsgálat azonban információt nyújt az orvosnak a szövetek anyagcseréjéről. A PET olyan kisméretű daganatokat mutathat ki, amelyek nem láthatók CT-n vagy MRI-n, amelyek diagnózisát akkor meg kell erősíteni. A PET a kemoterápia aktivitására is utalhat.
A következő táblázat összefoglalja ezeket az információkat:
| Az orvosi képalkotás típusa | Ultrahang | Röntgen képalkotás | MRI | Radioizotóp képalkotás |
|---|---|---|---|---|
| Elv | Az ultrahangnyalábot egy szonda bocsátja ki a test egy részére, továbbadható, elnyelhető vagy visszaverődhet attól függően, hogy milyen szövetekkel találkozik. A nyaláb változásainak elemzése lehetővé teszi a kép kialakítását | A testen röntgensugár kerül. Minél sűrűbb a keresztezett rész, annál több sugár szívódik fel. Az átvitt sugarakat egy film rögzíti. | Az erős és stabil mágneses mező létrehozza a szöveti mágnesezést, a gyengébb oszcilláló mágneses mezők precessziós jelenséget eredményeznek, amely mérhető elektromágneses jelet eredményez. | |
| Alkalmazás | A has, a nemi szervek, az izmok felépítése, a szív működése. | A csontok, a tüdő felépítése. | kardiológia, neurológia, a has felépítése. | bármilyen funkcionális feltárás |
| Vizsga időtartama (perc) | 5-15 | 5-15 | 20–60 | a vizsgától függ. A radionuklid beadása és a képek készítése között gyakran van várakozási idő. |
| érzékenység | Az érzékenység a mélységgel csökken. 3D képek. | a lágyrész kivételével érzékeny. 2D képalkotás (3D szkennerhez) | érzékeny a lágy szövetekre. 3D képek. | Célzott és pontos. 3D képek. |
| Kockázatok | A szövetek melegítése. | alacsony ionizáló sugárterhelés a hagyományos radiológiában. Az expozíció egy kicsit fontosabb a szkennerben. Kiegyensúlyozottnak kell lennie a módszer nagyon fontos diagnosztikai előnyével. | A szövetek melegítése. | alacsony ionizáló sugárterhelés. A kapcsolt vizsgálatok során hozzá kell adni az elvégzett vizsgálathoz kapcsolódó expozíciót |
Terápiás alkalmazások
Vektorizált belső sugárterápia (korábban metabolikus sugárterápia)
Fontosak a nukleáris orvoslás terápiás alkalmazásai.
A RIV-t általában használják
Sugárterápia jóddal 131A 131 jód radioaktív forrását minden beteg számára külön rendeljük meg , a kezeléshez szükséges aktivitásnak megfelelően. Ezt a forrást leggyakrabban kapszula formájában adják be. Azokban a ritka esetekben, amikor a beteg nem tud lenyelni, folyékony formák lehetségesek.
hyperthyreosis (akár Graves-kór, akár mérgező csomó) kezelésére.Ehhez olyan forrásokat használnak, amelyek aktivitása 300-800 MBq nagyságrendű jód-131.
Marinelli képlete elméleti számítást tesz lehetővé. Azonban leggyakrabban a beteget hypothyreosisban (LT4 hormonterápiával kezeljük), mint euthyreosisban próbáljuk a betegség megismétlődésének veszélye miatt felvenni.
pajzsmirigyrák kezeléséreA teljes pajzsmirigy-eltávolítás után és a patológia eredményeitől függően a 131-es jóddal történő kezelésre lehet szükség. Ennek a kezelésnek a célja a pajzsmirigy-maradványok elpusztítása (szinte mindig létezik), valamint az áttétek feltárása és kezelése. A kezelt tevékenységek 1,1–5,5 GBq-ig terjednek. A legtöbbet kezelt aktivitás azonban 3,7 GBq. Ezt a kezelést az agyalapi mirigy TSH-termelésének stimulálásával végzik, hogy a fennmaradó pajzsmirigy-sejteket a lehető legnagyobb mértékben stimulálják. Ez a stimuláció kiváltható hormonterápiától (az LT4 körülbelül egy hónapig történő leállítása) vagy endogén TSH (TyrogenΘ) injekciójával a jód bevételét követő 48 órán belül.
Egyéb jóindulatú patológiák kezeléseA polycythemia verát 32P-vel kezeljük.
Szinoviorthézisek (ízületi patológia kezelése) is megvalósíthatók az ízület méretéhez igazított radionuklidok intraartikuláris injektálásával.
Egyéb rosszindulatú (rákos) patológiák kezeléseMegemlíthetjük a 90Y-vel jelölt gömböket a hepatocarcinomák kezelésére, a feokromocitómák kezelését MIBG-131I-vel, a fájdalmas csontáttétek 223Ra-val történő kezelését, immunoradioterápiát stb.
A nukleáris orvostudomány terápiás alkalmazási területei új radionuklidok, például 177Lu vagy 223Ra alkalmazásával bővülnek.
| használat | Izotóp | Sugárzás | Felezési idő |
|---|---|---|---|
| Képalkotás | 18 F | 511 keV 2 fotonja | 110 perc |
| 99m Tc | 140 keV gamma | 6 óra | |
| 123 I | 159 keV gamma | 13 óra | |
| 111m A | Gamma 171 és 245 keV | 2,8 nap | |
| 201 TI | Gamma 167 keV | 3 nap | |
| 67 Ga | Gamma 92 keV | 3,3 nap | |
| Kezelés | 188 Re | Beta | 1 nap |
| 153 Sm | Béta és gamma | 1,9 nap | |
| 90 Y | Beta 2300 keV | 2,7 nap | |
| 177 Olvassa el | Beta | 6,7 nap | |
| 131 I | Béta és gamma | 8,2 nap | |
| 32 P | Beta | 14,4 nap | |
| 192 Ir | Beta | 74 nap |
99m Tc
A technécium-99m a radioizotóp, amely a nukleáris orvosi képalkotásban a leghasznosabb . Fizikai jellemzői szinte ideálisak erre a célra:
- a 6 órás felezési idő elég hosszú ahhoz, hogy lehetővé tegye az érdeklődő fiziológiai folyamatok követését, de elég rövid ahhoz, hogy korlátozza a felesleges besugárzást
- A gammafoton energiája , a 140 keV , ideális, mivel elég energikus ahhoz, hogy áthaladjon az élő szöveten, de elég alacsony ahhoz, hogy kényelmesen észlelhető legyen: hatékonyan képes megfogni egy nátrium-jodid kristály, amelynek tipikus vastagsága kb. 10 és 15 mm közötti nagyságrendű
- A gamma-fotonok bősége nagy, a bomlások körülbelül 98% -a . Kevés behatolatlan részecske bocsát ki, ami korlátozza az élő szövet által befogadott energia dózisát.
A technéciumot általában nátrium-pertechnetát formájában nyerik: Natco 4. Anionos tulajdonságai miatt ebben a formában használható . Ebben a formában valójában biológiai viselkedése utánozza a Cl- vagy I- anionok viselkedését . Így például kutathatjuk Meckel diverticuláit, vagy képet készíthetünk a pajzsmirigyről .
Azonban, annak fő felhasználási lesz, mint egy marker a biológiailag aktív molekulák . A kötődés egy atom a 99m Tc:
- különféle foszfátokkal vagy foszfonátokkal képessé tehetjük a csontanyagcserét (HDP, HMDP, DPD ...)
- bizonyos kelátképzőkkel, például a DTPA-val , a vesefunkciót képezik le. Ugyanaz a DTPA , aeroszol formájában kerül belélegzésre a tüdő szellőzésének feltérképezéséhez
- az albumin makroaggregátumai, amelyek lehetővé teszik a pulmonalis perfúzió képalkotását
- a diimino-ecetsavval vagy annak származékai, a hepatobiliáris funkció fog leképezni
- a különböző kolloidok , általában a kén , eloszlásának feltérképezésére Kupffer féle májsejtek
- a páciens vörösvértestjeire, hemangiomák vagy emésztőrendszeri vérzés ellenőrzésére
- bizonyos lipofil molekulákhoz , például MIBI vagy tetrofozmin, a regionális vér perfúzió feltérképezéséhez ; hasznos különösen a szívizom ischaemia értékelésében vagy bizonyos daganatok felkutatásában.
18 F
A Fluor 18 egy pozitronokat kibocsátó izotóp ; a 18 F fluor bomlását az 511 keV 2 fotonja fogja kimutatni, amelyet 180 ° -on emittálnak a megsemmisítés során, amikor a pozitron egy középső elektronnal találkozik .
A fluoratom atom sűrűsége megegyezik a hidrogén . A T1 / 2 109 percig tart. Az orvostudomány előnyei a rövid béta + útnak (jobb térbeli felbontás), az atom kis méretének és a rövid felezési időnek (az expozíció rövid időtartama) köszönhetők.
Különösen érdekes a neurológia, a kardiológia és az onkológia iránt, a dezoxi-glükóz molekula felcímkézésével, amelyet akkor 18FDG-nek hívtak (eredetileg a Brookhaven Nemzeti Laboratórium csapata javasolta 1976-ban). A 18 FDG vagy 2- [ 18 F] fluor-2-dezoxi-D-glükóz a glükóz analógja, amelyet a daganatos sejtek jelentős mennyiségben szívnak fel gyorsan fejlődő állapotban, és fokozott energiafogyasztást igényelnek, miközben a fruktóz romlása blokkolni lehet a 2 e hidroxilcsoport fluorral történő helyettesítésével , amely nem metabolizálódik, ami felhalmozódást eredményez a tumorsejtekben (vagy más sejtekben, amelyek gyorsan felszívják a glükózt: gyulladások, izomaktivitás, idegsejtek aktivitása).
A 18FDG a vezető pozitronemisszióval jelölt radiofarmakon (MRP) gyógyszer . Ez az 1 st plotter Regulatory Affairs (AMM) alkalmazott pozitronemissziós tomográfia (PET), a felfedezések az onkológiában.
A detektálás véletlenszerűen történik, általában PET típusú kamerával (még Anger típusú kamera is dupla CDET fejjel, szinte elhagyva)
A béta + emisszió kiterjedtebb sugárvédelmi intézkedések bevezetését igényli, mint a 99 m Tc-nél.
201 Tl
A tallium-201 egy izotóp a tallium olyan kémiai tulajdonságai hasonlóak a kálium . A sejtek a Na-K Atpase pumpán keresztül felszívódva elosztja magát a regionális vér perfúzió szerint. Régóta használják, különösen a szívizom vér perfúziójának értékelésére, általában elhanyagolják a technetizált lipofil markerek (MIBI, tetrofozmin) mellett.
Fizikai tulajdonságai valóban kevésbé optimálisak: gammafotonjainak energiája alacsony, az időtartama pedig kissé hosszú. A kapott képek tehát a csillapítás és a szóródás által okozott romlásnak vannak kitéve.
123 I
A jód-123 egy izotóp a jód használt, hogy tanulmányozza a pajzsmirigy anyagcserét. Gamma-fotonokban gazdag sugárzása és 13 órás felezési ideje miatt alkalmas képalkotó eszköz. Ezt alkalmazzák különösen pajzsmirigy szcintigráfia, hogy jelölje jobenguán alkalmazott szcintigráfia (MIBG) és ioflupán (DaTSCAN) szcintigráfia a dopaminerg pályákat .
131 I
A 131 a jód egy másik izotópja , gazdag béta sugárzási részecskékben és viszonylag hosszú, 8,2 napos felezési ideje nagyon elősegíti a kezelést. Túlműködő pajzsmirigy-csomók ablációjára, a pajzsmirigy túlműködésének bizonyos formáinak, például Graves-Basedow-kór vagy Plummer- kór kezelésére , vagy a jól differenciált pajzsmirigyrák (áttétes vagy hólyagos) metasztázisainak kimutatására és ablációjára használják. Azt is használják védjegy iobenguan a szcintigráfia (MIBG) helyébe a jód 123 ma.
Néhány kivételtől eltekintve a diagnózis során már nem használják.
67 Ga
A gallium-67 a gallium izotópja, amely utánozza a vas anyagcseréjét . Hasznos a csontvelő működésének képalkotására és bizonyos gyulladásos fertőzések vagy betegségek vizsgálatára. Limfómák vagy bizonyos daganatok miatt hagyták el, az FDG PET kiszorította.
111m A
Az indiummal jelölt DTPA ágyéki szúrással injekciózható a subarachnoidális térbe, hogy a cerebrospinalis folyadék termelését, migrációját és újrafelszívódását ábrázolja .
Megtalálhatjuk a páciens fehérvérsejtjeihez (in vitro) indiummal vagy technéciummal ellátott DTPA-t fertőzés kimutatása esetén is (hatékonyabb, mint a gallium ).
Főleg egy szomatosztatin-analóg: Octreoscan jelölésére szolgál.
Sugárvédelem
A nukleáris orvostudományban ionizáló sugárzást alkalmaznak. A "sugárvédelem" szabályait tehát a betegek, a munkavállalók, a lakosság és a környezet védelmére alkalmazzák. (európai irányelvek alkalmazása).
Az alkalmazott radiofarmakonokat nagyon kis mennyiségben adják be, és nem jelentenek farmakológiai problémát. (allergiát nem észleltek, gyakorlatilag nem bizonyított mellékhatás).
Fontos paraméter a radiofarmakon felezési ideje vagy tényleges periódusa. Ötvözi a radioaktív bomlást (amelyet a fizikai felezési idő vagy a felezési idő jellemez), valamint a gyógyszer fiziológiás felszabadulását és a radioaktivitást leggyakrabban a vizeletben vagy a székletben (a biológiai felezési idő vagy a felezési idő jellemzi).
A két fő sugárvédelmi szabályt kell alkalmazni, mint minden ionizáló sugárzást alkalmazó vizsgálatra és kezelésre:
- Indoklás: egyensúly az előny és a kockázat között
- Optimalizálás: a szükséges diagnosztikai információk vagy a kívánt terápiás hatás eléréséhez éppen szükséges sugárzás felhasználása.
A beadott tevékenységek függhetnek az életkortól (a vizsgálatot és a terápiát születésüktől kezdve gyermekeknél végzik), a súlytól és a magasságtól. Előfordul az is, hogy minden beteg számára azonos mennyiségű radioaktivitást adnak be, ezáltal lehetővé téve a "kalibrálást", amely hozzáférést biztosít a kvantitatív információkhoz (például a jód felvétele a pajzsmirigy által).
A magasabb aktivitást igénylő kezelések kórházi kezelést igényelnek (általában 48 órás nagyságrendben) a pácienseket olyan helyiségekben (ólmozottak), amelyek WC-je retenciós tartály rendszeréhez csatlakozik.
Sugárvédelmi tanácsokat kell adnia a nukleáris orvosnak, amikor elhagyja a nukleáris gyógyászati egységet, hogy segítsen csökkenteni a rokonok, a lakosság és a környezet expozícióját.
A szcintigráfiák túlnyomó többségében használt izotóp a technécium ( 99m Tc ). A technécium iránti kereslet egyre növekszik, mivel az előállításához használt reaktorok elöregednek. Ezek az atomreaktorok repesztik a katonai minőségű erősen dúsított uránt . A hasadási melléktermékek egyikét , a molibdént gyógyszeripari laboratóriumok csomagolják technécium-generátorokban . Valójában a molibdén a Tc szülőeleme, Tc-re bomlik. Ezeket a generátorokat ezután hetente vagy kéthetente szállítják a nukleáris gyógyászati osztályokhoz, ahol elkészítik a betegek szcintigráfiájához beadott radiofarmakonokat.
2007-ben és 2008-ban a kanadai és a holland reaktor meghibásodása vagy nagyjavítása nyomán a világ néhány hónapra elfogyott az orvosi izotópokból.
2009-ben, míg a nukleáris orvostudományban használt radioizotópokat előállító reaktorok többsége több mint 40 éves, a Francia Nukleáris Biztonsági Hatóság (ASN) emlékeztetett a rosszul biztosított radioizotóp-gyártás upstream kockázataira : " Az orvosi felhasználásra szánt rádióelemek hiányának kockázatát fel kell tüntetni. nem vezethet az őket előállító reaktorok biztonságának figyelmen kívül hagyásához ”. Az Ügynökség sürgeti, hogy ne hosszabbítsák meg a veszélyesen régi reaktorok működését, hanem kezdeményezzenek új, összehangolt nemzetközi megközelítést; Az ASN felkéri az egészségügyi hatóságokat, hogy „optimalizálják” a technécium 99m használatát , és találjanak alternatív módszereket annak előállítására, például gyorsítóval, valamint tanulmányozzák más orvosi képalkotó módszerek alkalmazását; robusztus gazdasági modellt kell építeni ezen rádióelemek gyártására. A jelenlegi modell valójában nem tartalmazza a rádióelemek gyártásának teljes költségét, különös tekintettel az állami kutatóreaktorokban előállított molibdén előállítási költségeire.
A molibdént termelő fő reaktorok kutató reaktorok, és régiek. Ezek :
- a Nemzeti Kutatási Univerzális Reaktor (NRU) a Chalk River Nukleáris Laboratóriumokban (Kanada); 1957 óta üzemel, 2007-ben kiterjesztett karbantartási leállításon esett át, 2007-ben, a Parlament által engedélyezett újraindítás után, a Kanadai Biztonsági Hatóság tanácsára (ez a reaktor adja a világ termelésének mintegy 40% -át);
- a nagyáramú reaktor (HFR) Pettenben (Hollandia); 1961 óta üzemel, 2008-ban meghibásodást tapasztalt, ami hiányhoz vezetett (ez a reaktor a világ termelésének mintegy 30% -át adja), közepén újra leállt.2009. május és legalább 2010 tavaszáig;
- A Safari reaktor a Pelindaba (Dél-Afrika); 1965 óta szolgálatban (a világ termelésének ~ 10% -a);
- Belga reaktor -2 (BR2) az SCK • CEN intézetben, Mol-ban (Belgium) ; 1961 óta szolgálatban (a világtermelés ~ 9% -a);
- Az OSIRIS reaktorban a CEA Saclay Központ (Franciaország); 1965 óta üzemel, és az ASN 2015 előtt leállítja, feltéve, hogy végrehajtanak egy jelentős biztonságfejlesztési programot (ez a reaktor adja a globális termelés körülbelül 5% -át, és ezt felül kellett volna vizsgálni, és ezért márciustól2010. szeptember).
Az RJH (Jules Horowitz reaktor) közelgő építése Franciaországban Cadarache-nál az Atomenergia és Alternatív Energiaügyi Bizottság (CEA) szerint kompenzálnia kell a főreaktorok meghibásodását, de 2025 előtt nem fog működni.
Másrészt fontos megjegyezni, hogy bizonyos izotópok előállítását: a PET összes izotópját (főleg fluor-18) és a klasszikus szcintigráfiához szükséges bizonyos izotópokat (például a 123 jódot vagy a tallium 201-et) sokkal több ciklotron termeli, elterjedt a különböző országokban. Ezt a decentralizált gyártási módot nem befolyásolják a fent említett hiánykockázatok, amelyek nem használnak atomreaktorokat. Nagyon fejlett tanulmányok lehetővé teszik a technécium-99m előállításához felhasznált molibdén-99 ciklotronok általi előállítását.
Megjegyzések és hivatkozások
- Zimmermann, Richard. , Nukleáris orvostudomány (Radioaktivitás a diagnózis és a terápia szolgálatában). , EDP Tudományok ,1 st január 2006, 192 o. ( ISBN 978-2-7598-0228-9 , OCLC 476159980 , online olvasás ) , 26. oldal
- " NUCLEAR MEDICINE " , az universalis.fr oldalon (hozzáférés : 2020. november 12. ) .
- http://gfme.free.fr/diagnostic/petscan.html
- Az orvosi rendeltetésű rádióelementekről szóló Főiskola állásfoglalását követő sajtóközlemény . „Az orvosi felhasználásra szánt rádióelemek hiányának kockázata nem vezetheti az őket előállító reaktorok biztonságának figyelmen kívül hagyását. » 2009. szeptember 16
- (en) Abrams DN Adelfang P Alldred K et al. , Nem HEU gyártási technológiák a Molybdenum-99 és a Technetium-99m számára , Bécs, Nemzetközi atomenergia-ügynökség , coll. "NAÜ Nukleáris Energia Sorozat / NF-T-5.4 sz.",2013, 75 p. ( ISBN 978-92-0-137710-4 és 920137710X , OCLC 830370852 , online olvasás [PDF] )
- http://meteopolitique.com/fiches/depistage/actualite/35/est-de-la-fin-du-nucleaire-medical.htm „A nukleáris orvoslás vége felé. "