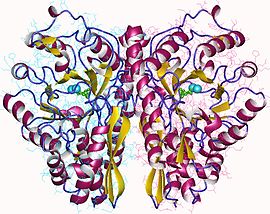
Enolase
A enoláz , alatt is ismert, a nevét phosphopyruvate hidratáz vagy 2-foszfoglicerát-dehidratáz , egy metalloenzim felelős katalizátort, amely átalakítja a 2-foszfo- D -glycérate (2PG) által foszfoenol (PEP), a 9 -én és az előzetes utolsó lépésében glikolízis :
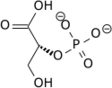
|
H 2 O + |

|
| 2-foszfoglicerát | Foszfoenol-piruvát |
Az enoláz a lyázok osztályába tartozik . Az enoláz a fordított reakciót is katalizálhatja, a táptalajban lévő szubsztrátok koncentrációjától függően. Ennek az enzimnek az optimális pH-ja 6,5. Az enoláz minden olyan szövetben és organizmusban jelen van, amely képes glikolízist vagy fermentációt végrehajtani . Az enzimet Lohmann és Meyerhof fedezte fel 1934-ben, és azóta különféle forrásszervekből, például emberi izomból és vörösvértestekből izolálták .
Foszfopiruvát-hidratáz Az élesztő dimer enoláz 2PG-vel és PEP- vel komplexálva ( PDB 2ONE ).
Az élesztő dimer enoláz 2PG-vel és PEP- vel komplexálva ( PDB 2ONE ).
| EK sz. | EK |
|---|---|
| CAS-szám | |
| Kofaktor (ok) | Magnézium |
| IUBMB | IUBMB bejegyzés |
|---|---|
| IntEnz | IntEnz nézet |
| BRENDA | BRENDA bejárat |
| KEGG | KEGG bemenet |
| MetaCyc | Metabolikus út |
| PRIAM | Profil |
| EKT | Szerkezetek |
| MEGY | AmiGO / EGO |
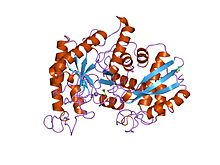 Enolase Homarus gammarus ( PDB 1PDZ )
Enolase Homarus gammarus ( PDB 1PDZ )
| Pfam | PF03952 |
|---|---|
| Pfam klán | CL0227 |
| InterPro | IPR020811 |
| PROPITÁS | PDOC00148 |
| SCOP | 1els |
| SZUPERCSALÁD | 1els |
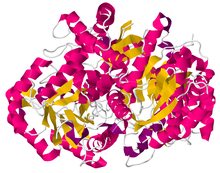 Humán Enolase 3 ( PDB 2XSX )
Humán Enolase 3 ( PDB 2XSX )
| Pfam | PF00113 |
|---|---|
| InterPro | IPR000941 |
| PROPITÁS | PDOC00148 |
Izoenzimek
Az enoláznak három alegysége van, az α, a ß és a γ, mindegyiket különböző gén kódolja , amelyek öt különböző izoenzim képződésével kombinálódhatnak : αα, αß, αγ, ββ és γγ. Ezen izoenzimek közül három (minden homodimer) gyakrabban található meg a felnőtt emberi sejtekben, mint a többi:
- Az αα vagy nem neuronális enoláz (NNE) mindenféle szövetben megtalálható, például a májban, az agyban, a vesében, a lépben
és a zsírszövetben. Enoláz 1-nek is nevezik - ββ vagy izomspecifikus enoláz (MSE). Más néven enoláz 3.
- γγ vagy neuron specifikus enoláz (NSE). Más néven enoláz .
Szerkezet
Az enoláz molekulatömege az izoformától függően 82 000 - 100 000 dalton . Humán alfa-enolázban a két alegység párhuzamosan orientált, így az egyik alegység Glu 20 ionos kötést képez a másik alegység Arg 414- jével. Minden alegységnek két különálló tartománya van. A kis N-terminális domén három alfa hélixből és négy béta lapból áll . A nagy C-terminális domén két β-lappal kezdődik, amelyet két α-hélix követ, és egy β-lemezekkel körülvett üreggel végződik, felváltva a β-lapokat körülvevő α-hélixekkel. Az enzim kompakt és gömbös szerkezete e két domén közötti jelentős hidrofób kölcsönhatások eredményeként jön létre.
Az enoláz egy nagyon jól védett enzim, öt aktív hellyel, amelyek különösen fontosak az aktivitás szempontjából. Ha összehasonlítjuk a vad típusú enoláz - mutáns enoláz, amely különbözik a Glu 168 , Glu 211 , Lys 345 , vagy Lys 396 maradékot - van egy olyan aktivitási szintet, amely csökkent faktorral 105. Hasonlóképpen Ezen a módon, a változások a His 159 az enolázt katalitikus aktivitásának csak 0,01% -ával mutatva hagyja. Az enoláz alapvető funkcióját két aktív Mg 2+ kofaktora szabályozza az aktív helyen, amelyek a szubsztrát negatív töltésének stabilizálását szolgálják.
-
Enoláz dimer 3D szerkezete antiparallel orientációban. A dimer Glu 20 N-terminálisa ionkötést képez a másik Arg 414 C-terminálisával, hogy stabilizálja az enzim kvaterner struktúráját.
-
Az enoláz aktív helye.
Gépezet
Izotópos próbák alkalmazásával a 2-PG PEP-vé történő átalakulásának teljes mechanizmusa egy E1cb-típusú eliminációs reakció, amely egy karbanion-köztiterméket tartalmaz. Az ezt követő részletes mechanizmus kristálytani és kémiai kinetikai vizsgálatokon alapul. Amikor a szubsztrát, a 2-foszfoglicerát, az a-enolázhoz kötődik, karboxilcsoportja koordinációs kötést képez az aktív hely két magnézium-ionjával. Ez stabilizálja a deprotonált oxigén negatív töltését, miközben növeli az alfa-hidrogén savasságát. A Lys 345 enoláz deprotonálja az alfa-hidrogént, és a keletkező negatív töltést a magnézium-kofaktor-ion rezonanciája stabilizálja a karboxilát oxigénjén . A köztes karbanion képződése után a C3-ban lévő hidroxid vízzel távozik a Glu 211-nek köszönhetően , és így képződik a PEP.
Ezenkívül az enzimen belül a katalízist elősegítő konformációs változások is előfordulhatnak. A humán α-enolázban a szubsztrát olyan helyzetben van, amely elősegíti az enzim megkötését a magnézium két katalitikus ionjával, a Gln 167 és Lys 396- tal való kölcsönhatás miatt . A Ser 36 hurkaiban történő mozgása a His 43 felé , a Ser 158 a Gly 162 irányába és az Asp 255 az Asn 256 felé történő mozgása lehetővé teszi, hogy a Ser 39 megkötődjön az Mg 2+ -val, és ezáltal bezárja az aktív helyet. A katalitikus magnéziumionokkal való összehangolás mellett az alfa-hidrogén szubsztrát pKa-értéke csökken a foszforilcsoport His 159 általi protonálása és Arg 374 közelsége miatt . Az Arg 374 felelős a Lys 345 aktív helyén történő deprotonálásáért is , biztosítva ezzel elsődleges szerepét a mechanizmusban.
Diagnosztikai felhasználások
A legutóbbi orvosi kísérletek során az enoláz koncentrációit mintavételezték bizonyos neoplasztikus állapotok és súlyosságuk diagnosztizálása céljából . Például a cerebrospinális folyadékban (CSF) az enoláz magasabb koncentrációi jobban korrelálnak a rosszindulatú asztrocitómák képződésével, mint más vizsgált enzimek (aldoláz, piruvát-kináz, kreatin-kináz és laktát-dehidrogenáz). Ugyanez a tanulmány kimutatta, hogy a tumor gyorsabban fejlődött azoknál a betegeknél, akiknél az enoláz koncentrációja nagyobb volt a cerebrospinalis folyadékban. Emelkedett enolázt is azonosítottak olyan betegeknél, akik a közelmúltban szenvedett a miokardiális infarktus vagy stroke. A CSF-enoláz, a szérum NSE (γγ típus) és a kreatin-kináz (ßß típus) szintjét arra a következtetésre utaltuk, hogy ez a szívmegállás áldozatainak prognózisának értékelésére utaló jellegű. Más vizsgálatok az NSE mennyiségének prognosztikai értékére összpontosítottak a stroke áldozataiban. Más vizsgálatok az NSE-koncentrációk prognosztikai értékére összpontosítottak a stroke áldozataiban.
Az alfa-enoláz elleni auto-antitestek ritka betegséggel társulnak, amely a Hashimoto encephalopathia.
Fluorid gátlás
A fluorid a 2-PG szubsztrát enolázhoz való kötődésének jól ismert versenytársa. A fluor egy magnéziummal és foszfáttal képzett komplex része, amely a 2-PG helyett az enoláz aktív helyéhez kötődik. Ily módon a fluoriddal dúsított víz elfogyasztása olyan szintre juttatja a fluoridot, amely gátolja az enoláz baktériumok aktivitását a szájban anélkül, hogy károsítaná a személy egészségét. A baktériumok glikolitikus útjának megzavarása - és ezáltal annak normális metabolikus funkciója - megakadályozza a fogszuvasodás kialakulását.
Megjegyzések és hivatkozások
- (a) Todd Larsen, Joseph E. Wedekind, Ivan Rayment és George H. Reed , " A karboxilát Az oxigén szubsztrát Bridges a magnéziumion-aktív helyén enoláz: az enzim szerkezetét, Élesztő komplexbe a egyensúlyi keveréke 2 -Foszfoglicerát és foszfoenol-piruvát 1,8 Å felbontással ” , Biochemistry , vol. 35, n o 14, 1996. április 9, P. 4349-4358 ( PMID 8605183 , DOI 10.1021 / bi952859c , olvassa el online )
- Az itt feltüntetett tömeg és maradékok száma megegyezik a gén transzlációjából származó fehérje prekurzor értékével, a poszttranszlációs módosítások előtt , és jelentősen eltérhet a a funkcionális fehérje megfelelő értékei .
- (en) Pancholi V, „ Multifunkcionális α-enoláz: szerepe a betegségekben ” , Cell Mol Life Sci. , vol. 58, n o 7,2001. június, P. 902–20 ( PMID 11497239 , DOI 10.1007 / PL00000910 , online olvasás )
- (en) Hoorn RK, Flickweert JP, Staal GE, „ Humán eritrociták enolázának tisztítása és tulajdonságai ” , Int J Biochem , vol. 5, n os 11-12,1974, P. 845–52 ( DOI 10.1016 / 0020-711X (74) 90119-0 )
- (de) Lohman K & Meyerhof O (1934), Über die enzymatische umwandlung von phosphoglyzerinsäure in brenztraubensäure und phosphorsäure ( A foszfo-glicerinsav enzimatikus átalakulása piruvos- és foszforsavakká ). Biochem Z 273, 60–72.
- (en) Peshavaria M, IN nap, „ Az emberi izom-specifikus enoláz gén (ENO3) molekuláris szerkezete ” , Biochem J. , vol. 275 (Pt 2), n o Pt 2,1991. április, P. 427–33 ( PMID 1840492 , PMCID 1150071 )
- (in) Dinovo EC Boyer PD, " Az enoláz reakciómechanizmus izotópos próbái " , J Biol Chem , Vol. 240,1971, P. 4586–93
- (in) Poyner RR Laughlin LT, Sowa GA, GH Reed, " Sav / bázis katalizátorok azonosítása felé az enoláz aktív helyén: a K345A, E168Q és E211Q variánsok tulajdonságainak összehasonlítása " , Biochemistry , vol. 35, n o 5,1996. február, P. 1692–9 ( PMID 8634301 , DOI 10.1021 / bi952186y )
- (in) Reed GH Poyner RR Larsen TM, I Wedekind, Rayment I, " Az enoláz strukturális és mechanisztikus vizsgálata " , Curr Opin Struct Biol. , vol. 6, n o 6,1996 december, P. 736–43 ( PMID 8994873 , DOI 10.1016 / S0959-440X (96) 80002-9 , online olvasás )
- (a) Wedekind JE, Reed GH Rayment I, " Az oktaéderes koordináció a nagy affinitású fém helyen en enoláz: krisztallográfiai elemzése MgII-enzim komplex élesztőgomba-1,9 Å felbontású " , Biochemistry , Vol. 34, n o 13,1995. április, P. 4325–30 ( PMID 7703246 , DOI 10.1021 / bi00013a022 )
- (a) Wedekind I., Poyner RR Reed GH Rayment I, " kelátkötésének a szerin 39 Mg 2+ reteszeli egy kapu az aktív helyén az enoláz: szerkezete a bisz (Mg2 +) komplex élesztő enoláz és a közbenső analóg foszfono-acetohidroxamát 2,1-Å felbontással ” , Biochemistry , vol. 33, n o 31,1994. augusztus, P. 9333–42 ( PMID 8049235 , DOI 10.1021 / bi00197a038 )
- (a) Larsen TM Wedekind I, Rayment I, Reed GH " A karboxilát oxigén a szubsztrát áthidalja a magnézium-ion aktív honlapján enoláz: szerkezete az élesztő enzim komplexet a egyensúlyi keveréke 2-foszfoglicerát és foszfoenolpiruvát 1,8 Å felbontás ” , Biokémia , vol. 35, n o 14,1996. április, P. 4349–58 ( PMID 8605183 , DOI 10.1021 / bi952859c )
- (en) Duquerroy S, C Camus, J Janin, " X-ray, szerkezetük és katalitikus mechanizmust a homár enoláz " , Biochemistry , Vol. 34, n o 39,1995. október, P. 12513–23 ( PMID 7547999 , DOI 10.1021 / bi00039a005 )
- (a) Royds JA, Timperley WR, Taylor CB, „ szintje enoláz és más enzimek a liquor van bizonyíték patológiai változásokra ” , J. Neurol Neurosurg Psychiatr. , vol. 44, n o 12,1981. december, P. 1129–35 ( PMID 7334408 , PMCID 491233 , DOI 10.1136 / jnnp.44.12.1129 )
- (en) Roine RO, Somer H Kaste M, L Viinikka, Karonen SL, " Neurológiai utáni eredmény-out-of-kórház szívmegállás. Jóslás cerebrospinalis folyadék enzim analízissel ” , Arch Neurol. , vol. 46, n o 7,1989. július, P. 753–6 ( PMID 2742544 )
- (en) Hay E, Royds JA, Davies Jones GA, Lewtas NA, Timperley WR, Taylor CB, " agy-gerincvelő folyadék enoláz stroke " , J. Neurol Neurosurg Psychiatr. , vol. 47, n o 7,1984. július, P. 724–9 ( PMID 6747647 , PMCID 1027902 , DOI 10.1136 / jnnp.47.7.724 )
- (en) Fujii A, Yoneda M, Ito T, Yamamura O, Satomi S, Higa H, Kimura A., Suzuki M, Yamashita M, Yuasa T, Suzuki H, Kuriyama H, " elleni autoantitestek az amino-terminális alfa-enoláz hasznos diagnosztikai marker a Hashimoto-féle encephalopathiában ” , J. Neuroimmunol. , vol. 162, n csont 1-2,2005. május, P. 130–6 ( PMID 15833368 , DOI 10.1016 / j.jneuroim.2005.02.004 )
- (in) Centers for Disease Control, " populációk részesülő send optimálisan fluorid közüzemi ivóvíz Single-Egyesült Államok, 2000 " , MMWR Morb Mortal Wkly Rep. , vol. 51, n o 7,2002. február, P. 144–7 ( PMID 11905481 )
- (in) Hüther FJ, Psarros N, H Duschner, " Streptococcus rattus FA-1-ből származó enoláz izolálása, jellemzése és gátlásának kinetikája " , Infect Immun. , vol. 58, n o 4,1 st április 1990, P. 1043–7 ( PMID 2318530 , PMCID 258580 , online olvasás )
- (fr) Ez a cikk részben vagy egészben venni a Wikipedia cikket angolul című „ enolázt ” ( lásd a szerzők listáját ) .