Halohidrin
A szerves kémia, halogénhidrinek vagy halogénalkoholok egy család szerves vegyületek halogénezett származó alkoholok . Az IUPAC meghatározása szerint ezek olyan alkoholok , amelyek telített szénatomon halogénatommal vannak helyettesítve , amelyek egyébként csak hidrogénatomokat vagy szénhidrogéncsoportokat tartalmaznak . A „halohidrin” kifejezés gyakran csak a β-halogénalkoholokra korlátozódik , vagyis azokra a vegyületekre, amelyekben a hidroxilcsoportot és a halogénatomot a szomszédos szénatomok ( vicinális ) hordozzák . Mivel a meghatározás csak telített vegyületekre vonatkozik, kizárja például az aromás vegyületeket, például a 2-klór-fenolt . A halohidrinek halogénatomjuk jellege szerint alkategóriákba sorolhatók, illetve fluorhidrinekké, klórhidrinekké, brómhidrinekké és jódhidrinekké.
Bizonyos klórhidrineket, például 1-klór-2-propanolt (propilén-klórhidrint) évente több megatonne mennyiségben állítanak elő a polimerek prekurzoraként .
Szintézis
Alkénekből
A halhidrineket általában úgy állítják elő, hogy egy alként dihalogénnel kezelnek víz jelenlétében. Ez a reakció egy elektrofil addíció , hasonlóan a dihalogenizációs reakcióhoz (en) , amely anti-addícióként megy végbe . Például az etilén etilén-klórhidrinné ( 2-klór-etanol ) való átalakításának egyenlete :
H 2 C = CH 2 + Cl 2 + H 2 O → H 2 (OH) C-CH 2 Cl + HCIBrómozáshoz N- bróm-szukcinimidet (NBS) használnak reagensként , nem dibroma helyett , mivel ez kevesebb mellékterméket eredményez .

Epoxidokból
Halogénhidrinek is elő, hogy egy epoxidot egy hidrogén-halogeniddel , vagy egy fém-halogenid .
2-klórsavaktól
A 2-klór-karbonsavakat lítium-tetrahidro -alumináttal redukálhatjuk 2-klór -alkoholokká . Ezeket a savakat különféle módon lehet előállítani, például Hell-Volhard-Zelinski halogénezéssel . A 2-klór- propionsavat (in) propanoil-klorid klórozásával , majd az így kapott 2-klór- propanoil-klorid hidrolízisével állítják elő. Az enantiomer tiszta ( S ) -2-klór- propánsav és különböző rokon vegyületek állíthatók elő aminosavakból diazotálás útján .
Reakciók
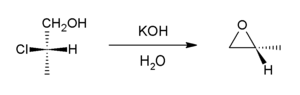
Jelenlétében egy bázis , halogénhidrinek alávetni intramolekuláris S N 2 alkotnak epoxidok . Ipari szempontból kalcium-hidroxidot használnak erre, de a laboratóriumban általában előnyös kálium-hidroxidot használni .
Ez a reakció fordítottja az epoxidokból képződő halohidrineknek, és Williamson szintézisének egyik változatának tekinthető . A propilén-oxid nagy részét ezzel a módszerrel állítják elő :
valamint az epiklórhidrin . Másrészt, ha egy időben az etilén-oxidot 2-klór-etanolból állították elő , amelyet erre a célra nagy mennyiségben állítottak elő, az etilén-oxid ma már közvetlenül az etilén oxidációjával jön létre .
Az ilyen reakciók alapja a bonyolultabb folyamatoknak is, például az epoxidképződés kulcsfontosságú lépés a Darzens-reakcióban .
Ez a reakció a természetben, baktériumokban is létezik , ahol a halohidrin-dehalogenáz (en) katalizálja .
Halogénezett halohidrinek
Az olyan vegyületek, mint a 2,2,2-triklór-etanol , amelyek a hidroxilcsoport szomszédságában több drágakő- halogént tartalmaznak, halogén- hidrineknek tekinthetők (bár nem felelnek meg szigorúan az IUPAC definíciójának ), mivel kémiai tulajdonságaik hasonlóak, különösen intramolekuláris ciklizációnak vethető alá. dihaloepoxicsoportokat alkotnak. Ezek a fajok rendkívül reaktívak és hasznosak a szintézisben, ezek a Jocic-reakció (en) , a Bargellini-reakció (en) és a Corey-Link-reakció (en) alapját képezik .
Biztonság
Mint minden funkcionális csoportnál , a halohidrinek veszélyeit is nehéz általánosítani, mivel ezek szinte korlátlan számú vegyületsorozat részét képezhetik, amelyek mindegyikének más a farmakológiája. Általában az alacsony molekulatömegű egyszerű vegyületek gyakran mérgezőek és rákkeltők (például 2-klór-etanol , a 3-MCPD (in) ), hogy alkilező szerek . Ez a reaktivitás kihasználható például a rákellenes mitobronitol ( fr ) gyógyszerben . Számos szintetikus kortikoszteroid létezik fluorhidrin mintázatú ( triamcinolon , dexametazon ).
Hibák
Potenciálisan zavaros elnevezésük ellenére sem az epiklórhidrin (2- (klór-metil) -oxirán), sem a kénsav-klórhidrin ( klór- kénsav) nem klór- hidrin .
Megjegyzések és hivatkozások
- ( fr ) Ez a cikk részben vagy egészben az angol Wikipedia " Halohidrin " című cikkéből származik ( lásd a szerzők felsorolását ) .
- (in) " halogénhidrinek " Compendium of Chemical Terminology [ " Gold Book "], IUPAC 1997 javított verzió online (2006-), 2 th ed.
- William Reusch, „ addíciós reakciók alkének ” [ archív2012. december 14] , a szerves kémia virtuális tankönyvéről
- Carlo Bonini és Giuliana Righi , „ Halohidrinek regio- és kemoszelektív szintézise az oxiránok fémhalogenidekkel történő hasításával ”, szintézis , vol. 1994 N o 03,1994, P. 225–238 ( DOI 10.1055 / s-1994-25445 )
- Bernhardt Koppenhoefer és Volker Schurig , „ (S) -2-klór-alkánsavak nagy enantiomer tisztaságú (S) -2-aminosavakból: (S) -2-klór-propánsav ”, Organic Syntheses , vol. 66,1988, P. 151 ( DOI 10.15227 / orgsyn.066.0151 )
- Dietmar Kahlich, Uwe Wiechern, Jörg Lindner „Propilén-oxid” Ullmann ipari kémiai enciklopédiájában, Wiley-VCH, Weinheim, 2002. DOI : 10.1002 / 14356007.a22_239 Cikk online közzététele: 2000. június 15
- Ullmann ipari kémiai enciklopédiája , Weinheim, Wiley-VCH,2005( DOI 10.1002 / 14356007.a06_565.pub2 )
- TS Snowden , „ A drágakő-diklór- epoxid köztitermékek legújabb alkalmazásai szintézisben ”, Arkivoc , vol. 2012 N o 22012. február 28, P. 24–40 ( DOI 10.3998 / ark.5550190.0013.204 )