Atomi orbitális
A kvantummechanikában az atompálya olyan matematikai függvény, amely leírja egy elektron vagy egy elektronpár hullám viselkedését az atomban . Ez a függvény megadja az atom elektronjának jelenlétének valószínűségét az atom adott régiójában. Ezért gyakran izoszurfétumok segítségével ábrázolják , amelyek körülhatárolják azt a régiót, amelyen belül az elektron jelenlétének valószínűsége nagyobb, mint egy adott küszöb, például 90%. Az ilyen régiók nem feltétlenül kapcsolódnak egymáshoz, és gömbharmóniákból adódóan összetett alakokat jeleníthetnek meg .
Minden egyes atompályát egy egyedi kvantumszámú triplett ( n , ℓ , m ℓ ) határoz meg, amelyek az elektron energiáját , szögmomentumát és ennek a szögmomentumnak az adott tengelyre vetített vetületét képviselik. Mindegyik pályák által elfoglalható legfeljebb két elektron különböznek egymástól a mágneses kvantumszám spin m s . Beszélünk s , p , d és f pályák jelölésére pályák által meghatározott egy perdület ℓ , értéke 0, 1, 2 és 3 volt. Ezek a nevek származnak a régi nevét a spektrális vonalak az alkálifémek le, mint éles , fő , diffúz és finom vagy alapvető ; a pályák megfelelő ℓ > 3 Ezután elemzi ABC g , h , i , k , stb , elhagyva a j betűt, mert néhány nyelv nem különbözteti meg az i betűtől.
Az atompályák az elektronfelhő elemi alkotóelemei, ami lehetővé teszi az elektronok anyagban való viselkedésének modellezését. Ebben a modellben, az elektron felhő egy több-elektron atom lehet közelíteni, mint egy elektron konfiguráció képezünk a termékből több hydrogenoid pályák . A szerkezet a periódusos rendszer elemeinek a blokkok tartalmazó, az egyes időszakban , összesen 2, 6, 10 vagy 14 elemet , egy közvetlen következménye a maximális elektronok száma, amelyek elfoglalják atomi pályák s , p , d és f .
Az elektron tulajdonságai
Kvantum jellegű
A kvantummechanika és olyan kísérleti megfigyelések fejlesztése, mint például egy elektronnyaláb diffrakciója Young résein keresztül, megalapozta a hullám-részecske kettősséget az elemi részecskék leírására . Így elektronok nem keringenek az atommagok a meghatározott kering , mint bolygó körül Sun csinálni . Valójában nem írhatók le olyan kis szilárd gömbökként, amelyeket a mag körüli helyzet és sebesség határoz meg. Inkább állóhullámoknak kell tekinteni őket, amelyek olyan térfogatot foglalnak el, amelyen belül meghatározták a kvantumtulajdonságokat, és képesek kölcsönhatásba lépni más részecskékkel.
- Corpuscularis jelleg :
- csak egy atomban lehet egész számú elektron;
- energiacsere egy beeső részecske, például egy foton , és egy atom elektronjai között mindig csak egy elektront érint, az összes többi kizárásával, annak ellenére, hogy több elektronnak nem nulla a valószínűsége, hogy egyidejűleg az a hely, ahol egyikük kölcsönhatásba lép ezzel a fotonnal;
- egy elektron meghatározott és állandó elektromos töltéssel rendelkezik , és olyan spinet mutat be, amelynek vetülete a kvantálási tengelyen egyenlő lehet +12(spin up ), vagy -12(pörögj le ).
- Hullám természet :
- az elektron minimális energiája megfelel a húr rezgésének alapvető frekvenciájához hasonlítható állapotnak , amelyet alapállapotnak nevezünk ; az elektron magasabb energiaszintjei ennek az alapvető frekvenciának a harmonikusai ;
- az elektronok soha nem helyezkednek el a tér egy pontos pontján, hanem olyan térfogatban nyilvánulnak meg, amelynek belsejében az adott pontban való kölcsönhatás valószínűségét a hullámfüggvényük határozza meg .
Matematikai kifejezés
Az atompályák pontosabban meghatározhatók a kvantummechanika matematikai formalizmusával . Ebben az összefüggésben, a kvantum állapotát Egy elektron a hullám funkció Ψ , amely megfelel a sajátérték egyenlet a Hamilton- H , más néven „idő független Schrödinger egyenlet” , vagy akár „egyenlete Államok. Helyhez kötött„: H Ψ = E Ψ , ahol E a hullámfüggvényhez kapcsolódó energia. A többelektronikus atom elektronikus konfigurációját a monoelektronikus funkciók termékeinek lineáris kombinációja ( konfigurációs interakció , bázisok ) közelítik meg ( Slater-determinánsok ). Ezeknek a monoelektronikus funkcióknak a térbeli komponense az atompálya, és a spin- komponens figyelembevétele meghatározza a spinorbitákat .
Az atompálya az elektron jelenlétének valószínűségi amplitúdója egy izolált atom magja körül . Ez a valószínűség sűrűsége függ a téren a modulus a hullám funkció Ψ . Ez határozza meg a Schrödinger-egyenlet segítségével orbitális közelítése , amely magában foglalja a figyelmen kívül hagyva a korrelációk közötti elektronok, és kiszámítjuk az elektronikus konfiguráció egy atom termékeiként monoelectronic hullám funkciók. Ez azonban közelítő érték, mivel a különböző elektronok eloszlása a pályájukon tulajdonképpen összefüggésben van, a londoni erők ennek a korrelációnak a megnyilvánulásai.
Pályák számítása
Atomic pályák lehetnek monoelectron pályák, amelyek egzakt megoldásait a Schrödinger-egyenlet egy hidrogénatom (azaz egyetlen elektron) atom . Alapul szolgálhatnak az atom vagy a molekula különböző elektronjait leíró hullámfüggvények kiszámításához is. A választott koordinátarendszer általában, hogy a gömbi koordináták (r, θ, φ) a atomok és derékszögű koordinátái (x, y, z) a többatomos molekulák. A gömbkoordináták előnye, hogy egy pálya hullámfüggvénye három függvény eredménye, amelyek mindegyike a három koordináta egyikétől függ: ψ (r, θ, φ) = R (r) Θ (θ) Φ (φ) .
Az R (r) sugárfüggvény általában három általánosan használt matematikai forma segítségével modellezhető:
- A hidrogenoid atompályák a Schrödinger-egyenlet pontos megoldásaiból származnak egy elektronra és egy atommagra. A részét a funkciót, amely attól függ, hogy a sugárirányú távolság sugárirányú csomópontok és mentén csökken e - egy R , a , hogy egy állandó.
- A Slater-típusú pálya ( STO ) egy olyan pálya alakja, amelyen nincsenek radiális csomópontok, de az r mentén csökken, mint egy hidrogénoid pálya.
- A Gauss-pályán ( GTO ) nincsenek radiális csomópontok, és az e - a r 2 mentén csökken .
A hidrogenoid pályákat oktatási eszközökben használják, de elsősorban a Slater típusú pályákat használják atomok és diatomiás molekulák modellezésére a digitális kémia területén . A három vagy több atomot tartalmazó többatomú molekulákat általában Gauss-pályák segítségével modellezik, amelyek kevésbé pontosak, mint a Slater-pályák, de amelyek nagy számban történő kombinációja lehetővé teszi a hidrogénoid pályák pontosságának megközelítését.
A szögletes faktor Θ (θ) Φ (φ) generál funkciókat, amelyek valós lineáris kombinációi a szférikus harmonikusok Ym
ℓ(θ, φ) , ahol ℓ és m az azimutális kvantumszám és a mágneses kvantumszám .
Hidrogénatom pályái
Pályák vannak számolva komplex számok úgy, hogy beszélünk komplex pályák , de a leggyakrabban használ lineáris kombinációi a szférikus harmonikus megválasztani, hogy a képzetes részek kioltják egymást: a pályák így lett a valós számok , és beszélünk valódi pályák .
Összetett pályák
Mindegyik atomi határozza meg triplett a kvantum számok ( N , ℓ , m ℓ ) , és tartalmazhat legfeljebb két elektron egyes különböző saját mágneses spin-kvantum száma , amely csak felfelé vagy lefelé ; a Pauli-kizárási elv valójában tiltja, hogy ugyanazon atom két elektronja ugyanazt a kvantumállapotot használja :
- A főkvantumszám n egy nem nulla természetes szám : n ≥ 1 ;
- A másodlagos kvantum számát (vagy azimutális kvantumszám) ℓ egy pozitív vagy nulla egész szám ellenőrzése 0 ≤ ℓ ≤ n - 1 , és kapcsolódik a kvantálás a perdület a orbitális;
- A mágneses kvantumszám m ℓ jelentése egész szám, kielégíti - ℓ ≤ m ℓ ≤ ℓ , és kapcsolódnak az kvantálás a vetülete a perdület egy adott tengelyen;
- A mágneses kvantum száma centrifugálás m s jelentése megegyezik a -12vagy +12ahol a megfelelő elektronokat általában a ↓ és ↑ szimbólumok képviselik; ez az elektron belső tulajdonsága, független a másik három kvantumszámtól.
A főkvantumszám n határozza meg a elektronikus héj , míg a azimutális kvantumszám ℓ típusát határozza meg elektronikus alburok az elektron. Attól függően, hogy ℓ jelentése 0, 1, 2, 3, 4, 5, 6 vagy több, a típusú ezeknek alrétegből jelöli a leveleket s , p , d , f , g , h , i , stb
Magukat az alrétegeket úgy jelöljük, hogy az n kvantumszámot összekapcsoljuk a ℓ kvantumszámot képviselő betűvel ; így az ( n , ℓ ) = (2, 1) -nek megfelelő alréteget 2p-vel jelöljük.
Az atomok elektronikus konfigurációját úgy jegyezzük meg, hogy az elektronikus alrétegeket hatványként felsoroljuk az elektronok számával ezen az alrétegen. Konstrukció szerint az alrétegek száma egy elektronikus rétegre megegyezik n-vel , míg az s , p , d , f elektronikus alrétegre eső pályák száma 1, 3, 5, 7 stb. Ezen pályák mindegyike legfeljebb két elektronot tartalmazhat, az s , p , d , f alhéj típusonkénti maximális elektronszám 2, 6, 10, 14.
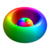
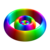
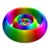
Táblázat az első komplex pályák egy hidrogén atom| Kvantumszámok | Alapozás | Mágneses kvantumszám m ℓ | |||||||
|---|---|---|---|---|---|---|---|---|---|
| Fő | Azimuthal | -3 | -2 | -1 | 0 | 1 | 2 | 3 | |
| n = 1 | ℓ = 0 | 1 s |

|
||||||
| n = 2 | ℓ = 0 | 2 mp |

|
||||||
| ℓ = 1 | 2 p |

|

|

|
|||||
| n = 3 | ℓ = 0 | 3 mp |

|
||||||
| ℓ = 1 | 3 p |

|

|
|
|||||
| ℓ = 2 | 3 d |

|

|

|

|

|
|||
| n = 4 | ℓ = 0 | 4 mp |

|
||||||
| ℓ = 1 | 4 p |

|

|

|
|||||
| ℓ = 2 | 4 d |

|

|

|

|

|
|||
| ℓ = 3 | 4 f |

|

|

|

|

|

|

|
|
| n = 5 | ℓ = 0 | 5 s |

|
||||||
| ℓ = 1 | 5 p |

|

|

|
|||||
| ℓ = 2 | 5 d |

|

|

|

|
|
|||
| n = 6 | ℓ = 0 | 6 s |

|
||||||
| ℓ = 1 | 6. o |

|

|

|
|||||
| ℓ = 2 | 6 d |
|

|

|

|

|
|||
A fent bemutatott felületek színei a hullámfüggvény valós és képzeletbeli részének jelét jelzik (ezek a színek tetszőlegesek és nem tükröznek egyezményt):
| Hullám funkció | Igazi rész | Képzeletbeli rész |
|---|---|---|
| Pozitív érték | Kék | Piros |
| Negatív érték | Sárga | Zöld |
Ezek a számítások jelenti a választás egy kiváltságos tengely - például a z tengelyre a derékszögű koordináta-rendszerben - és kiváltságos irányt ezen a tengelyen: ez az, ami lehetővé teszi, hogy meghatározza a jel a mágneses kvantumszám m ℓ . Ez a modell ezért hasznosak olyan rendszerekkel, amelyek osztják ezt a szimmetriát, mint abban az esetben a Stern és Gerlach kísérlet , ahol az ezüst atomok vannak kitéve egy függőleges, nem-egyenletes mágneses mezőt .
Valódi pályák
A kristályos szilárd anyagban elhelyezkedő atomnak több preferenciális tengelye van, de ezeken a tengelyeken nincs preferenciális orientáció. Ilyen körülmények között ahelyett, hogy egy ilyen atom atompályáit sugárfüggvényekből és egyetlen gömbharmóniából építenénk , általában a gömb harmonikusainak lineáris kombinációit használjuk, amelyeket úgy választunk meg, hogy képzeletbeli részük eltűnjön. Ami valódi harmonikusokat ad . Ezeket a tényleges pályákat használják általában az atomi pályák vizualizálására.
Például a valódi hidrogén- pályákon n és ℓ jelentése azonos a komplex párjukon , de m ℓ már nem érvényes kvantumszám , bár modulusa igen . A tényleges hidrogén p pályákat például a következők adják meg:
ahol , és .
A p x és p y pályák egyenletei a gömb harmonikusokra választott fáziskonvenciótól függenek. Az előző egyenletek azt feltételezik, hogy a gömb harmonikusokat Y határozza megm
ℓ(θ, φ) = N e i m φ Pm
ℓ(cosθ) . Néha azonban egy (–1) m fázisfaktort is beleszámítanak, amelynek hatására a p x pálya megfelela harmonikus különbségnek, a p y pályapedig a harmonikusok összegének.
| Kvantumszámok | Alapozás | Modul | m ℓ | a mágneses kvantumszám | |||||||
|---|---|---|---|---|---|---|---|---|---|
| Fő | Azimuthal | 0 | 1 | 2 | 3 | ||||
| n = 1 | ℓ = 0 | 1 s |
 1s |
||||||
| n = 2 | ℓ = 0 | 2 mp |
 2s |
||||||
| ℓ = 1 | 2 p |
 2p z |
 2p x |
 2p y |
|||||
| n = 3 | ℓ = 0 | 3 mp |
 3s |
||||||
| ℓ = 1 | 3 p |
 3p z |
 3p x |
 3p y |
|||||
| ℓ = 2 | 3 d |
 3d z 2 |
 3d xz |
 3d yz |
 3d xy |
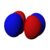 3d x 2 –y 2 |
|||
| n = 4 | ℓ = 0 | 4 mp |
 4s |
||||||
| ℓ = 1 | 4 p |
 4p z |
 4p x |
 4p y |
|||||
| ℓ = 2 | 4 d |
 4d z 2 |
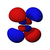 4d xz |
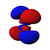 4d yz |
 4d xy |
 4d x 2 –y 2 |
|||
| ℓ = 3 | 4 f |
 4f z 3 |
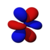 4f xz 2 |
 4f yz 2 |
 4f xyz |
 4f z (x 2 –y 2 ) |
 4f x (x 2 –3y 2 ) |
 4f y (3x 2 –y 2 ) |
|
| n = 5 | ℓ = 0 | 5 s |
 5s |
||||||
| ℓ = 1 | 5 p |
 5p z |
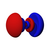 5p x |
 5p y |
|||||
| ℓ = 2 | 5 d |
 5d z 2 |
 5d xz |
 5d yz |
 5d xy |
 5d x 2 –y 2 |
|||
| n = 6 | ℓ = 0 | 6 s |
 6s |
||||||
| ℓ = 1 | 6. o |
 6p z |
 6p x |
 6p y |
|||||
| ℓ = 2 | 6 d |
 6d z 2 |
 6d xz |
 6d yz |
 6d xy |
 6d x 2 –y 2 |
|||
| n = 7 | ℓ = 0 | 7 mp |
 7s |
||||||
A fenti ábrán a szín jelzi a hullámfüggvény előjelét, amely vörösben pozitív, kékben negatív.
Az atompályák geometriája
A pályák grafikus ábrázolásának célja, hogy bemutassa azokat a térrészeket, amelyeket egy atompálya elektronjai valószínűleg elfoglalnak. Ezek a modellek nem reprezentálhatják azt a teljes régiót, ahol az elektron valószínűleg elhelyezkedni fog, mert az elektron kvantumtulajdonságai miatt nem nulla a valószínűsége annak, hogy az atom körül szinte az elektrontérben bárhol megtalálható legyen. Ezért ezek az ábrázolások olyan izfelületekből állnak, amelyeken a valószínűségi sűrűség | ψ (r, θ, φ) | A 2. ábra állandó és ezen belül az elektron jelenlétének valószínűsége megegyezik egy adott értékkel, például 90% -kal. Bár | ψ | A 2 soha nem negatív , általában a hullámfüggvény the jelét jelezzük (r, θ, φ) .
Lehetséges a ψ függvény és annak fázisa is , nem pedig a ψ 2, amely jelzi a valószínűség sűrűségét, de nincs fázisa. A | . Ábrázolásai ψ (r, θ, φ) | 2 általában kevésbé gömbölyű és keskenyebb lebenyű, mint a ψ (r, θ, those ) , de a két ábrázolás ugyanolyan lebenyekkel rendelkezik, azonos térbeli elrendezéssel, és egymástól felismerhetők.
A kvantumszámok értelmezése
Általánosságban elmondható, hogy az n fő kvantumszám meghatározza a pálya nagyságát és energiáját egy adott atommag esetében : minél több n nő, annál inkább nő a pálya mérete. Több kémiai elem pályájának összehasonlításakor azonban minél magasabb a Z atomszám , annál több atompálya összehúzódik, mert az elektromos töltés teljes magja is növekszik Z-vel . Ennek eredményeként az atomok mérete az elektronikus rétegek felhalmozódása ellenére viszonylag állandó marad .
Mégis általában a azimutális kvantumszám ℓ alakját meghatározó az orbitális, míg a mágneses kvantumszám m ℓ határozza meg a térbeli orientáció. Az m ℓ szám azonban meghatározza néhány összetett pálya alakját is . Az adott párnak ( n , ℓ ) megfelelő pályák halmaza a lehető legszimmetrikusabban tölti be a növekvő számú lebenyt és csomópontot.
S pályák
A s pályákat , amelyeket ℓ = 0 jelöl , gömbök képviselnek. Az n = 1 , a valószínűség-sűrűség nagyobb a központban, és csökken kifelé, de az n = 2 vagy több, a valószínűség-sűrűség belül minden s orbitális formák egy radiális hullám szerkezet, amelyben alternatív koncentrikus rétegek nagy valószínűséggel és kisebb valószínűséggel.
Az egyedüli s pályák mutatnak be egy anticsomót, vagyis egy olyan régiót, ahol a hullámfüggvénynek nagy a modulusa, a mag közepén. A p , d , f , és az azt követő pályák van perdület és elkerülni a sejtmagba, ahol bemutatják egy csomót.
P, d és f pályák
A három p pályák az n = 2 alakúak két ellipsoids megosztása egy pont érintési szintjén az atommag . Ez az alak néha a súlyzók . Ezek orientált ortogonálisán egymáshoz képest más függvényében azok mágneses kvantumszám m ℓ .
Négy öt d pályák az n = 3 hasonló formák, egyenként négy körte alakú lebeny, ezek a lebenyek hogy ortogonálisán érintő kettesével, középpontjai a négy lebeny hogy egy síkban . Ezek közül a d xy , d yz és d xz nevű pályák közül három az xy , yz és xz síkra igazodik - a lebeny a koordinátatengely három párja között helyezkedik el - míg a negyedik, d x 2 - y 2 , magához az x és y tengelyhez igazodik .
A d z 2 nevű , m ℓ = 0-nak megfelelő ötödik d pályát három régió alkotja, ahol a valószínűségi sűrűség nagy: két körte alakú régió a mag mindkét oldalán a z tengely mentén, és egy tórusz a mag körül az xy síkban .
-
Orbita d xy
-
Orbital d yz
-
Orbita d xz
-
Orbita d x 2 - y 2
-
D z 2. pálya
Hét f pálya van, és összetettebb formájúak, mint d pályák .
A hidrogénatomok atompályáinak alakja gömb harmonikusokból származik . Ezek az alakzatok nem egyediek, és sok lineáris kombináció érvényes, például átalakulás köbös harmonikákká (in) . Létre lehet hozni olyan függvénykészleteket is, amelyek mindegyike azonos alakú d pályákat állít elő , például p pályák .
Nem szabad megfeledkezni arról, hogy ezek a pályák, külön-külön, a hidrogénatomok modelljeinek részeként, egyidejűleg léteznek a valós atomokban.
Analógia a membrán rezgésével
Két dimenzióban lehet ábrázolni az atompályák különböző háromdimenziós alakjainak jelentését egy kör alakú membrán, például egy dob bőrének rezgési módjaival . Ebben az ábrázolásban a membrán közepétől való távolság egyenértékű az elektron és az atommag távolságával , és a membrán egyensúlyi síkjától való eltérés nagysága képviseli az elektron jelenlétének sűrűségét az atomban. . Ez a hasonlat nem tökéletes, különösen azért, mert egy olyan fizikai membrán feszültsége, mint a dob bőre, az kereszti a hullámokat, amelyek áthaladnak rajta, de az atompályák számos kvalitatív tulajdonságával jár, például az a tény, hogy csak az s pályák középpontjában anti-csomópont (maximális amplitúdó), míg a többieknél ezen a helyen van egy csomópont (nulla amplitúdó), vagy a Student rangú pályák lebenyeinek geometriai eloszlásának megjelenítésére:
- A dob bőrének első 9 rezgési módja
-
U 01 mód , analóg az 1-esekkel
-
U 02 mód , analóg a 2-esekkel
-
U 03 mód , analóg a 3-asokkal
-
U 11 mód , analóg a 2p-vel
-
U 12 mód , analóg a 3p-vel
-
U 13 mód , analóg a 4p-vel
-
U 21 mód , analóg a 3d-vel
-
U 22 mód , analóg a 4d-vel
-
U 23 mód , analóg az 5d-vel
Az s és p atompályák hullámfüggvényének valós része , amelyet ugyanúgy ábrázolunk az n és az ain különböző értékeire, így analóg a dobfej különböző rezgési módjaival:
- Valós része a hullámfüggvénye s és p pályák
-
1s orbitális
-
2s orbitális
-
orbitális 3s
-
2p orbitális
-
pálya 3p
-
pálya 4p
Alkalmazások
A atomfizika , spektrális vonalak megfelelnek az elektronikus átmenetek eredő átmenet egyik kvantum állapot a atom egy másik. Ezek az állapotok által meghatározott egy sor kvantum számok általában társított elektronikus konfiguráció , azaz forgalmazásával elektronok a különböző atomi pályák. Így, az elektronikus konfiguráció neon az alapállapotú van 1s 2 2s 2 2p 6 , összefoglalt a kifejezés1S
0.
Atomic pályák kulcsfontosságú fogalom láthatóvá gerjesztő folyamatok az eredete elektronikus átmenetek . Például egy adott átmenetet össze lehet kapcsolni az n = n 1 fő kvantumszám elfoglalt pályájáról az n = n 2 kvantumszám üres pályájára haladó elektron gerjesztésével . Így a hidrogénatomban lévő elektron energiája megegyezik:
,tudjuk következtetni Rydberg-képlet , amely a hullám számot társított elektronikus átmenet egy olyan n = n 1 orbitális egy n = n 2 orbitális egy hydrogenoid atom, ahol λ a hullámhossz , R ∞ a Rydberg állandó , és Z eff az effektív nukleáris töltet (ben) :
Alkalmazva a hidrogén , a képlet kiszámításához használt emissziós vonalak a spektrum a hidrogén :
Nem szabad megfeledkezni arról, hogy az így definiált pályák monoelektronikus hullámfüggvények, amelyek a hidrogénatomokra vonatkoznak . Mivel az atomok általában nem hidrogénatomok, éppen ellenkezőleg, polielektronikusak, így ez a közelítés az atomok elektronikus konfigurációjának modellezésének egyszerűsítésére szolgál, de korlátai lehetnek, különösen a nagy atomok leírására.
Megjegyzések és hivatkozások
- (in) David Griffiths, Bevezetés a Quantum Mechanics , 1995, Prentice Hall, pp. 190–191 . ( ISBN 0-13-124405-1 )
- (en) Ira Levine, (2000). Quantum Chemistry , 5 -én kiadás, 2000, Prentice Hall, pp. 144–145 . ( ISBN 0-13-685512-1 )
- (a) Keith J. Laidler, John H. Meiser, Physical Chemistry , 1982-ben, Benjamin / Cummings, p. 488 . ( ISBN 0-8053-5682-7 )
- (in) Peter Atkins, Julio de Paula, Ronald Friedman, Quanta, Anyag és Változás: A molekuláris megközelítés Fizikai Kémia , 2009, Oxford University Press, p. 106 . ( ISBN 978-0-19-920606-3 )
- Roger Penrose , Az univerzum törvényeinek felfedezése: A matematika és a fizika csodálatos története , 2004.
- (a) Ira Levine, Quantum Chemistry , 7 -én kiadás, Pearson Education, 2014 pp. 141–142 . ( ISBN 0-321-80345-0 )
- (in) Miguel A. Blanco, Mr. Flórez és Mr. Bermejo , " A rotációs mátrixok értékelése valós gömb harmonikusok alapján " , Journal of Molecular Structure: THEOCHEM , vol. 419, n csont 1-3, 1997. december 8, P. 19–27 ( DOI 10.1016 / S0166-1280 (97) 00185-1 , online olvasás )
- (in) Albert Messiás, kvantummechanika: két kötet kötve egy 1999 Mineola, Dover, New York. ( ISBN 978-0-486-40924-5 )
- Claude Cohen-Tannoudji, Bernard Dui, Franck Laloë, Kvantummechanika , Természettudományi Gyűjtemény, Herman, Párizs, 1973. Bibcode : 1973mequ.book ..... C
- (a) Richard E. Powell , " Az öt d pályák egyenértékű " , Journal of Chemical Education , vol. 45, n o 1, 1968. január, P. 45 ( DOI 10.1021 / ed045p45 , Bibcode 1968JChEd..45 ... 45P , online olvasás )
- (in) George E. Kimball , " Directed Valencia " , The Journal of Chemical Physics , vol. 8, n o 2 1940. február, P. 188-198 ( DOI 10.1063 / 1.1750628 , Bibcode 1940JChPh ... 8..188K , online olvasás )
Lásd is
Kapcsolódó cikkek
- Schrödinger modellje
- Hidrogénatom
- Gömb alakú harmonikus
- Molekuláris pálya







