Aminoacil-tRNS-szintetáz
A aminoacil-tRNS-szintetázok (aaRS rövidítése) alkotnak család ligázok ( EK ), amelyek katalizálják az észterezési a proteinogén aminosavak (rövidítve aa) a 3 „végén a transzfer RNS (tRNS rövidítése). Ez a lépés lényeges a fordítást a messenger RNS-ek be fehérjék , aminosavak és így adjuk a végén a tRNS-ek, amelyeket a leírásban a riboszómák a polipeptid-lánc szintetizálandó. Lényeges fehérjék, minden élőlényben megőrződtek .
A legtöbb organizmusban mindegyik proteinogén aminosavhoz tartozik egy aminoacil-tRNS-szintetáz, a szelenocisztein kivételével , amely a transzfer-RNS-hez kapcsolódik egy közvetett, szerinnen áthaladó mechanizmus révén . Ezen enzimek mindegyike felismer egy aminosavat és egy vagy több izo-akceptor tRNS-t. Funkciójuk elengedhetetlen a genetikai kód fordításának hűségéhez , mert ezek garantálják, hogy a tRNS végén így észterezett aminosav megfeleljen a helyes antikodonnak . Ezután a riboszóma szintjén nem hajtanak végre ellenőrzést.
Gépezet
Az amino-acil-tRNS-szintetázok katalizálják a kétlépcsős aminoacilezési reakciót, először aktiválják az aminosavat úgy, hogy ATP-vel amino-acil-adenilátot képeznek, pirofoszfát felszabadulásával. Az így aktivált aminosav kötve marad az enzimhez, és átkerül a tRNS 3'- végén elhelyezkedő adenozin ribóz 2'-OH vagy 3'-OH funkciójába :
A legtöbb aminoacil-tRNS-szintetáz képes e két reakció közül az első végrehajtására tRNS nélkül, de a glutamil-tRNS-szintetáz , a glutaminil-tRNS-szintetáz , az arginil-tRNS-szintetáz és a lizil-tRNS-szintetáz I nem képes erre, ha a tRNS hiányzó. Ezen aminosavak ( glutamát , glutamin , lizin , arginin ) aktivációja tRNS-függő.
Az enzim-nómenklatúra szempontjából az aminoacil-tRNS-szintetázok ligázok és az EC kategóriába . Elérhetők az aminosav jellege szerint, amelyre specifikusak: alanil-tRNS-szintetáz az alaninhoz , a metionil-tRNS-szintetáz a metioninhoz stb.
Az Escherichia coli baktériumban és a Saccharomyces cerevisiae élesztőben ( eukarióta ) valóban 20 aminoacil-tRNS-szintetáz található, mindegyik standard aminosavhoz egy.
Noha ezek a modellorganizmusok rendelkeznek az összes aminoacil-tRNS-szintetázzal, nem minden organizmus rendelkezik. Valójában nem ritka, hogy a glutaminil-tRNS-szintetáz (GlnRS) hiányzik, különösen a baktériumok 90% -ában, és az összes archeában . Kimutatták azt is, hogy a mitokondriumokban szintén hiányzik ez az enzim. Baktériumoknál és archeákban az aszparaginil-tRNS szintetáz szintén hiányozhat. Minden esetben (és mivel a két aminoacil-tRNS, az Asn-tRNS (Asn) és a Gln-tRNS (Gln) szintézise elengedhetetlen ), a szervezetek alternatív utat alkalmaznak, amely két egymást követő enzimatikus lépést foglal magában.
Az aminoacil-tRNS-szintetázok osztályai
Az aminoacil-tRNS-szintetázoknak (aaRS) két osztálya van, az úgynevezett I. és a II. Osztály , nagyon eltérő szerkezeti és funkcionális tulajdonságokkal. Az I. osztályú aminoacil-tRNS-szintetázok észterezik az aminosavat a terminális adenozin tRNS-jének 2'-OH-jához, és az utóbbihoz kötődnek az akceptorkar kisebb hornyán keresztül. Szerkezetük egy párhuzamos béta lapból álló domén köré szerveződik , körülvéve alfa hélixekkel, az úgynevezett Rossmann-hajtásokkal, és sok enzim esetében közösek egy nukleotid- kofaktor ( ATP , NAD + ) alkalmazásával. A II. Osztályú aminoacil-tRNS-szintetázok észterezik az aminosavat a tRNS terminális adenozinjának 3'-OH-jához, és megkötik az akceptorkar fő hornyát. Szerkezetük egy antiparallel béta lap köré épül.
Kivéve a lizil-tRNS-szintetáz , amelyekre jelenleg osztály I vagy osztály II formában , attól függően, hogy a faj , az összes többi aminosav, csak egy formáját enzim szisztematikusan találtuk, nevezetesen osztály I vagy osztály II . Úgy tűnik, hogy az enzimek e két szerkezetileg elkülönülő osztálya egy konvergens evolúciós folyamat eredménye .
Az I. osztályú enzimek közül megtaláljuk a szintetáz leucil-tRNS- eket (ezek), a szintetáz izoleucil-tRNS-t (IleRS), a szintetáz-valil-tRNS-t (ValRS), a szintetáz-ciszteinil-tRNS-t (CysRS), a metionil-tRNS-szintetázt (MetRS), arginil-tRNS-szintetáz (ArgRS), glutamil-tRNS-szintetáz (GluRS), glutaminil-tRNS-szintetáz (GlnRS), I típusú lizil-tRNS-szintetáz (LysRSI), tirozil-tRNS-szintetáz (TyrRS) és triptofanil-tRNS-szintetáz .
A II. Osztályú enzimek közé tartoznak a széril -tRNS-szintetáz (SerRS), a treonil-tRNS-szintetáz (ThrRS), a hisztidil-tRNS-szintetáz (HisRS), a prolil-tRNS-szintetáz (ProRS), a glicil-tRNS-szintetáz (GlyRS), az alanil-tRNS-szintetáz (Alars ) szintetáz-aszpartil-tRNS (AspRS) szintetáz-aszparaginil-tRNS (AsnRS), lizil-tRNS-szintetáz II -es típusú (LysRSII) fenilalanil-tRNS-szintetáz (PheRS) szintetáz-pirrolizil-tRNS (PylRS) és O - foszfoszeril-tRNS .
Szerkezetek
Az aminoacil-tRNS-szintetázok mindkét osztálya többdoménes fehérje. Általában katalitikus doménből és antikodonkötő doménből állnak . Néhányuknak van egy másik RNS- kötő doménje is, amely korrektúra funkciót lát el azzal, hogy a kötést olyan aminosavakkal hasítja le, amelyek nem felelnek meg a transzfer RNS-nek .
Az összes aminoacil-tRNS-szintetáz katalitikus doménje homológ egymással, míg az I. és II . Osztályú enzimek nincsenek kapcsolatban. Azok osztály I. van Rossmann szeres , valamint egy architektúra párhuzamos β szál míg az osztály II van egy különös hajtogatásra antiparallel β szálak .
A α helikális domén kötődik az antikodonja arginyl- , glicil- és ciszteinil-tRNS-szintetázok az úgynevezett DALR domént, mert a konzervált aminosavak ( Asp , Ala , Leu és Arg ), amelyek jellemzőek belőle.
Antikodonkötő domén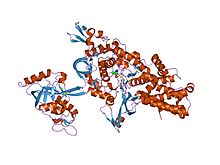 Leucil-tRNS szintetáz a Thermus thermophilus (en) HB27-től ( PDB 1OBC )
Leucil-tRNS szintetáz a Thermus thermophilus (en) HB27-től ( PDB 1OBC )
| Pfam | PF08264 |
|---|---|
| InterPro | IPR013155 |
| SCOP | 1ivs |
| SZUPERCSALÁD | 1ivs |
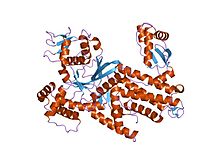 A Thermus thermophilus (en) arginil-tRNS-szintetáza ( PDB 1IQ0 )
A Thermus thermophilus (en) arginil-tRNS-szintetáza ( PDB 1IQ0 )
| Pfam | PF05746 |
|---|---|
| Pfam klán | CL0258 |
| InterPro | IPR008909 |
| SCOP | 1bs2 |
| SZUPERCSALÁD | 1bs2 |
 E. coli ciszteinil-tRNS-szintáz Cys tRNS- sel komplexben ( PDB 1U0B )
E. coli ciszteinil-tRNS-szintáz Cys tRNS- sel komplexben ( PDB 1U0B )
| Pfam | PF09190 |
|---|---|
| Pfam klán | CL0258 |
| InterPro | IPR015273 |
Lektorálás
Bizonyos aminoacil-tRNS-szintetázoknak meg kell különböztetniük a szerkezetileg nagyon közeli aminosavakat, például az izoleucil-tRNS-szintetázokat, amelyeknek meg kell különböztetniük az izoleucint a valintól , amelyek csak metilcsoportonként különböznek egymástól - CH 3. Az affinitásbeli különbség a természetes szubsztrát, az izoleucin és a helytelen szubsztrát, ebben az esetben a valin között nem elegendő ahhoz, hogy megakadályozza, hogy a valin időnként észtereződjön a tRNS Ile-en ezen enzimmel. Ha ez az esemény túl gyakran fordul elő, az izoleucin helyett valin gyakori beépülését eredményezi a riboszómában, és ezért abnormális fehérjék szintéziséhez vezet.
Ezeknek az aminocil-tRNS-szintetázoknak ezért általában mechanikus korrektúrájuk van (angolul: proofreading ), amely lehetővé teszi az enzim ellenőrzését a reakció után a tRNS végéig észterezett aminosav a megfelelő aminosav. Van egy második tRNS-észterezett aminosav-kontroll hely az enzimen. Ha hibát vétettek, a képződött észterkötést hidrolizálják , lehetővé téve a korrekciót. A helytelen aminoacil-tRNS ezen korrekciója egy úgynevezett poszttranszfer mechanizmusnak felel meg , egész egyszerűen azért, mert a téves aminosav átkerült a tRNS-be. Van egy másik típusú korrekció is, az úgynevezett "előtranszfer", amely akkor fordul elő, amikor a helytelen aminosavat aktiválják aminoacil-adeniláttá. Az utóbbit ezután hidrolizálják, mielőtt a tRNS-be transzferálódna.
Ezek enzimatikus mechanizmusok, amelyek lehetővé teszik a genetikai üzenet fordításának hűségének növelését .
Megjegyzések és hivatkozások
- (in) John G. Thomas A. Steitz és Arnez , " kristályszerkezete Három Misacylating mutánsok Escherichia coli glutaminil-tRNS szintetáz komplexált tRNS Gin és ATP " , biokémia , vol. 35, n o 47, 1996. november 26, P. 14725-14733 ( PMID 8942633 , DOI 10.1021 / bi961532o , online olvasás )
- (a) P. Berg és EJ Offengand , „ enzimes mechanizmus összekapcsolása aminosavakat RNS ” , Proc. Natl. Acad. Sci. USA , vol. 44,1958, P. 78–86 ( PMID 16590176 )
- (a) Daniel Kern, Andrew Dietrich, Franco Fasiolo Michel Renaud, Richard Giegé és Jean-Pierre Ebel , „ Az élesztő amino-acil-tRNS-szintetázok: Módszertan teljes azok arany részleges tisztítása és összehasonlítása a viszonylagos tevékenységek alapján különböző extrakciós körülmények ” , Biokémia , vol. 59, n csont 5-6 1977. július, P. 453-462 ( PMID 329894 , DOI 10.1016 / S0300-9084 (77) 80050-3 , online olvasás )
- (a) Kelly Sheppard, Jing Yuan, Michael J. Hohn, Brian Jester, Kevin Devine és Dieter Söll , " Az egyik aminosavat Vélemények másik: tRNS-függő aminosav bioszintézis " , Nucleic Acids Research , Vol. 36, n o 6, 2008. április, P. 1813-1825 ( PMID 18252769 , PMCID 2330236 , DOI 10.1093 / nar / gkn015 , online olvasás )
- (in) Richard Giégé , " A korai története tRNS elismerés aminoacil tRNS szintetáz, " , J. Biosci. , vol. 31,2006, P. 477–488 ( PMID 17206068 )
- (in) Patrick O'Donoghue és Zaida Luthey-Schulten , " A szerkezet evolúciójáról az aminoacil-tRNS-szintetázokban " , Microbiology and Molecular Biology Reviews , vol. 67, n o 4, 2003. december, P. 550-573 ( PMID 14665676 , PMCID 309052 , DOI 10.1128 / MMBR.67.4.550-573.2003 , online olvasás )
- (in) Michael Ibba és Dieter Söll , " amino-acil-tRNS-Synthesis " , Annual Review of Biochemistry , Vol. 69, 2000. július, P. 617-650 ( PMID 10966471 , DOI 10.1146 / annurev.biochem.69.1.617 , online olvasás )
- (in) Jurij I. Farkas, L. Aravind, Nick V. Grishin és Eugene V. Koonin , " Evolution of amino-acil-tRNS szintetáz-Domain elemzése Egyedi architektúrák és filogenetikai fák feltárja a komplex története Vízszintes géntranszferje " , Genomkutatás , vol. 8, n o 9, 1999. augusztus, P. 689-710 ( PMID 10447505 , DOI 10.1101 / gr.9.8.689 , online olvasás )
- (in) M. Ibba és D. Söll , " Az aminoacil-tRNS szintézis " , Annu. Fordulat. Biochem. , vol. 69, 2000, P. 617-650 ( PMID 10966471 )
- (in) Jiqiang Ling, Noah Reynolds és Michael Ibba , " amino-acil-tRNS szintézis és transzlációs minőségellenőrzés " , Annual Review of Microbiology , vol. 63, 2009. október, P. 61-78 ( PMID 19379069 , DOI 10,1146 / annurev.micro.091208.073210 , olvasható online )