Tejsav
| Tejsav | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
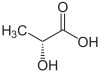
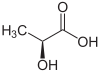
| A tejsav R enantiomerje (fent, balra), S-tejsav (fent, jobbra) és az S-tejsav háromdimenziós szerkezete (alul). | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Azonosítás | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| IUPAC név | 2-hidroxi-propánsav | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS |
(RS) (S+ vagy L) (R- vagy D) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100 000 017 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o EC | 200-018-0 209-954-4 ( RS ) 201-196-2 ( S ) 233-713-2 ( R ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ATC kód | G01 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o E | E270 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| FEMA | 2611 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mosoly |
CC (O) C (= O) O , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = InChI = 1 / C3H6O3 / c1-2 (4) 3 (5) 6 / h2,4H, 1H3, (H, 5,6) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Megjelenés | színtelen vagy sárga viszkózus folyadék vagy színtelen vagy sárga kristályok (DL) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kémiai tulajdonságok | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Képlet |
C 3 H 6 O 3 [izomerek] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Moláris tömeg | 90,0779 ± 0,0037 g / mol C 40%, H 6,71%, O 53,29%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| pKa | 3,86 ( 20 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fizikai tulajdonságok | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fúzió |
D / L : 16,8 ° C L : 53 ° C D : 53 ° C |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° forráspontú | 122 ° C ( 12 Hgmm ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oldékonyság | kissé őrölt. in -éter ; insol. a kloroformot , petrolétert , szén-diszulfid |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Keverhetőség | keverhető vízzel , alkohollal , glicerinnel és furfuraldehiddel , egy szol. alkohol-éter | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Térfogat | 1,248 5 g cm −3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lobbanáspont | 110 ° C (zárt pohár) (DL) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termokémia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C o |
egyenlet:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Optikai tulajdonságok | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Törésmutató | 1.4414 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Forgóerő |
-2,6 ° ( 80 g l -1 , R) + 2,6 ° ( 25 g l -1 , k) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Óvintézkedések | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tejsav: A termék nincs besorolvaEnnek a terméknek az osztályozását még nem erősítette meg a Toxicological Directory Service 1.0% -os nyilvánosságra hozatala az összetevők közzétételi listája szerint Tejsav, (dl-): E,  E : Erősen savas maró anyag (9% -os oldathoz számított pH = 1,9) Kiadás 1,0% -nál az összetevők közzétételi listája szerint |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 67/548 / EGK irányelv | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Xi Szimbólumok : Xi : Irritatív R mondatok : R38 : Bőrizgató hatású. R41 : Súlyos szemkárosodás veszélye. S-mondatok : S26 : Ha szembe jut, bő vízzel azonnal ki kell mosni és orvoshoz kell fordulni. S39 : Viseljen szem- / arcvédőt. R mondatok : 38, 41, S-mondatok : 26, 39, |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kapcsolódó vegyületek | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Izomer (ek) | 3-hidroxi-propánsav | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Egység SI és STP hiányában. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
A tejsav egy szerves sav , amely szerepet játszik a különböző biokémiai folyamatokban . A laktát ennek a savnak a konjugált bázisa (vagyis a tejsav ionizált formája). Ellentétben azzal, amit a neve is sugallhat, a tejsav csak abban a tejben van, amelyből Carl Wilhelm Scheele svéd kémikus először kivonta . Megtalálható a borban , bizonyos gyümölcsökben és zöldségekben , az állati sejtekben is, ahol disszociált és laktát formájában van jelen, valamint bizonyos készítményekben ( savanyú káposzta stb.).
A tejsav egy α-hidroxisav , nyers képlete C 3 H 6 O 3 és szerkezetét szisztematikus neve, a 2-hidroxi-propánsav tükrözi.
Kémia
A atom a szén-dioxid- 2 hordozó csoportot hidroxi van aszimmetrikusan így a molekula tejsav királis . Ezért két enantiomer formájában van :
- ( R ) -tejsav vagy D (-) - tejsav;
- ( S ) -tejsav vagy L (+) - tejsav.
Az oldatot , a karboxil-csoport -COOH lehet veszíteni egy H + ion . Így a tejsav (C 3 H 6 O 3 ) átalakul laktát - ionné : CH 3 CHOHCOO -.
Másrészt az izomban két H + -iont adnak a piruváthoz (C 3 H 3 O 3 ) laktát képződéséhez (C 3 H 5 O 3 2+ ) .
A tejsav vízben oldódik és gyenge savnak tekinthető ( pKa = 3,90), vagyis a vízben történő disszociációs reakció nem teljes:
CH 3 CHOHCOOH+ H 2 O⇄ CH 3 CHOHCOO -+ H 3 O +A tejsav tehát oldatban és bázikus formájában, a laktátionban is megtalálható, a pH-tól függően változó arányban .
Izomfeszültség és tejsavas erjedés
A tejsav különösen az izmok energiatermelésének egyik kulcsfontosságú terméke. A sejtlégzés (a cukrok fogyasztása az energia előállítása érdekében) két fő szakaszra bontható, az első a glikolízis , a folyamat citoplazmatikus része , amely oxigén hiányában megy végbe. Piruvátot szolgáltat, amely biztosítja a sejtlégzés második, mitokondriális részét ( Krebs-ciklus és oxidatív foszforiláció), ami az oxigén redukcióját eredményezi a vízben. A lánc egyik végén a glükóz oxidálódik, a másikban az oxigén csökken. A felszabadult energiát a sejt visszanyeri.
Ha az oxigénellátás nagyobb, mint a cukorfogyasztás, akkor az előállított piroszav teljes mennyisége azonnal elfogy a mitokondriális részben.
Ha a cukorfogyasztás nagyobb lesz, mint az oxigénellátás (intenzív erőfeszítések), akkor a folyamat első részében előállított pironsav egy része tejsavvá redukálódik, ami lehetővé teszi a glikolízis oxidatív ciklusának folytatását. Ez egy erjedés . A mitokondriális rész telített, és az energiahozam jelentősen csökken. A cukor- / oxigénfogyasztás ezen elméletét azonban megkérdőjelezik. Ami az anaerob energiahozamot illeti, az arányosan magasabbnak tűnik, mint az aerob energiahozam, ellentétben az általánosan elfogadottal.
A laktát áthalad a sejtmembránon és bejut a véráramba. A máj , a vázizmok, a szív és az agy felhasználhatja ezt a szubsztrátot energiához. A máj újrahasznosítja az úgynevezett glükoneogenezisben, amely újraszintetizálja a glükózt, míg egy másik részét a szívizom, valamint a sportos erőfeszítések által kevésbé igényelt izmok oxidálják. A laktát a testmozgás után körülbelül egy órával metabolizálódik a testmozgás utáni sporttevékenység nélkül, azaz jóval az izommerevség megjelenése előtt , amiért ezért nem felelős.
Bakteriális erjedés
A tejsavat termelő baktériumfermentációnak két fő típusa van: a borban és a tejtermékekben.
- A borban ez a tejsavas erjedés : a borban természetesen található almasav baktériumok hatására tejsavvá bomlik.
- A tejben és a tejtermékekben a tejsav a laktóz baktériumok általi lebontásából származik . Minél frissebb a tej, annál kevesebb tejsavat tartalmaz. A tej tejsavkoncentrációja Dornic-fokban (° D) van kifejezve : 1 ° D 0,1 g tejsavnak felel meg liter tejben. A friss tej tartalmaz 15- a 18- ° D , ez fürj 60 - 70 ° D .
A tejsav megjelenéséért felelős szervezetek a laktobacillusok . Amikor a szájban működnek, a keletkezett tejsav üregekhez vezethet .
Ez a tejsavas erjedési mód bizonyos zöldségeknél is előfordul ( káposzta = savanyú káposzta és más úgynevezett „laktóban erjesztett” zöldségek). Tejsav használt AHA a kozmetikumokban nem tejből kivont, de például, cukor cékla , fekete áfonya , stb
Használ
Forrás.
Közvetlenül az emberi táplálékban
A tejsavat az élelmiszeriparban adalékként (E270) használják antioxidánsként , savasítószerként vagy ízfokozóként . A tejsav sók formájában is jelen van: nátrium ( E325 ), kálium ( E326 ) és kalcium ( E327 ) só . Ezek a sók por alakúak és vízben is oldódnak. Bakteriosztatikus ágensként működik, különösen olyan patogén baktériumokon, mint a szalmonella (vagy listeria ), és a víz aktivitására is depresszív hatást gyakorol .
Quebec-ben végzett kutatások szerint úgy tűnik, hogy a tejsav az egyik legtermészetesebb eszköz a húgyhólyagrák megelőzésére , de a bőré is .
A kozmetikában
Ezt a savat néha esztétikus héj részeként használják, különösen a színes bőr számára (az esztétikai elszíneződési termékek sorozata tejsavból áll); ezt a savat azonban bőrgyógyász felügyelete mellett, a beteg bőrtónusának megfelelő adagolási és fajlagos hígítási körülmények között kell alkalmazni.
Dekontamináló szerként és tisztítószerként
A tejsav a 2000-es évek után előtérbe került a mosószeriparban, jó vízkőtelenítő , szappaneltávolító és antibakteriális szer. Ez gazdaságilag is előnyös, és része a környezetre biztonságosabb és természetesebb összetevők felé irányuló tendenciának. A tejsavat ezért az Egyesült Államokban használják a szarvasmarha tetemek baktériummentesítésére a vágóhidakon . A marhahúst, amelyre ez a gyakorlat vonatkozik, először az Európai Unió betiltotta , mivel a tejsav használata a laza fakitermelési gyakorlatokkal kapcsolatos higiénia hiányának orvoslására szolgál. Az észak-amerikai marhahús Európába történő behozatalára vonatkozó kompromisszum részeként a hormonhús- marhahús embargóját követően ezt a felhasználást a kezdetektől a 101/2013 európai rendelet közzététele után engedélyezték.2013 február. Európában ez a gyakorlat elvileg nyomon követhető.
Műanyag prekurzor
A tejsav polimerizáljuk , így politejsav (PLA), a biológiailag lebomló műanyag alkalmazni, különösen a 3D-nyomtatók , az élelmiszer-csomagolás és a műtét .
Történelmi
A tejsavat Carl Wilhelm Scheele (1742-1786) fedezte fel .
Kereskedelmi
Franciaország a francia szokások szerint 2014-ben a tejsav nettó importőre. Az átlagos tonnánkénti importár 1400 euró volt.
Megjegyzések és hivatkozások
- tejsav, a kémiai biztonsági nemzetközi program biztonsági adatlapja (i) , konzultálva 2009. május 9-én
- " CAS-nyilvántartási szám: 50-21-5 " , az ntp.niehs.nih.gov címen (hozzáférés : 2010. február 14. )
- számított molekulatömege a „ atomsúlya a Elements 2007 ” on www.chem.qmul.ac.uk .
- (en) JG Speight és Norbert Adolph Lange, Lange kémiai kézikönyve , New York, McGraw-Hill ,2005, 16 th ed. , 1623 p. ( ISBN 978-0-07-143220-7 , LCCN 84643191 ) , p. 2,289
- (a) Carl L. yaws, Handbook of Termodinamikai diagramok , Vol. 1, Huston, Texas, Gulf Pub. Co.,1996( ISBN 978-0-88415-857-8 , LCCN 96036328 )
- (en) Maryadele J. O'Neil, Ann Smith, Patricia E. Heckelman és Susan Budavari, The Merck Index: An Encyclopedia of Chemicals, Drugs and Biologicals , Egyesült Államok, Merck,2001, 13 th ed. , 2564 p. ( ISBN 978-0-911910-13-1 )
- „ tejsav ” az adatbázis a vegyi anyagok Reptox a CSST (Quebec szervezet felelős a munkahelyi biztonság és egészségvédelem), elérhető április 24, 2009
- „ A tejsav (dl) ” az adatbázisban vegyszerek Reptox a CSST (Quebec szervezet felelős a munkahelyi biztonság és egészségvédelem), elérhető április 25, 2009
- " Tejsav " , a societechimiquedefrance.fr oldalon (hozzáférés : 2019. szeptember 18. )
- (a) George A. Brooks , " The Science and Translation Laktát Shuttle Theory " , Cell Metabolism , Vol. 27, n o 4,2018. április, P. 757-785 ( ISSN 1550-4131 , DOI 10.1016 / j.cmet.2018.03.008 , olvasható online , elérhető május 30, 2018 )
- Luc Léger , Georges Cazorla , Cyril Petibois és Laurent Bosquet , „ Laktát és testmozgás: mítoszok és valóságok ”, Staps , vol. No. 54, n o 1,2001, P. 63–76 ( ISSN 0247-106X , DOI 10.3917 / sta.054.0063 , online olvasás , hozzáférés : 2018. május 30. )
- Pascal Prevost, „ Courbatures ” , a Sciensport- on ,2006(hozzáférés : 2008. január 8. )
- ENSZ Wiesmann , S. DiDonato és NN Herschkowitz , „ A klorokin hatása a tenyésztett fibroblasztokra: lizoszomális hidrolázok felszabadulása és felvételük gátlása ”, Biochemical and Biophysical Research Communications , vol. 66, n o 4,1975. október 27, P. 1338-1343 ( ISSN 1090-2104 , PMID 4 , olvasható online , elérhető 1 -jén április 2018 )
- C. Chêne (2002), Szerves savak [PDF] , Agrár-élelmiszeripari vállalkozások technológiai erőforrás-központja, http://www.adrianor.com .
- http://sante.canoe.com/channel_health_news_details.asp?channel_id=2001&relation_id=3483&news_channel_id=2001&news_id=3695
- Kérdések és válaszok a szenátusban
- " Az import / export kereskedelem mutatója " , a Vámigazgatóságon. Adja meg NC8 = 29181100 (hozzáférés : 2015. augusztus 7. )
Lásd is
Kapcsolódó cikkek
- Élelmiszer-adalék
- Aroma
- Tej és bor
- Tejsav , biológiailag lebontható polimer
Külső linkek
- [videó] "Molecular Mojito - Molecular Cocktail - Molecular Cuisine - Molecular Gasztronómia" a YouTube-on ,2016. november 15.
Bibliográfia
- Ackerman SH és Sachar EJ (1974), A szorongás laktátelmélete: áttekintés és átértékelés , Psychosom. Med. , 1974. január – február, 36. (1), 69–81.





