Oxaziridin
| Oxaziridin | |
| Azonosítás | |
|---|---|
| IUPAC név | Oxaziridin |
| N o CAS | |
| PubChem | 15817734 |
| Mosolyok |
C1NO1 , |
| InChI |
InChI: InChI = 1S / CH3NO / c1-2-3-1 / h2H, 1H2 InChIKey: SJGALSBBFTYSBA-UHFFFAOYSA-N |
| Kémiai tulajdonságok | |
| Brute formula |
C H 3 N O [izomerek] |
| Moláris tömeg | 45,0406 ± 0,0015 g / mol C 26,67%, H 6,71%, N 31,1%, O 35,52%, |
| Egység SI és STP hiányában. | |
A oxaziridines egy osztály szerves vegyületek Heterociklusos három szénatomot tartalmazó atom szénatom , egy atom nitrogén- és egy atom oxigén . Oxaziridin CH 2 NHOis a szülő vegyület a funkciós csoport .
Általános tulajdonságok
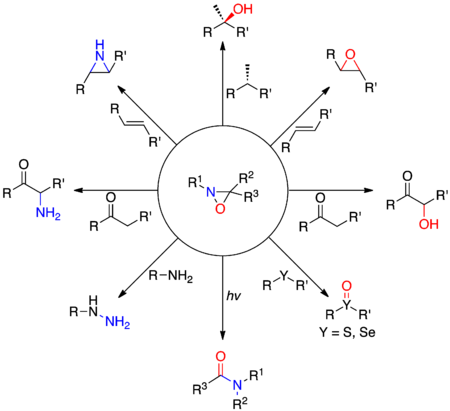
Az oxaziridinek első származékait az 1950-es években szintetizálták Emmons, Krimm, valamint Horner és Jürgens. Míg az oxigén- és nitrogénatomok nagy elektronegativitásuk miatt általában nukleofilekként működnek , az oxaziridinek lehetővé teszik a két heteroatom elektrofil átadását . Ez a különleges reakcióképesség az erősen korlátozott háromatomos gyűrű jelenlétének és az NO-kötés relatív gyengeségének köszönhető. A nukleofil hajlamosak támadni a nitrogén az oxaziridin, amikor a szubsztituens a nitrogénatomon kicsi (jellegzetesen R 1 = H), és az oxigén, amikor a szubsztituens a atom nitrogén nagyon sztérikusan gátolt . Ezek az elektronikus hatások kihasználható végez különböző oxigén- vagy nitrogénatom transzfer reakciók, mint például a α-hidroxilezése enolátok , a epoxidálást az alkének vagy a szelektív oxidációja szulfidok és szelenidek. .
Kiralitás
Kidolgozták az oxaziridin-származékok királis reagenseit , amelyek lehetővé teszik a sztereospecifikus heteroatomok átvitelének reakcióit . Az oxaziridinek kiralitása a gyűrű szubsztituenseinek szerkezetéből vagy a nitrogénatom ( invertomer ) konformációjából származhat . Az oxazirinek valójában egyedülállóak a nagyon magas nitrogén-inverziós gát miatt, amely lehetővé teszi sztereokémiai konfigurációjuk megőrzését. Ez a gát szobahőmérsékletre való inverziója 24 és 31 kcal · mol -1 közötti nagyságrendű , és az 1980-as években enanti tiszta oxaziridineket készítettek .
A kámforszármazékokon alapuló oxaziridin- származékokat az 1970-es években szintetizálták , és az aszimmetrikus szintézis alapkövévé váltak . Az oxaziridinek felhasználásával végzett összes teljes szintézis közül a taxol Holton és Wender csapata általi teljes szintézise az aszimmetrikus α-hidroxilezést javasolja kámforszulfoniloxaxiridinnel, mint kulcsfontosságú lépés ezen rákellenes szer szintézisében.
Szintézis
NH, N-alkil, N-ariloxaziridinek
A két fő stratégiát szintézisére NH, N-alkil- és N-Aryloxaziridines vannak (A) oxidációja az iminek által persavak és (B) aminálás a karbonilok .

Ezenkívül a királis iminek oxidációja és az iminek királis savakkal való oxidációja enantiomerileg tiszta oxaziridinek előállításához vezethet .
N-szulfonil-oxaziridinek
Az 1980-as évek elején elkészítették az első N-szulfonil-oxaziridint. Ezeket a szulfonil- származékokat kizárólag oxigénatomátviteli reakciókhoz használják, és jelenleg az oxaziridinek leggyakrabban használt osztályai. Eredetileg m-CPBA-ból és benzil-trimetil-ammónium-kloridból fázistranszfer katalizátorként állították elő. A szintézis javítása lehetővé teszi a kálium-hidrogén- szulfát vagy az oxon alkalmazását oxidálószerként.
Számos N-szulfonil-oxaziridin-származékot használnak, amelyek mindegyikének eltérő fizikai-kémiai tulajdonságai és reakcióképessége van. E különböző reagensek összefoglalását a következő táblázat tartalmazza.

Perfluorozott oxaziridinek
A perfluorált (in) oxaziridin- származékok erőteljes reakcióképességet mutatnak az egyenértékű szénhidrogénhez képest . A perfluorozott szubsztituensek elektron-akceptorok, így a perfluorozott oxaziridinek reakcióképessége hasonló a dioxiránok reakcióképességéhez . A perfluor-alkil-oxaziridinek különösen hidroxilezhetnek bizonyos CH-kötéseket nagyon nagy szelektivitással. A perfluorozott oxaziridinek szintetizálhatók egy perfluorozott imin perfluor-metil-fluor- karbonil- peroxiddal és egy fluorozott fémmel történő reakciójával a HF elszívására. megjelent.

Reakciók
Az oxigénatom transzferek
Az enolátok a-hidroxilezéseAz α-hidroxi- ketoncsoport vagy aciloin sok természetes termékben található egység. Sok szintetikus utak volna használni, hogy reprodukálja ezt a motívumot, mint például a csökkentése az α-deiketones, a szubsztitúció a hidroxilcsoportok egy kilépő csoport , vagy a közvetlen oxidációjával egy enolát . Ez utóbbi módszerben az oxodiperoxi-molibdén (piridin) - (hexametil-foszforsav-triamid) (MoOPH) és az N-szulfonil-oxaziridinek a leggyakrabban használt elektrofil oxigénforrások . Az N-szulfonil-oxaziridinek előnye, hogy nagyobb kiralitást váltanak ki a MoOPH és más oxidánsok alkalmazásához képest. A királis indukciót sok más királis ketonnal és királis segédanyagokkal rendelkező ketonokkal, például SAMP- nal és RAMP- val igazolták .

A prokiral- enolátok kámforszulfonil-oxaziridin-származékokkal történő aszimmetrikus hidroxilezésével kapcsolatos munkát végeztek, lehetővé téve a jó enantiomer-felesleg elérését . Általánosan elfogadott, hogy az átmeneti állapot, amely lehetővé teszi ennek a jó sztereokémiának az elérését, egy nyitott átmeneti állapotot foglal magában, amelyben a szterikailag akadályozott csoport határozza meg azt az oldalt, amelyen a molekula megközelíti.

A szelektivitás bizonyos hidroxilációk javítható hozzáadásával koordináló csoportok az alfa helyzetben a oxaziridin-gyűrű, mint a oxaziridines 3b és 3c a fenti táblázatban. Javasoljuk, hogy a reakció zárt átmeneti állapoton megy keresztül , amelyben a fém-oxianion kelátképződéssel stabilizálódik a szulfátnak és a kámfor koordináló csoportjainak köszönhetően .

Az oxaziridinekkel végzett a-hidroxilezést nagyon széles körben alkalmazták a teljes szintézis során . Ez kulcsfontosságú lépés a taxol Holton (in) teljes szintézisében és a taxol Wender (en) teljes szintézisében . Hasonlóképpen, Forsyth is ezt a reakciót használja az okadainsav C3-C14 rendszerének (1,7-dioxaspiro [5.5] undec-3-én szubsztituált) szintézisében.
 Az alkének epoxidálása
Az alkének epoxidálása
A epoxidálást az alkének széles körben használják a szerves szintézis , mivel epoxidok lehet alakítani számos funkciós csoportok . Az epoxidálás során általában m-CPBA-t (vagy más savsavakat ) használnak, de az oxaziridnekről kimutatták, hogy hasonló szintézisek elvégzésére alkalmasak, és nagyon hasznosak savas körülményekre érzékeny epoxidok előállításához . Az alábbiakban ismertetjük a (-) - kaotominin szintézisét, amely az alkén oxaziridin általi epoxidációját használja szintézisének utolsó szakaszai egyikében.

A szerves szintézis feldolgozási osztályában még egy széles körben használt epoxidációs aszimmetrikus , mint a Sharpless epoxidáció , Jacobsen epoxidáció vagy Julia-Colonna (en) epoxidációja . E reakciók legfőbb hátránya, hogy a szelektivitáshoz nagyon specifikus funkciókra van szükség . Sharpless epoxidációs működik allil-alkoholok , Jacobsen epoxidálásról cisz- diszubsztituált alkének a aromások, és Julia-Colonna epoxidálásával telítetlen α-β ketonok . Használata aszimmetrikus oxaziridines lehetővé teszi, hogy végezzen sztereospecifikus transzformációk a funkcionálisan nem alkének . Az alábbi reakcióvázlat mutatja az epoxidálási a transstilbene királis oxaziridiniumsók sót használva oxont , mint egy oxidálószer.
 Dezaktivált szénhidrogén hidroxilezés
Dezaktivált szénhidrogén hidroxilezés
A oxaziridines perfluorozott (en) ismert, hogy hidroxilezni a szénhidrogének dezaktivált nagy regio- és diastéréospécificité . Ez a reakció nagyon fontos, és kevés más vegyület mutat ilyen típusú reaktivitást. A perfluorozott oxaziridinek nagyon jó szelektivitást mutatnak a tercier szénnel szemben . Soha nem figyelték meg a primer szénatomok hidroxilezését vagy a két oxidálható hellyel rendelkező vegyületek dihidroxilezését. A sztereokémia retenciója nagyon magas, 95-95% nagyságrendű, és tovább növelhető fluorid-só hozzáadásával .

Nitrogénatom transzferek
Kevesebb figyelmet szenteltek az oxaziridineknek, mint nitrogénatom transzfer reagenseknek. Az oxaziridinek, amelyek nem szubsztituáltak, vagy amelyek a nitrogénatomon acilcsoporttal rendelkeznek, használhatók ilyen reakciókhoz, az első példa a hatvanas évekből származik .
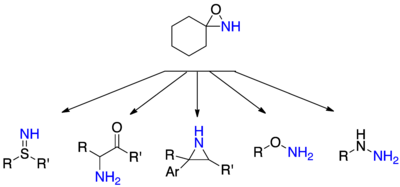
Az N-nukleofilek megsemmisítéseA aminálást a nukleofil a oxaziridines szubsztituálatlan nitrogénatomon nagyon sokoldalú tekintetében nukleofilekkel, amely felhasználható. A hidrazinok tehát előállíthatók a a aminok szekunder vagy tercier aminok, hidroxil- és a thiohydroxylamines el az alkoholok és a tiolok , a szulfil-imin a tioéterek és α-amino-ketonok el az enolátok .
 N-acilamidálás
N-acilamidálás
Az acilezett aminok átadása nehezebb, mint a helyettesítetlen aminoké. Ezeket a transzferreakciókat először nukleofilek , például aminok és hidrazinok alkalmazásával hajtották végre . Néhány ritka példát is leírtak az acilezett aminok nukleofil szénatomokba történő átvitelére.

Átrendezések
Az oxaziridinek ultraibolya besugárzás útján átrendeződési reakciókat hajthatnak végre , radikális mechanizmus útján vagy redukálószer, például CuI jelenlétében .. A spirociklusos oxaziridinek szintén meghosszabbíthatják ciklusukat, hogy megkapják a megfelelő laktámot . Migrációja a szubsztituens által ellenőrzött sztereoeiektronikus hatásokat, és a transz -csoport a nem- nitrogén -kötő dublett túlnyomórészt ad a migrációs termék. Ez a hatás lehetővé teszi a nitrogén kiralitásának felhasználását a magas nitrogén inverziós gát miatt az átrendeződés irányítására, amint azt az alábbi ábra bemutatja. Az ábra bal oldalán kizárólag a termodinamikailag kedvezőtlen termék figyelhető meg, míg a diagram jobb oldalán a kevésbé stabil gyökös köztitermékből származó termék részesül előnyben.

Ez a típusú átrendezési használunk kulcsfontosságú lépés a teljes szintézis a (+) - yohimbin , természetes hatóanyag, amely lehet ellen hatásos impotencia és a szexuális problémák által okozott szelektív szerotonin-újrafelvétel inhibitorok szerinti hatóanyag. National Institutes of Health .

Az oxaziridinek termikus átrendeződési reakciókon is áteshetnek, így nitronokat kapnak . A cisz-transz szelektivitás alacsony, de a hozamok jók. Az is elképzelhető, hogy bizonyos oxaziridinek idővel racemizálódnak egy nitron köztiterméken átjutva .

Cycloaddionok heterokumulénekkel
Az oxaziridinek hetero kumulénekkel reagálva különböző öt atom heterociklust eredményezhetnek , amint az az alábbi ábrán látható. Ez a reaktivitás a háromatomos gyűrű korlátozásának és az NO-kötés gyengeségének köszönhető.

Megjegyzések és hivatkozások
- számított molekulatömege a „ atomsúlya a Elements 2007 ” on www.chem.qmul.ac.uk .
- (in) WD Emmons , " Az oxaziránok szintézise " , J. Am. Chem. Soc. , vol. 78, n o 23,1956, P. 6208–6209 ( ISSN 0002-7863 és 1520-5126 , DOI 10.1021 / ja01604a072 ).
- (de) H. Krimm , " Uber-izonitron " , Chem. Ber. , vol. 91, n o 5,1958, P. 1057-1068 ( ISSN 0009-2940 , DOI 10.1002 / cber.19580910532 ).
- (de) L. Horner és E. Jürgens , „ Notiz Über Darstellung und Eigenschaften einiger Isonitrone (Oxazirane) ” , Chem. Ber. , vol. 90, n o 10,1957, P. 2184–2189 ( ISSN 0009-2940 , DOI 10.1002 / cber.19570901010 ).
- (EN) FA Davis és AC Sheppard , „ Applications of oxaziridines a szerves szintézisekben ” , Tetrahedron , Vol. 45, n o 18,1989, P. 5703–5742 ( DOI 10.1016 / S0040-4020 (01) 89102-X ).
- (a) FA Davis , R. Jenkins et al. , " 2 - [(-) - kámfor-10-il-szulfonil] -3- (nitrofenil) oxaziridin: új királis oxidálószer " , J. Chem. Soc., Chem. Gyakori. ,1979, P. 600-601 ( ISSN 0022-4936 , DOI 10.1039 / C39790000600 ).
- (a) RA Holton , C. Somoza et al. , „ A taxol első teljes szintézise. 1. A B gyűrű funkcionalizálása ” , J. Am. Chem. Soc. , vol. 116, n o 4,1994, P. 1597–1598 ( ISSN 0002-7863 és 1520-5126 , DOI 10.1021 / ja00083a066 ).
- (a) RA Holton , HB Kim et al. , „ A taxol első teljes szintézise. 2. A C és D gyűrűk kiteljesedése ” , J. Am. Chem. Soc. , vol. 116, n o 4,1994, P. 1599–1600 ( ISSN 0002-7863 és 1520-5126 , DOI 10.1021 / ja00083a067 ).
- (a) PA Wender , NC Badham et al. , „ A taxinokhoz vezető pinene út. 5. Egy sokoldalú taxán prekurzor sztereokontrollált szintézise ” , J. Am. Chem. Soc. , vol. 119, n o 11,1997, P. 2755–2756 ( ISSN 0002-7863 és 1520-5126 , DOI 10.1021 / ja9635387 ).
- (a) PA Wender , NC Badham et al. , „ A taxinokhoz vezető pinene út. 6. A taxol tömör sztereokontrollált szintézise ” , J. Am. Chem. Soc. , vol. 119, n o 11,1997, P. 2757–2758 ( ISSN 0002-7863 és 1520-5126 , DOI 10.1021 / ja963539z ).
- (in) FA Davis és OD Stringer , " Chemistry of oxaziridines. 2. A 2-szulfonil-oxaziridinek jobb szintézise ” , J. Org. Chem. , vol. 47, n o 9,1982, P. 1774–1775 ( ISSN 0022-3263 és 1520-6904 , DOI 10.1021 / jo00348a039 ).
- .
- (en) FA Davis és BC Chen , „ Az enolátok aszimmetrikus hidroxilálása N-szulfonil-oxaziridinekkel ” , Chem. Fordulat. , vol. 92, n o 5,1992, P. 919–934 ( ISSN 0009-2665 és 1520-6890 , DOI 10.1021 / cr00013a008 ).
- (in) FA Davis és RH Jenkins , " Chemistry of oxaziridines. 3. A szerves kénvegyületek aszimmetrikus oxidációja királis 2-szulfonil-oxaziridinek alkalmazásával ” , J. Am. Chem. Soc. , vol. 104, n o 20,1982, P. 5412–5418 ( ISSN 0002-7863 és 1520-5126 , DOI 10.1021 / ja00384a028 ).
- (en) FA Davis , RT Reddy et al. , „ Az oxaziridinek kémia. 15. Aszimmetrikus oxidációk 3-szubsztituált 1,2-benzizotiazol-1,1-dioxid-oxidokkal ” , J. Org. Chem. , vol. 56, n o 21991, P. 809–815 ( ISSN 0022-3263 és 1520-6904 , DOI 10.1021 / jo00002a056 ).
- (in) JC Towson , MC Weismiller és mtsai. , " (+) - (2R, 8aS) -10- (kamphorilszulfonil) oxaziridin " , Org. Synth. , vol. 69,1990, P. 158 ( ISSN 0078-6209 ).
- (in) FA Davis és JC Towson , " Chemistry of oxaziridines. 11. (Camphorylsulfonyl) oxaziridin: szintézis és tulajdonságok ” , J. Am. Chem. Soc. , vol. 110, n o 25,1988, P. 8477–8482 ( ISSN 0002-7863 és 1520-5126 , DOI 10.1021 / ja00233a025 ).
- (en) RD Bach , BA Coddens et al. , „ Az oxaziridin szulfiddá és szulfoxiddá történő oxigénátadásának mechanizmusa: elméleti tanulmány ” , J. Org. Chem. , vol. 55, n o 10,1990, P. 3325–3330 ( ISSN 0022-3263 és 1520-6904 , DOI 10.1021 / jo00297a062 ).
- (in) FA Davis , A. Kumar és mtsai. , „ Az oxaziridinek kémia. 16. A γ-rodomicionon és az α-citromicinon AB-gyűrűs szegmenseinek rövid, nagyon enantioszelektív szintézise (+) - [(8,8-dimetoxi-kamforil) -szulfonil] -oxaziridin alkalmazásával " , J. Org. Chem. , vol. 53, n o 3,1991, P. 1143–1145 ( ISSN 0022-3263 és 1520-6904 , DOI 10.1021 / jo00003a042 ).
- (en) FA Davis , MC Weismiller et al. , „ (Camphorylsulfonyl) imin-dianion új optikailag tiszta (kamporylszulfonil) oxaziridin-származékok szintézisében ” , Tetrahedron Lett. , vol. 30, n o 13,1989, P. 1613-1616 ( ISSN 0040-4039 , DOI 10.1016 / S0040-4039 (00) 99534-0 ).
- (in) BC Chen , MC Weismiller és mtsai. , „ (+) - kjellmanianone enantioszelektív szintézise ” , Tetrahedron , vol. 47, n o 21991, P. 173–182 ( ISSN 0040-4020 , DOI 10.1016 / S0040-4020 (01) 80914-5 ).
- (en) VA Petrov és G. Resnati , „ Polifluorozott oxaziridinek: szintézis és reaktivitás ” , Chem. Fordulat. , vol. 96, n o 5,1996, P. 1809–1824 ( ISSN 0009-2665 és 1520-6890 , DOI 10.1021 / cr941146h ).
- (a) DA Evans úr Morrissey és mtsai. , „ A királis imid aszimmetrikus oxigénellátása enolál. Az enantiomertiszta α-hidroxi-karbonsav-szintonok szintézisének általános megközelítése ” , J. Am. Chem. Soc. , vol. 107, n o 14,1985, P. 4346–4348 ( ISSN 0002-7863 és 1520-5126 , DOI 10.1021 / ja00300a054 ).
- (a) RA Holton , HB Kim et al. , „ A taxol első teljes szintézise. 2. A C és D gyűrűk kiteljesedése ” , J. Am. Chem. Soc. , vol. 116, n o 4,1994, P. 1599–1600 ( ISSN 0002-7863 és 1520-5126 , DOI 10.1021 / ja00083a067 ).
- (a) PA Wender , NC Badham et al. , „ A taxinokhoz vezető pinene út. 5. Sokoldalú taxán prekurzor sztereokontrollált szintézise ” , J. Am. Chem. Soc. , vol. 119, n o 11,1997, P. 2755–2756 ( ISSN 0002-7863 és 1520-5126 , DOI 10.1021 / ja9635387 ).
- (in) AB Dounay és CJ Forsyth , " Okadainsav C3-C14 (helyettesített 1,7-dioxaspiro [5.5] undec-3-én) rendszerének rövidített szintézise " , Org. Lett. , vol. 1, n o 3,1999, P. 451-454 ( ISSN 1523-7060 és 1523-7052 , DOI 10.1021 / ol9906615 ).
- (en) B. Malgesini , B. Forte és mtsai. , „ A (-) - kaotominin egyenes teljes szintézise ” , Chem. Eur. J. , vol. 15, n o 32,2009, P. 7922–7929 ( ISSN 0947-6539 és 1521-3765 , DOI 10.1002 / chem.200900793 ).
- (in) L. Bohé G. Hanquet et al. , „ Egy új királis oxaziridinium-só sztereospecifikus szintézise ” , Tetrahedron Lett. , vol. 34, n o 45,1993, P. 7271–7274 ( ISSN 0040-4039 , DOI 10.1016 / S0040-4039 (00) 79306-3 ).
- (in) A. Arnone , S. Foletto és mtsai. , „ A nem aktivált szénhidrogén helyek rendkívül enantiospecifikus oxifunkcionálása perfluor-cisz-2-n-butil-3-n-propiloxaziridinnel ” , Org. Lett. , vol. 1, n o 21999, P. 281–284 ( ISSN 1523-7060 és 1523-7052 , DOI 10.1021 / ol990594e ).
- (de) E. Schmitz , R. Ohme és mtsai. , „ Isomere Oxime mit Dreiringstruktur ” , Chem. Ber. , vol. 97, n o 9,1964, P. 2521–2526 ( ISSN 0009-2940 , DOI 10.1002 / cber.19640970916 ).
- (en) S. Andeae és E. Schmitz , " Elektrofil aminálás oxaziridinekkel " , Szintézis , n o 5,1991, P. 327-341 ( ISSN 0039-7881 és 1437-210X , DOI 10.1055 / s-1991-26459 ).
- (en) J. Aubé , „ Oxiziridine átrendeződések aszimmetrikus szintézisben ” , Chem. Soc. Fordulat. , vol. 26, n o 4,1997, P. 269-277 ( ISSN 0306-0012 és 1460-4744 , DOI 10.1039 / CS9972600269 ).
- (en) A. Lattes , E. Oliveros és munkatársai. , „Az oxaziridinek fotokémiai és termikus átrendeződése. Kísérleti bizonyítékok a sztereoelektronikus kontrollelmélet alátámasztására ” , J. Am. Chem. Soc. , vol. 104, n o 14,1982, P. 3929–3934 ( ISSN 0002-7863 és 1520-5126 , DOI 10.1021 / ja00378a024 ).
- „ Yohimbe ” az nlm.nih.gov-tól (hozzáférés : 2012. augusztus 27. ) .
- ( Fr ) Ez a cikk részben vagy egészben venni a Wikipedia cikket angolul című „ oxaziridin ” ( lásd a szerzők listáját ) .