Nemesgáz-kémia
A nemesgázok , gyakran nevezik nemesgázok , ritkán inert gáz (lásd cikket nemesgáz ezekről különböző nevek) egy család az elemek a priori nagyon reaktív, mert, amelynek vegyértéke héj teljes, akkor n „nincs elektron a vegyérték alkotnak egy kémiai kötés . Ennek eredményeként ezeknek az elemeknek nagy az ionizációs energiájuk és gyakorlatilag nulla elektron-affinitásuk van , és sokáig azt hitték, hogy nem vehetnek részt semmilyen kémiai reakcióban vegyületek képződéséhez .
| 1 | 2 | 3 | 4 | 5. | 6. | 7 | 8. | 9. | 10. | 11. | 12. | 13. | 14 | 15 | 16. | 17. | 18. | ||
| 1 | H | Hé | |||||||||||||||||
| 2 | Li | Lenni | B | VS | NEM | O | F | Született | |||||||||||
| 3 | N / A | Mg | Al | Igen | P | S | Cl | Ar | |||||||||||
| 4 | K | Azt | Sc | Ti | V | Kr. | | Mn | Fe | Co | Vagy | Cu | Zn | Ga | Ge | Ász | Se | Br | Kr | |
| 5. | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | CD | Ban ben | Sn | Sb | Ön | én | Xe | |
| 6. | Cs | Ba |
* |
Olvas | HF | A te | W | Újra | Csont | Ir | Pt | Nál nél | Hg | Tl | Pb | Kettős | Po | Nál nél | Rn |
| 7 | Fr | Ra |
* * |
Lr | Rf | Db | Vminek | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |
| ↓ | |||||||||||||||||||
|
* |
A | Ez | Pr | Nd | Délután | Sm | Volt | Gd | Tuberkulózis | Dy | Ho | Er | Tm | Yb | |||||
|
* * |
Ac | Th | Pa | U | Np | Tudott | Am | Cm | Bk | Vö | Is | Fm | Md | Nem | |||||
| Li | Alkálifémek | ||||||||||||||||||
| Lenni | Alkáliföldfémek | ||||||||||||||||||
| A | Lanthanides | ||||||||||||||||||
| Ac | Aktinidák | ||||||||||||||||||
| Sc | Átmeneti fémek | ||||||||||||||||||
| Al | Szegény fémek | ||||||||||||||||||
| B | Metalloidok | ||||||||||||||||||
| H | Nemfémek | ||||||||||||||||||
| F | Halogén | ||||||||||||||||||
| Hé | nemesgázok | ||||||||||||||||||
| Mt | Ismeretlen kémiai természet | ||||||||||||||||||
Elméleti megközelítés
Linus Pauling már 1933-ban megjósolta, hogy a legnehezebb nemesgázok kombinálhatók fluorral , sőt oxigénnel . Pontosabban az XeF 6 xenon-hexafluorid létezését jósoljaés kripton-hexafluorid KrF 6xenon-oktafluorid XeF 8 létezésére spekuláltinstabil, és azt javasolta, hogy a xénsav H 2 XeO 4perxenát sókat képezhetnek XeO 64- . Ezeket az előrejelzéseket majdnem pontosnak találták, bár a későbbi vizsgálatok azt mutatták, hogy a xenon-oktafluorid XeF 8nemcsak termodinamikailag, hanem kinetikailag is instabil lenne; a mai napig nem szintetizálták.
A nehezebb nemesgázok valóban több elektronréteggel bírnak, mint a könnyebbek, így a perifériás elektronok számára a belső elektronikus rétegek inkább a nehéz atomokban ( xenon , kripton , argon ), mint a könnyebb atomokban ( neon , hélium ) vetítik át a magot . Ennek eredményeként ezek a nehezebb nemesgázok alacsonyabb ionizációs energiát eredményeznek, amely kellően alacsony ahhoz, hogy stabil vegyületeket képezzenek, amelyek a legtöbb elektronegatív elemet tartalmazzák , jelen esetben fluort és oxigént .
Első ismert nemesgázokat tartalmazó szerkezetek
1962-ig az egyetlen ismert nemesgáz "vegyület" a klatrát és a hidrát volt . Koordinációs vegyületeket is megfigyeltek, de csak spektroszkópiával, izolálás nélkül.
ClathratesEzek a szerkezetek nem igaz kémiai vegyületek a nemesgázokból. Akkor fordulnak elő, amikor egy atom csapdába esik a kristály rácsában vagy bizonyos szerves molekulákban. A nehezebb atomok, például a xenon , a kripton és az argon klatratákat képezhetnek a β-kinollal, de a neon és a hélium túl kicsi ahhoz, hogy csapdába essenek.
A 85 Kr- klatrátok a β-részecskék forrása, míg a 133 Xe- eket y- sugárforrásokként használják .
Koordinációs vegyületekA tényleges megfigyelésüket még soha nem igazolták. Az a megfigyelés, a komplex a argon és bór-trifluorid (Ar • BF 3), Állítólag létezik alacsony hőmérsékleten, nem erősítették meg, és a komplexeket a hélium a volfrám whe 2és higany HgHe 10amelyeket e fémek elektronbombázása után figyeltek meg, valójában a hélium ezen fémek felületén történő adszorpciójának eredményei lennének .
HidratálA nemesgáz- hidrátok valóságáról még mindig vita folyik. Mivel a vízmolekula erősen dipoláris, dipolt kell indukálnia a nemesgáz atomjaiban, közülük a legnehezebb a legérzékenyebb erre a hatásra. Ez a dipól magas nyomáson stabil hidrátok képződéséhez vezetne; a legstabilabb lenne xenon hexahidrát Xe • 6H 2 O.
A nemesgáz első "igazi" vegyületei
A xenon-hexafluor-platinát szintézise
Neil Bartlettnek köszönhetjük a nemesgáz-vegyület első szintézisét, 1962-ben. Az érvelés a következő volt:
- A ionizációs energia az oxigén O 2dioxigenil- oxikációban O 2+ értéke 1 165 kJ / mol az 1 170 kJ / mol ellen, hogy ionizálja Xe-t Xe-ben+ .
- Arany Platinum Hexafluorid PtF 6képes oxidálni az O 2 -otaz O 2 -ben+ .
- Tehát a PtF 6 képesnek kell lennie Xe oxidálására Xe-ben+ mivel az oxigén és a xenon ionizációs energiája hasonló.
Így publikálta Bartlett egy kristályos szilárd anyag szintézisét, amelyet xenon-hexafluor- platinátként Xe- ként fogalmazott meg+ PtF 6- .
Ezt követően bebizonyosodott, hogy a valóságban ez a fázis összetettebb volt, és több molekuláris faj, az XeFPtF 6 keverékéből származott .XeFPt 2 F 11és Xe 2 F 3 PTF 6.
Valóban ez volt az első nemesgázból szintetizált vegyület.
Xenon-fluoridok
A xenon-hexafluor- platinát szintézisét követően Howard Claassen 1962 szeptemberében publikálta a xenon , a xenon- tetrafluorid XeF 4 egyetlen bináris vegyületének szintézisét xenon és fluor keverékének magas hőmérsékletnek való alávetésével.
Két hónappal később az XeF 2 xenon-difluorid jelentette be Rudolf Hoppe.
Azóta a szintetizált nemesgáz-vegyületek túlnyomó részét xenonból állítják elő.
Az eddig ismert nemesgáz-vegyületek áttekintése
Excimerek és exciplexek
Ha az atomok nemesgázok kémiailag nem reaktívak az alapállapotú , tudják, másrészt, formájában komplexeket egymással vagy halogénnel , amikor izgatott . Ezek a komplexek izgatott állapotban stabilak, de disszociálnak, amint az atomok visszaállnak alapállapotukba: ezt akkor nevezzük excimernek, ha a komplex atomjai homogének, vagy exciplexnek, ha a komplex atomjai heterogének. A gerjesztett állapotok és az alapállapot közötti energiaátmenet bizonyos hullámhosszúságú sugárzás eredete, amelyet bizonyos lézerek megvalósításához használnak . A fő fajok:
- Noble gáz excimers : Ar 2 *, Kr 2 *, Xe 2 *.
- Halogének és nemesgázok exclexje : Nef *, ArF *, KrF *, XeF *, ArCl *, KrCl *, XeCl *, XeBr *.
Héliumkémia
Elektronikus konfiguráció a hélium : 1s 2 .Emellett bizonyos számú excimers a volfrám , fluor- , jódatom , kén- és foszfor , hélium kitéve elektronok áramlását (hatása alatt egy bombázás, a kisülés vagy a. Egy plazma) is képezhetnek vegyületek (amelynek „kémiai” valóságban még vitatott) és higany (HgHe 10) és volfrám (WHe 2), valamint HeNe molekuláris ionok+ , He 2+ , He 22+ , HeH+ ( hélium-hidrid ) és HeD+ (hélium-deuterid).
Elméletileg más vegyületek is lehetségesek, például a HHeF hélium-fluor- hidrid, amely analóg lenne a HArF argon- fluorid-hidriddel 2000-ben észlelték.
Egyes számítások szerint a hélium stabil ionos oxidokat képezhet. A modell által megjósolt két új molekuláris faj, a CsFHeOés N (CH 3 ) 4 FHeOA metasztabil OHeF anionból származna- már 2005-ben egy tajvani csapat javasolta, amelyben az O-He kötés kovalens jellegű lenne, és a negatív töltést lényegében a fluoratom hordozza . Ezek a javaslatok azonban egyelőre pusztán spekulációk maradnak.
Neon kémia
Elektronikus konfiguráció a neon : 1s 2 2s 2 2p 6 .A neon az összes nemesgáz-elv közül a legkevésbé reaktív, és általában azt tartják, hogy valójában kémiailag inert. A neonhoz különféle elemekkel ( hidrogén , bór , berillium , nemesfémek ) számított kötési energiák még mindig alacsonyabbak, mint a héliumra számítottak . Nincs semleges neon vegyületet azonosítottak, ellentétben a HNE molekuláris ionokat+ , HeNe+ , Ne 2+ és NeAr+ optikai vagy spektroszkópiai vizsgálatok során figyeltek meg.
Argon kémia
Az argon elektronikus konfigurációja : 1s 2 2s 2 2p 6 3s 2 3p 6 .Az argon valamivel reaktívabb, mint a neon . Az egyetlen ismert vegyület az argon körül az argon- hidrofluorid HArF, 2000 augusztusában szintetizálták a Helsinki Egyetemen . Ezt a molekulát valójában soha nem izolálták, csak spektroszkópiával detektálták. Rendkívül instabil, és legalább 246 ° C-on disszociál argonban és hidrogén-fluoridban .
Kripton kémia
A kripton elektronikus konfigurációja : 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 .A kripton a legkönnyebb a nemesgázok közül , amelyek izolátumaként legalább egy kovalens vegyület volt, ebben az esetben a kripton-difluorid KrF 2, először 1963-ban szintetizálták a xenonnal végzett munka nyomán . Más vegyületeket, amelyekben egy kripton atom kötődik egy nitrogén atom néhány és egy oxigén- atom mások számára, is megjelent, de ezek csak a stabil alatt -60. ° C az első és a -90 ° C-on , a második . Egyes eredmények tehát állapotában a szintézis különböző oxidok és fluoridokat a kripton , valamint egy só a oxosav a kripton (hasonló kémiai xenon ).
Az ArKr molekuláris ionok vizsgálata+ és KrH+ és a KrXe fajok és KrXe+ megfigyelték.
A Helsinki Egyetem csapatai, a HArF argon-fluor- hidrid kimutatásának kiindulópontjánál, a HKrC≡N kripton-ciano-hidridet is kimutatta volna valamint hidrokriptoacetilén HKrC≡CHAmelyek elhatárolódnak 40 K-tól .
Általában szélsőséges körülményekhez ( kriogén mátrix vagy szuperszonikus gázsugár) van szükség ahhoz, hogy megfigyeljük azokat a semleges molekulákat, amelyekben egy kriptonatom kapcsolódik egy nem fémhez , például hidrogénhez , szénhez vagy klórhoz , vagy akár egy átmenetifémhez, például mint réz , ezüst vagy arany .
Xenon kémia
A xenon elektronikus konfigurációja : 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 4d 10 5p 6 .A xenon-hexafluor-platinát volt az első szintetizált xenon- vegyület (és általánosabban egy nemesgáz : lásd fent ).
Ennek a munkának az eredményeként, oxidációs reakciók alapján, számos fluor és / vagy oxigénnel kombinált xenon vegyületet állítottak elő, amely egy sor xenon oxidot , fluort és oxifluoridot eredményezett :
- XeF 2 : Xenon-difluorid
- XeF 4 : Xenon-tetrafluorid
- XeF 6 : Xenon-hexafluorid
- XeO 3 : Xenon-trioxid , robbanásveszélyes szilárd anyag
- XeO 4 : Xenon-tetraoxid
- XeOF 2 : Xenon-oxidifluorid
- XeO 2 F 2 : Xenon-dioxidifluorid
- XeO 3 F 2 : Xenon-trioxidifluorid
- XeOF 4 : Xenon-oxitetrafluorid
- XeO 2 F 4 : Xenon-dioxitetrafluorid
A oxidok a xenon vízben oldódnak, ahol adnak két oxoacids :
A perxénique sav önmagában is képes képezni perxénates , például:
- Na 4 XeO 6 : Nátrium-perxenát , vízben oldódik
- K 4 XeO 6 : Vízben oldódó kálium-perxenát
- Ba 2 XeO 6 : Bárium-perxenát , oldhatatlan
A xenon-dioxid Xeo 2továbbra is ellenáll a szintézis minden kísérletének, és csak az XeO 2 + kationkriogén argonban spektroszkóposan detektáltuk .
Az 1980-as évekig előállított xenonvegyületek túlnyomó többsége fluort és / vagy oxigént kombinált a xenonnal ; intégraient amikor más elemek, mint például a hidrogén vagy a szén , de általában nem volt szén elektronegatív az oxigén és / vagy fluoratommal . Ennek ellenére egy csapat, amelyet Markku Räsänen vezetett a Helsinki Egyetemről, 1995-ben közzétette az XeH 2 xenon- dihidrid szintézisét, majd a HXeOH xenon-hidroxi-hidridé, hidroxenoacetilén HXeCCHés más xenonvegyületek . Ezt követően Khriatchev et al. közzétette a HXeOXeH szintézisétáltal fotolízis vízben egy kriogén xenon mátrixot. Beszámoltak a deuterált HXeOD molekulákról is és a DXeOD. A xenon ismert vegyületeinek száma ma nagyságrendileg ezer nagyságrendű, némelyikben xenon és szén , nitrogén , klór , arany vagy higany közötti kötések láthatók, míg mások, extrém körülmények között megfigyelve ( kriogén mátrixok vagy szuperszonikus gázsugarak), kötéseket mutatnak xenon és hidrogén , bór , berillium , kén , jód , bróm , titán , réz és ezüst .
A xenon egyik legváratlanabb vegyülete az arannyal képzett komplex . A tetraxenon-arany kation AuXe 4A 2+ -ot valóban Konrad Seppelt német csapata jellemezte az AuXe 4 2+ (Sb 2 F 11 - ) 2 komplexumban..
A nemesgáz- vegyületeket hiperkoordinált fajoknak tekintik, mivel megsértik a bájtszabályt . Bonds az ilyen típusú struktúrát lehet leírni szerint három-központ, négy-elektron kötés modellt , amelyben három kollineáris atomok két kötést, mindegyik keletkező három molekulapályák származó p atomi pályák mindegyikének a három atom. Az elfoglalt nagy molekulájú orbitális a ligandumokon koncentrálódik , ezt a konfigurációt az elektronegatív jellegük stabilizálja : jellemzően oxigén és mindenekelőtt a fluor .
A 3C-4e kötést létesíteni két ligandum mindkét oldalán helyezkednek el a xenon atom . A fluoridok a xenon különösen jól leírta ezt a modellt, ami részben magyarázható, hogy miért kell mindig páros számú szénatomot fluorid körül xenon ezekben a vegyületekben, és miért azok geometriai alapja minden esetben „ortogonális F-Xe-F egységek:

|
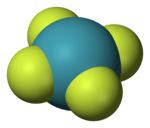
|

|
| Xenon- difluorid XeF 2 | Xenon tetrafluorid XeF 4 | Xenon-hexafluorid XeF 6 |
|---|
A 3c-4e kötést alkotó F-Xe-F egységek két rezonáns ionforma egyensúlyában is láthatók:
F-Xe + - F F - + Xe-FEz a Lewis-képletekkel történő ábrázolás figyelembe veszi a fluoratomok körüli elektronsűrűség növekedését, valamint e molekulák geometriáját is.
Radonkémia
A radon elektronikus konfigurációja : 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 4d 10 5p 6 6s 2 4f 14 5d 10 6p 6 .A radon egy nemesgáz radioaktív . A legstabilabb izotópja, 222 Rn származik 226 Ra és bomlások által α radioaktivitás a 218 Po egy felezési az 3,823 napon. Ezek az adatok szigorúan korlátozzák ennek az elemnek a gyakorlati kutatását, valamint a kutatás lehetséges következményeit, különösen azért, mert ez a nemesgáz meglehetősen drága. Ez az oka annak, hogy bár a radon kémiailag reaktívabb, mint a xenon , eddig viszonylag kevés radonvegyületet tettek közzé; egyszerűen oxidok vagy fluoridok .
A radon-fluoridot az 1970-es években szintetizálták; gyengén illékony szilárd anyag, amelynek pontos összetételét a radon radioaktivitása miatt soha nem állapították meg . Lehet több ionos vegyület, mint kovalens. Az RnF 2 radon-difluorid szerkezetének modellezése208 µm hosszúságot eredményez az Rn-F kötésnél, és kiváló termodinamikai stabilitás az RnF 2 esetébencsak XeF 2 esetén . Az RnF 6 oktaéderes radon-hexafluorid- molekulaaz RnF 2- nél még alacsonyabb kialakulási entalpia lenne.
Az RnF + ionképezné a dioxigenil hexaftuor O 2 AsF 6 a reakciótól függően:
Rn (g)+ 2 O 2 + AsF 6 - (s)→ RnF + As 2 F 11 - (s)+ 2 O 2 (g)Of -oxidok a radon is szintetizáltak, köztük trioxid radon RNO 3a Szovjetunióban. A radon-karbonil-RnCO stabil, lineáris konfigurációjú. Rn 2 molekulák és XeRn szorosan stabilizálódna spin-kapcsolással.
Az oganesson elméleti kémiája
Az oganesson klasszikus elektronikus konfigurációja : 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 4d 10 5p 6 6s 2 4f 14 5d 10 6p 6 7s 2 5f 14 6d 10 7p 6 ?A oganesson egy szintetikus elem, radioaktív a atomszámú 118 és Og szimbólum azé az oszlopra nemesgázok , de kémiailag nagyon különböző ezektől. A nagyon instabil atommag csak lehetővé tette, hogy szintetizálni három atom összesen eddig egy további felezési az 0,89 ms ( nuklidspecifikus 294 Og). Ilyen körülmények között az elem hatalmas tulajdonságaira vonatkozó összes tudásunk elméleti modellekből származik, akiket már az 1960-as években kidolgoztak.
A 118. elem elektronikus felépítése jelentős kémiai reakcióképességet eredményez, ami eltérést eredményezne a nemesgáz-paradigmától, markánsabb elektropozitív karakterrel . Számítások az Og 2 molekuláramegmutatta, hogy ugyanolyan nagyságrendű kötési energiával rendelkezik, mint a Hg 2 higany dimeréés a disszociációs energia 6 kJ / mol , azaz az Rn 2 dimerének négyszerese. De a legszembetűnőbb az, hogy az Og 2-re számított kötéshossz16 órával alacsonyabb lenne , mint az Rn 2, meglehetősen erős kötelék jele. Ennek ellenére az OgH ion+ disszociációs energiája alacsonyabb lenne, mint az RnH ioné+ . A semleges OgH vegyületrendkívül gyenge kötése lenne, amelyet egy tiszta Van der Waals-kötéssel asszimilálnának .
A oganesson úgy tűnik, hogy képeznek stabilabb vegyületek az elemek nagyon elektronegatív , különösen fluoratom a difluorid oganesson OGF 2és oganesson tetrafluorid OGF 4.
Más nemesgázokkal ellentétben a 118 elem állítólag elég elektropozitív ahhoz, hogy kovalens kötéseket képezzen klórral, és OgCl n Oganesson kloridokhoz vezessen..
Fullerene endohéder komplexek
Ez az egyik legtöbbet vizsgált forma a nemesgázok befogására . A fullerének a gömb alakú, ellipszoid alakú, tubuláris ( nanocsövekre utaló ) vagy gyűrűs atomcsoportok . Így megkülönböztetik azokat a klatrátokat, amelyek vízmolekulákból állnak. Ezen fullerének közül a legelterjedtebb hatvan szénatomból áll, amelyek egy csonka ikozaéder tetején helyezkednek el, és a molekulának egy üreges gömb látszatát kelti, amely hasonlít egy futball-labdára . Mivel ezek a molekulák üregesek, meg lehet csapdázni bennük bármilyen nemesgáz atomot , amelyet Ng-nek jelölünk, és komplexet képezünk, amely különleges fizikai-kémiai tulajdonságokkal rendelkezik, amelyet hagyományosan Ng @ 60-val jelölünk. (lásd a szemközti képet).
He @ C 60 komplexek képződéseés Ne @ C 60nyomás alkalmazásával a 300 kPa a hélium vagy neon a fullerén C 60már 1993-ban megjelent. De valójában a 650 000 fullerénmolekulából alig egy adható ilyen módon a nemesgáz endohéderes atomjával ; ez az arány növelhető, hogy egy molekula 1000 nyomás alkalmazásával a 300 MPa a hélium vagy neon .
Ar @ 60 60 endohéder argon komplexeket is kaptunk., A kripton Kr @ C 60és xenon Xe @ C 60.
Megjegyzések és hivatkozások
- Vagyis akinek s és p alhéját kettő, illetve hat elektron foglalja el, így összesen nyolc - kivéve természetesen a héliumot , amelynek az alhéjában csak két elektron van 1 másodperc alatt .
- (a) Linus Pauling , " A képletek a antimonic Acid és a antimonát " , J. Am. Chem. Soc. , vol. 55, n o 5,1933. június, P. 1895–1900 ( DOI 10.1021 / ja01332a016 ).
- (a) John H. Holloway , Noble-Gáz Chemistry , London, Methuen,1968.
- (in) Konrad Seppelt , " Újabb fejlemények a Chemistry of Néhány elektronegatív Elements " , Acc. Chem. Res. , vol. 12,1979. június, P. 211–216 ( DOI 10.1021 / ar50138a004 ).
- (a) JJ Manley , " Mercury Helides " , Nature , n o 117,1926, P. 587–588 ( DOI 10.1038 / 117587b0 ).
- (a) N. Bartlett , " Xenon hexafluoroplatinate Xe + [PTF 6 ] - " , Proceedings of the Chemical Society , n o 6, 1962, P. 218 ( DOI 10.1039 / PS9620000197 ).
- (in) L. Graham , O. Graudejus , NK Jha és N. Bartlett , " Az XePtF 6 fajtájáról " , Coord. Chem. Fordulat. , vol. 197, 2000, P. 321–334 ( DOI 10.1016 / S0010-8545 (99) 00190-3 ).
- Holleman, AF; Wiberg, E. "Szervetlen kémia" Academic Press: San Diego, 2001. ( ISBN 0-12-352651-5 ) .
- (in) HH Claassen , H. Selig és JG Malm , " Xenon-tetrafluorid " , J. Am. Chem. Soc. , vol. 84, n o 18, 1962, P. 3593 ( DOI 10.1021 / ja00877a042 ).
- (a) R. Hoppe , W. Daehne , H. Mattauch és K. Roedder , " fluorozása Xenon " , Angew. Chem. Gyakornok. Ed. Engl. , vol. 1, 1 st november 1962, P. 599 ( DOI 10.1002 / anie.196205992 ).
- (a) Julius W. Hiby, " Massenspektrographische évben Wasserstoff- Untersuchungen und Heliumkanalstrahlen (H 3 + , H 2- , HeH+ , HeD+ , Ő- ) ”, Annalen der Physik ,vol. 426,N o 5,1939, P. 473–487 ( DOI 10.1002 / andp.19394260506 )
- (a) Wah Ming Wong, " Prediction of metastabil Hélium vegyület: HHeF " , J. Am. Chem. Soc. , vol. 122, n o 26, 2000, P. 6289–6290 ( DOI 10.1021 / ja9938175 )
- (in) W. Grochala , " Mi a kémiai kötés a hélium és oxigén " , Pol. J. Chem. , vol. 83, 2009, P. 87–122
- „ Periódusos rendszer: Neon ” ( Archívum • Wikiwix • Archive.is • Google • Mit kell tenni? ) (Hozzáférés : 2013. március 25. ) . Lawrence Livermore Nemzeti Laboratórium . Utolsó frissítés: 2003.12.15 .; konzultált: 2007.08.31
- (en) Neil Bartlett, " A nemes gázok " , Chemical & Engineering News
- (a) John F. Lehmann, PA Hélène Mercier és Gary J. Schrobilgen , " A kémia kripton " , Coord. Chem. Fordulat. , vol. 233-234,2002, P. 1–39 ( DOI 10.1016 / S0010-8545 (02) 00202-3 )
- " http://www.bu.edu/ehs/ih/pdf/periodic_table.pdf " ( Archívum • Wikiwix • Archive.is • Google • Mit kell tenni? ) (Hozzáférés : 2013. március 25. )
- (en) Wojciech Grochala , „ A nemesnek nevezett gázok atipikus vegyületei ” , Chem. Soc. Fordulat. , vol. 36, n o 36,2007, P. 1632–1655 ( DOI 10.1039 / b702109g )
- (a) Zhou, Y. Zhao, Y. Gong és J. Li, " kialakulása és jellemzése a XeOO + kation Solid Argon " , J. Am. Chem. Soc. , vol. 128, 2006, P. 2504–2505 ( DOI 10.1021 / ja055650n )
- " http://www.chemnetbase.com/periodic_table/elements/xenon.htm " ( Archívum • Wikiwix • Archive.is • Google • Mit kell tenni? ) (Hozzáférés : 2013. március 25. )
- (a) GJ Moody , " egy évtizede Xenon Chemistry " , J. Chem. Educ. , vol. 51, 1974, P. 628–630 ( online olvasás , hozzáférés : 2007. október 16. )
- (a) Charlie J. Harding és Rob Janes elemei a P blokk , Cambridge, Royal Society of Chemistry , 2002, 305 p. ( ISBN 978-0-85404-690-4 , LCCN 2005472333 , online olvasás )
- (in) RB Gerber , " Új, ritkán gázmolekulák képződése alacsony hőmérsékletű mátrixokban " , Annu. Fordulat. Phys. Chem. , vol. 55, 2004. június, P. 55–78 ( DOI 10.1146 / annurev.physchem.55.091602.094420 , online olvasás )
- Bartlett, 2003: vö. § kezdete: " Sok friss megállapítás ".
- (in) Leonid Khriachtchev , Karoliina Isokoski Arik Cohen, Markku Räsänen és R. Benny Gerber, " Egy kis molekula semleges, két nemesgázatommal: HXeOXeH " , J. Am. Chem. Soc. , vol. 130, n o 19,2008, P. 6114-6118 ( DOI 10.1021 / ja077835v , online olvasás , hozzáférés : 2008. június 20. )
- (a) Mika Pettersson , Leonyid Khriachtchev Jan Lundell és Markku Räsänen, " egy kémiai vegyület, vízből kapott és Xenon: HXeOH " , J. Am. Chem. Soc. , vol. 121, n o 50, 1999, P. 11904–11905 ( DOI 10.1021 / ja9932784 , online olvasás , hozzáférés : 2007. október 10. )
- (a) Charlie J. Harding és Rob Janes elemei a P blokk , Royal Society of Chemistry ,2002( ISBN 0-85404-690-9 ) , p. 90-99
- (in) Konrád Seppelt és Stefan Seidel, " Xenon mint komplex ligandum: A Tetra Xenono arany (II) kation AuXe 4 2+ (Sb 2 F 11 - ) 2 " , Science , vol. 290, n o 54891993, P. 117–118 ( DOI 10.1126 / science.290.5489.117 )
- (in) L. Stein, " Radon Ionic Solution " , Science , vol. 168, 1970, P. 362 ( PMID 17809133 , DOI 10.1126 / science.168.3929.362 )
- (a) Kenneth S. Pitzer, " Fluorid radon és az elem 118 " , J. Chem. Soc., Chem. Gyakori. , 1975, P. 760–761 ( DOI 10.1039 / C3975000760b )
- (en) Liao Meng-Sheng és Zhang Qian-Er, " Chemical ragasztása XeF 2, XeF 4, KrF 2, KrF 4, RnF 2, XeCl 2és XeBr 2: A gázfázistól a szilárd állapotig ” , J. Phys. Chem. A , vol. 102,1998, P. 10647 ( DOI 10.1021 / JP 9825516 )
- (in) Michael Filatov, " ragasztása radon hexafluorid: Szokatlan relativisztikus probléma? » , Phys. Chem. Chem. Phys. , vol. 5, 2003, P. 1103 ( DOI 10.1039 / b212460m )
- (a) J Holloway, " nemesgáz fluoridok " , J. Fluor. Chem. , vol. 33, 1986, P. 149. ( DOI 10.1016 / S0022-1139 (00) 85275-6 )
- (a) VV Avrorin, RN Krasikova, VD Nefedov Toropova és MA, " The Chemistry of Radon " , Russ. Chem. Fordulat. , vol. 51, n o 1, 1982, P. 12–20 ( DOI 10.1070 / RC1982v051n01ABEH002787 )
- (in) Gulzari L. Malli, " A radon-karbonil létezésének előrejelzése: OPUAR " , Int. J. Quantum Chem. , vol. 90, 2002, P. 611 ( DOI 10.1002 / kb. 963 )
- (en) Nino Runeberg " Relativisztikus pszeudopotenciális számítások mi Xe 2 , RnXe és Rn 2: A radon van der Waals tulajdonságai ” , Int. J. Quantum Chem. , vol. 66,1998, P. 131 ( DOI 10.1002 / (SICI) 1097-461X (1998) 66: 2 <131 :: AID-QUA4> 3.0.CO; 2-W )
- (in) AV Grosse, " A 118. elem (Eka-Em) és a 86. tétel (Em) néhány fizikai és kémiai tulajdonsága " , Journal of Inorganic and Nuclear Chemistry , Elsevier Science Ltd., vol. 27, n o 3, 1965, P. 509-19 ( DOI 10.1016 / 0022-1902 (65) 80255-X )
- (a) Clinton S. Nash, " atomi és molekuláris tulajdonságai Elements 112, 114, és 118 " , J. Phys. Chem. A , vol. 109, n o 15, 2005, P. 3493–3500 ( DOI 10.1021 / JP050736o )
- (in) Han Young-Kyu Bae Cheolbeom, Son Sang-Kil és Lee Yoon Sup, " Spin-pálya hatások a transzaktinid elem p-blokk elem monohidrid MH-jára (M = 113-118 elem) " , J. Chem. Phys. , vol. 112, n o 6, 2000. február 8( DOI 10.1063 / 1.480842 )
- (a) Han Young-Kyu és Lee Yoon Sup, " Structures of RgFn (Rg = Xe, Rn, és Element 118. n = 2, 4) Számított által Két komponens spin-pálya Methods. A spin-pálya Induced izomer a (118) F 4 » , J. Phys. Chem. A , vol. 103, N o 8,1999. február 9, P. 1104–1108 ( DOI 10.1021 / jp983665k )
- (in) Uzi Kaldor és Stephen Wilson, Elméleti Chemistry and Physics a nehéz és a szupernehéz elemeket , Dordrecht, Springer, 2003, 565 p. ( ISBN 978-1-4020-1371-3 , LCCN 2003058219 , online olvasás ) , p. 105
- (in) Saunders, HA-Vázquez Jiménez, RJ Cross és RJ Poreda, " A hélium és a neon stabil vegyületei. He @ C60 and Ne @ C60 ” , Science , vol. 259, 1993, P. 1428-1430 ( PMID 17.801.275 , DOI 10,1126 / science.259.5100.1428 )
- (a) Martin Saunders, Hugo A. Jimenez-Vazquez R. James Kereszt , Stanley Mroczkowski, Michael L. Gross, Daryl E. Giblin és Robert J. Poreda, " Incorporation hélium, neon, argon, kripton, és a xenon a fullerének nagy nyomáson ” , J. Am. Chem. Soc. , vol. 116, N o 5, 1994, P. 2193–2194 ( DOI 10.1021 / ja00084a089 )
