Mellrák
Mellrák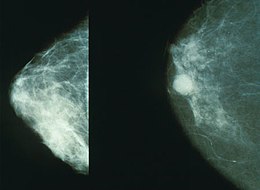 Mammogram mutatja a mellrákot a jobb oldalon.
Mammogram mutatja a mellrákot a jobb oldalon.
| Különlegesség | Onkológia |
|---|
A mellrák egy rosszindulatú daganat az emlőmirigy . Más szóval, ez egy rák , hogy indul cellaegységeinek amelynek feladata a titkos, a tej, a ducto-lebenykés egységek a mell , elsősorban a nők . Tízből 8 emlőrák 50 éves kor után jelentkezik.
Az első rák a világon, 2016-ban évente 1,8 millió nőt érint világszerte, köztük 50 000 nőt Franciaországban. Várhatóan minden nyolcadik nőnél emlőrákot diagnosztizálnak életében. Az emlőrák kezelése az évek során drámai módon javult, és több remisszióhoz vezetett.
Ezeknek a rákoknak 5-10% -a örökletes genetikai eredetű ; Az esetek 85-90% -a (úgynevezett szórványos vagy nem örökletes forma ) környezeti vagy ismeretlen eredetű. A szórványos emlőrák jelentős részét hormonok, ösztrogén és progeszteron fogamzásgátlókban történő bevétele vagy a menopauza elleni kezelések indukálják. A kockázati tényezők az alkohol , a cukor, a tejtermékek, a hidrogénezett zsírok , az elhízás , a fizikai aktivitás hiánya is. A késői első terhesség és a szoptatás hiánya szintén elősegíti ezt a rákot.
A kezelés a protokollok szerint sebészeti beavatkozást, sugárterápiát, kemoterápiát igényel, ezek kombinációja kiegészíthető hormonterápiával.
Járványtan
A kockázat jelentősen megnő a 30 és 60 év közötti életkorral; akkor 60 és 80 év között homogén; a diagnózis átlagos életkora 61 év.
Vannak bizonyos hajlamosító genetikai tényezők, valamint hormonális tényezők.
Meg kell jegyezni, hogy az incidencia jelentősen (alig 9% -kal) csökkent az Egyesült Államokban 2003 óta és Franciaországban is, ami a menopauza hormonpótló terápiájának alacsonyabb alkalmazásának felelne meg .
A 2002 , közel 1,1 millió új esetet vizsgáltak meg, több mint 400.000 emlőrák okozta halálozások. Úgy tűnik, hogy az incidencia folyamatosan növekszik, 2010-ben több mint 1,6 millió új eset és 425 000 haláleset következett be. Közel négymillió nőnél alakul ki mellrák . Azemlőrákban végződő szövettani vizsgálatok gyakoriságamindenekelőtt a szűrés intenzitásától függ (lásd a túldiagnosztikát ). A halálozás az 1990-es évek óta jelentősen csökkent a fejlett országokban. Más országokban tovább növekszik.
Mellrák Franciaországban
A France országok között, ahol az emlőrák előfordulása igen magas szerte a világon, és ha az előfordulási aránya az emlőrák gyorsabban növekedett (2,4 százalékkal 100 000 nő évente) időszakban 1980-2005, egy csepp ebben az arányban 2000 és 2005 között (+2,1 / 100 000 nő évente).
- Az emlőrák a 2000-es években évente körülbelül 11 000 halálesetet okozott, a halálozás stabil (2005-ben 11 201 haláleset).
- Franciaországban minden nyolcadik nőt érint az emlőrák.
- A nőknél az összes új rákos megbetegedésből minden harmadik új rákos eset több mint egy (2008-ban 36,7%).
- A 2000-es években évente körülbelül 50 000 új emlőrákot diagnosztizáltak.
- A 2005 , ez a szám 49.814, ami megfelel az egyik legmagasabb előfordulási arány Európában. Ez az arány Franciaországban átlagosan 2,4% -kal nőtt 25 éven át (1980-tól 2005-ig).
- Az emlőrák kevesebb mint 10% -a fordul elő 40 éves kor előtt, 25% -a 50 éves kor előtt, majdnem fele 65 éves kor előtt.
- A nők csaknem 10% -ánál emlőrák alakul ki. A feltárt új esetek 75% -a 50 év feletti nőket érint, és ez a szám folyamatosan növekszik: 1995-ben 35 000, 2001- ben 42 000 .
Ez a rák egyike annak a három ráknak, amelyek esetében a túlélés nőtt, mióta a túlélési arány 80% -ról 87% -ra emelkedett a 2000-es évek elején, a Francim hálózat Közegészségügyi Felügyeleti Intézetének közös jelentése szerint. a Nemzeti Rákkutató Intézet és a lyoni kórházak.
Mellrák Kelet-Ázsiában
Mellrák KínábanKínában a nők körében az emlőrák a leggyakoribb és a rákos megbetegedések legfőbb oka. Az emlőrák halálozása az elmúlt években nőtt. A második és harmadik kínai nemzeti retrospektív halálok-felmérés adatai szerint az emlőrák mortalitása 1990-1992 és 2004-2005 között 3,84 / 100 000 lakosról 5,09 / 100 000 lakosra növekedett. 2008-ban körülbelül 169 000 új emlőrákos esetet diagnosztizáltak, és ez volt a leggyakrabban diagnosztizált ráktípus a kínai nőknél. Ugyanebben az évben az emlőrák halálozása 10000 lakosra számítva 5,7 volt, ami körülbelül 44 900 halálesetet eredményezett.
Mellrák JapánbanEgy 2009-ben publikált tanulmány szerint Japánban az emlőrák előfordulása történelmileg sokkal alacsonyabb, mint a nyugati országokban; 1998-2002 között Oszakában 32,0 / 100 000 nő aránya van, ami Hawaii-on 105,6 / 100 000 kaukázusi nőre és 107,5 / 100 000 japán nőre vonatkozik. A szerző megjegyzi, hogy Japánban nagyobb a szójaételek fogyasztása, mint a nyugati országokban, és ennek az országban a mellrák arányára gyakorolt hatását.
Rizikó faktorok
Sporadikus (nem családi) rákok
A diagnosztizált emlőrák 5-10% -a genetikailag hajlamos emlőrák. A nem családi daganatok alkotják a fennmaradó 90-95% -ot. Ezek harmadát a nyugati országokban megakadályozhatja az életmód megváltoztatása.
Lehetséges mechanizmusokÚgy tűnik, hogy sok molekula vagy molekula koktél kiválthatja vagy elősegítheti az emlőrákot; az érintett mechanizmusokról:
- Az emlődaganatok felében szerepet játszhat a DNS- károsodási reakció gátlása , különösen azokban, amelyeket a menopauza hormonális kezelésére használt hormonok indítanak vagy segítenek elő.
- A sporadikus emlőrákok 50% -ában fehérje ( Akt1 ) túlexpresszálódik . Ezért hajlamos lehet emlőrákra és / vagy részt vehet más folyamatokban (környezeti és nem genetikai). Aktiválása Akt1 hatékony gátlását eredményezi által megkötés a BRCA1 fehérje a citoplazmában ; ha azonban ez a fehérje már nem képes behatolni és keringeni a magban, akkor a DNS már nem javul meg (mint például sok örökletes rák esetében a BRCA1 gén hiányában). Az AKT1-et aktiválják azok a hormonok is, amelyek gyaníthatóan emlőrákot okoznak (krónikusan a nőknél hosszú ösztrogén alapú hormonterápiát folytatnak). Ebben az esetben a nem mutált BRCA1 gén megszakadhat, ami megnövekedett emlőrák kockázatát eredményezheti.
- Hasonlóképpen egy másik fehérje; Úgy tűnik, hogy a „ CK2 protein kináz ” ( a hámsejtek plaszticitása szempontjából fontos enzim ) részt vesz ezen rákok előrehaladásában; e fehérje aktivitásának megváltozása az epithelsejtek ráksejtekké (mobilabbá és áttétforrássá) történő átalakulásával jár. Ez a fehérje általában úgy tűnik, hogy megakadályozza az „ epithelialis- mezenhimális átmenet ” nevű sejtmechanizmust (EMT; az epitheliális sejtek mezenhimális állapotúvá válásának és mobilitásának folyamata, amelyet bizonyos rákellenes gyógyszerekkel szembeni rezisztencia kísér ). Ez az enzim két elemet ötvöz; egy „katalitikus alegység” (CK2α) és egy „szabályozó alegység” (CK2β). Úgy tűnik, hogy a CK2β alegység diszfunkciója, amely lehetővé teszi az EMT-t, részt vesz az ilyen típusú rák metasztázisainak termelésében.
Az emlőrák gyakran hormonfüggő rák: az ösztrogénszintet növelő tényezők tehát veszélyeztetettek. Alapvetően az emlőrák kockázata növekszik a menstruációs ciklusok számával, legyen az mesterséges ( ösztrogén-progesztogén tabletta ) vagy természetes.
A menopauza hormonpótló terápiája jelentősen növeli az emlőrák kialakulásának kockázatát.
A késői menopauza és a koraérett pubertás a menstruációs ciklusok számának és ezáltal az ösztrogénszint növelésével jár. A koraérett pubertás tényezői a következők: gyermekkori elhízás , fokozott állati fehérjék (hús, tej ) fogyasztása, cukros italok fogyasztása, endokrin rendszert károsító anyagok expozíciója .
Nem termékenység vagy késői termékenységAzoknak a nőknek, akiknek még nem volt gyermekük, vagy akiknek első terhességük későn (30 éves kor után) volt, jelentősen nagyobb az emlőrák kialakulásának kockázata, mint azoknál, akiknek legalább egy gyermekük volt 30 éves kor előtt. Valójában az első terhességet megelőző ciklusok tűnnek a legveszélyesebbnek a mell számára. A terhesség megvédi az emlőt azáltal, hogy a mellsejteket nagyobb differenciálódás irányába változtatja. A differenciált sejtek kevésbé érzékenyek a rákkeltő anyagokra, különösen a hormonális sejtekre. A terhesség ezért oltóanyagként hat az ösztrogén ellen. Minél korábban jelentkezik ez az első terhesség, annál jobban működik.
Szennyező anyagok és más endokrin rendellenességekAz Endokrin Társaság nemzetközi szakértők által írt nyilatkozatában kiemeli az emlőrák előfordulásának az elmúlt 50 évben történő növekedése és az endokrin rendszert károsító anyagok, az ösztrogén vagy ösztrogén hatású szintetikus vegyi anyagok elterjedése közötti párhuzamosságot . Ezek a számtalan termék (a legismertebbek a DES , DDT , a biszfenol A és a dioxinok ), különféle forrásokból ( peszticidek , ipari vegyszerek, műanyagok és lágyítók , üzemanyagok és egyéb, a környezetben mindenütt jelenlévő vegyszerek) az endokrinológusok számára komoly aggodalomra adnak okot. . Így azok a lányok, akik az 1960-as években a méhben nagy mértékben ki voltak téve a DDT- nek, négyszeres kockázatot jelentenek az emlőrákban egy 2015 közepén közzétett tanulmány szerint. Az étel nagy szerepet játszik.
Az Endokrin Társaság számos ajánlást ad ki, amelyek célja
- az endokrin rendszert károsítók hatásainak jobb megértése (többek között alapkutatások és klinikai vizsgálatok révén);
- hivatkozhat az elővigyázatosság elvére ;
- támogassák az egyéni és a tanult társadalmak részvételét a probléma nyilvánosságra hozatala érdekében;
- jogszabályi változtatásokat kell végrehajtani.
Rosszul felfogott okokból az elhízás növeli az emlőrák kockázatát, különös tekintettel e rák gyors elterjedésére. Ezt bizonyították in vivo , valamint in vitro ; így amikor a daganatsejteket ( egér vagy ember) érett adipocitákkal együtt tenyésztik, az utóbbiak növelik a rák invazív kapacitását. Az elhízás általában megduplázza az emlőrák kockázatát.
Az elhízás a zsírszövet mennyiségének növelésével növeli az ösztrogén szintjét a vérben az aromatáz nevű enzim aktiválásával . Ez tulajdonképpen áttértek androgén típusú hormonok a ösztrogén . Ez a menopauza után is folytatódik ; Egy tanulmány kimutatta az emlődaganat kockázatának növekedését a posztmenopauzás nőknél súlygyarapodásuk alapján.
A rákos sejtekkel tenyésztett adipociták módosított fenotípust mutatnak a zsírtalanítás szempontjából, és a kóros aktivációval járó adipociták markereinek csökkenése jellemzi a proteázok , különösen a metalloproteináz -11, és a gyulladáscsökkentő citokinek ( interleukin-6 (IL-6 ) vagy IL-1β.
Ezzel szemben az emlőrák daganatos sejtjei módosítják az emlő zsírsejtjeit ( adipocitáit ). Ez utóbbiak különösen gyulladáscsökkentő tényezőket választanak ki, köztük az interleukin 6-ot (amely in vitro elegendő önmagában a rákos sejtek metasztázisát okozza ) Ez megmagyarázhatja, hogy az elhízás miért növeli a metasztázis és a rák gyors terjedésének kockázatát. Meg kell még értenünk a rákos sejtek és az adipociták közötti párbeszéd meghatározóit, és a nagyobb daganatok és / vagy a járulékos nyirokcsomók bevonásával magasabb az IL-6 szint a környező daganatban t adipociták.
A peritumorális adipociták módosított fenotípust és biológiai jellemzőket mutatnak, amelyek elég specifikusak ahhoz, hogy rákhoz társult adipocitáknak (vagy CAA- rákhoz kapcsolódó adipocitáknak ) lehessen nevezni .
Az állati zsírok, valamint a transz-zsírsavak fogyasztása (amelyek az élelmiszeriparban számos készítmény összetételének részét képezik) kockázati tényezőknek bizonyultak. Ez a kapcsolat az elfogyasztott állati zsír szintje és az emlőrák között régóta ismert. A többszörösen telítetlen lipidek hatása kevésbé nyilvánvaló
Egy tanulmány (Inserm-Gustave-Roussy, 1995-1998) kimutatta, hogy az emlőrák kockázata közel 50% -kal nő azoknál a nőknél, akiknél magas a transz-zsírsavszint , olyan termékek, amelyek jelen lehetnek feldolgozott élelmiszerekben, például ipari kenyerekben és sütik, sütemények, sütemények, chipsek, pizzatészta.
TejtermékekSzámos tudományos tanulmány megtartja a tejet a hormonfüggő rákok, például a prosztata, a petefészek és az emlő rizikófaktoraként. A megnövekedett kockázat a vér IGF-1 szintjének növekedésével függ össze, amely maga szorosan összefügg a tej fogyasztásával. A kapcsolat tehát a menopauza előtti szakaszban megalapozottnak tűnik, és összhangban áll a Laron-szindrómában érintett populációban megfigyelt rák hiányával is , amely nem termeli az IGF-1-et . Az IGF-1 koncentráció a tej fajtájától függően (tehén, kecske, juh stb.), Ha könnyű, vagy a kérődzők tenyésztési módszerétől ( szarvasmarha szomatotropin ) függően . Más vizsgálatok azonban inkább a D-vitamin és / vagy a kalcium tejtartalmához kapcsolódó védő szerepet hoznak létre.
Alkohol- és dohányfogyasztásAz emlőrák megnövekedett kockázata és gyakorisága legalább részben a nők alkoholfogyasztásának növekedésével függ össze ;
- Számos tanulmány kimutatta, hogy az alkohol fogyasztása (bármi legyen is az; bor , sör vagy kemény ital ) növeli az emlőrák kockázatát. Ezt a kockázatot átlagosan 30% -kal növeli napi három pohár alkohol. A metaanalízisek megerősítették az alkohol szerepét az emlőrák kialakulásában vagy elősegítésében. Egy tanulmány szerint ezt a kockázatot túlbecsülték, de megcáfolták egy metaanalízissel, amely 98 esetkontrollon és prospektív tanulmányon alapult.
- A kockázat körülbelül 10% -kal nő 10 g további, átlagosan naponta elfogyasztott alkohol után, az egyéntől függően eltérő genetikai érzékenységgel, bizonyos más rákkeltő kockázati tényezőknek kitett alcsoportok is érzékenyebbek rá. Ezt a kockázatot súlyosbítják más tényezők: 50 év felettiek, posztmenopauzális szakaszban vannak, jóindulatú emlőbetegség, ösztrogénreceptorokat tartalmazó daganat és / vagy előrehaladott / invazív daganatok befolyásolják.
- Ez a kockázat megduplázódik a krónikus alkoholfogyasztással ( normál testtömeg-indexű nőknél (BMI <25), míg az elhízás egy másik gyakran említett tényező).
- Az alkohol, mint rákkeltő faktor vagy kofaktor következményei a mellre meglehetősen gyorsak lehetnek, mert a statisztikák azt mutatják, hogy a közelmúltbeli fogyasztás hatása jelentősebb, mint a régi fogyasztásé.
Összefüggés van a dohányzás és a rák előfordulása között.
D-vitamin hiányaA D-vitamin és gyógyászati analógjai anti-proliferatív és pro-differenciáló hatásúak. Ezért fontos a rák megelőzésében és kezelésében általában. Különösen korlátozhatja az ösztrogén túlzott termelését az aromatáz hatására .
Az emlőrák gyakran társul alacsony D-vitamin-szinttel (hiány vagy elégtelenség az esetek 78% -ában 145 beteg vizsgálata szerint). Az afrikai amerikaiak túlzott halálozása a rákban (beleértve az emlőrákot is) a bőr pigmentációjának tulajdonítható, amely ezen a szélességi fokon a szükségesnél több ultraibolya sugarat blokkol, és jelentősen akadályozza a D-vitamin termelését. A közel 68 000 nő 10 év alatt történt evolúciójának francia tanulmánya megerősítette a D-vitamin-hiány és az emlőrák kialakulása közötti kapcsolat fontosságát. Ezeknek a nőknek az UV- expozíciós indexének elemzése kimutatta, hogy csak azok, akik az UV sugárzásnak voltak leginkább kitéve, elegendő védelmet nyújtottak az emlőrák ellen az élelmiszer-bevitel érdekében, hogy mérhető hatásuk legyen; az összes többi esetében az INSERM csapata arra a következtetésre jut, hogy minél északabbra él, annál nehezebb elérni ezt a D-vitamin küszöböt, amely véd az emlőrák ellen.
Homályos kifejezés a mell bármely betegségére. Általában a jóindulatú rendellenességek számára van fenntartva, amelyek összetéveszthetnek egy daganattal, és ez indokolja a mintát ( biopszia ) annak pontos azonosításához. Néhányan elősegíthetik a későbbi rák kialakulását, és rendszeres megfigyelést indokolhatnak .
A mammográfia sűrű megjelenése, különösen ha kiterjedt, jelentősen növelné az emlőrák kialakulásának kockázatát.
EgyébTörténelmileg olyan nőknél találták, akik sok fluoroszkópián estek át, amikor a tüdő tuberkulózis nagyon gyakori volt. Ezt a kockázatot olyan japán nőknél is észlelték, akiket Hirosimában vagy Nagaszakiban végzett nukleáris robbanások során nem halálos dózisokkal besugároztak . Ez lényegében a mellkas sugárterápiájának XXI . Századi kezdete bizonyos rákos megbetegedések - különösen Hodgkin-kór - kezelésében fiatal nőknél, akiknél az emlőrák kockázata jelentősen megnő. A radiológiai vizsgálatok bizonyos új módozatai, például a koszorúér-CT , elegendő besugárzást eredményezhetnek az emlőrák kockázatának növelése érdekében évtizedekkel a vizsgálat elvégzése után.
Az éjszakai munka növelheti az emlőrák kockázatát. Ezt a kockázatot Dániában törvényesen elismerték, és pénzügyi ellentételezés tárgyát képezi.
A szoptatás védelmet nyújt az emlőrák ellen, különösen a petefészkek elaltatásával és a ciklusok számának csökkentésével.
A terhesség megszakítása nem növeli az emlőrák kockázatát
A gazdag országokban (máshol nem végeztek tanulmányokat erről a kérdésről) az átlagosnál magasabb születési magasság korrelál az emlőrák kialakulásának jövőbeli kockázatával. A növekedésben szerepet játszó egyes hormonok magzati expozíciója érintett lehet (meg kell erősíteni). A fejlett országokban született nők emlőrákjának 5% -át közvetlenül érinti.
A férfiaknálAz emlőrák 1% -át egy férfi fejleszti. Ugyanabban a szakaszban a prognózis azonos. Ennek ellenére a férfiak emlőmirigye nagyon kicsi, a diagnózis gyakran késik, ezért sokkal több rákot észlelnek előrehaladott stádiumban, bőrrészesedéssel vagy mélysíkokkal együtt (T4). Az emlőrák megfertőződésének kockázata nő azoknál a férfiaknál, akiknek családtörténetében emlőrák van, különösen akkor, ha mutáció van a BRCA1 és BRCA2 génekben.
Családi rákok
A diagnosztizált emlőrák 5-10% -a genetikai hajlamú emlőrák, azaz évente 2000 és 4000 között érintett ember, 550-1000 haláleset Franciaországban. 2008-ban tíz gén társult az emlőrák fokozott kockázatával. Kilenc kapcsolódik a DNS károsító reakció rendszeréhez. A tizedik egy olyan fehérjét kódol, amely gátolja az AKT1 enzim (egy olyan enzim, amelynek gátlása szerepet játszik a nem genetikai rákos megbetegedésekben is) működését. A tíz gén közül kettő (az úgynevezett BRCA1 és BRCA2) egyedül felelős ezen genetikailag hajlamos daganatok feléért, vagy az összes emlőrák 2,5-5% -áért.
JellemzőkLeggyakrabban ez a típusú emlőrák egy nőnél jelentkezik, különösebb egészségügyi probléma nélkül. Nagyon ritkán a nő egy ismert genetikai betegség hordozója.
Számos jel sugallhatja az emlőrák genetikai hajlamát :
- Fiatal életkor (nem fertőző formában 60 év helyett átlagosan 43 év);
- Az emlőrák családtörténete;
- A mindkét mellben előforduló rák egymás után vagy egyidejűleg;
- A második rák megjelenése a petefészekben ;
- Medulláris szövettani típusú rák.
Autoszomális domináns típusú . Egy nőnél a gén egyetlen mutációjának jelenléte 80% -os kockázatot jelent az emlőrák kialakulására (mutáció hiányában 10% helyett).
A kóros génnel rendelkező családból származó nők kockázata attól függ, hogy örökölték-e vagy sem. Ha az öröklött gén nem abnormális, akkor a kockázat megegyezik a többi nő kockázatával; ha a gén mutálódik, akkor 70-80% esélyük van az emlőrák kialakulására. A probléma hasonló a petefészek- vagy vastagbélrák kockázataival kapcsolatban . Egyes családokban ezek a rákos megbetegedések megfigyelhetők a közvetlen vonalon (nagymama, anya, lánya) vagy közeli rokonoknál (néni, nővér, első unokatestvér). Ezek a rákok általában életük első részében fordulnak elő.
Egy genetikai teszt kiemelheti ezt a kockázatot, de a mutált gén tesztje csak akkor biztos, ha pozitív (ebben az esetben minden rokonot nyomon kell követni). Ezt a nagyon speciális cselekményt csak azoknál a családoknál kell kérni, akiknek felesége valószínűleg veszélyeztetett öröklődést mutat, amelyet onkogenetikai konzultáció bizonyít, amely megállapítja e család genealógiai fáját .
Gének érintettektöbb gént azonosítanak, de a két fő:
- BRCA1 a 17. kromoszómán . Már több mint 500 mutációt vagy szekvenciaváltozatot írtak le.
- BRCA2 a 13. kromoszómán . Több mint 100 különböző mutációt számoltak meg.
Ezen mutációknak csak egy része növeli a rák kockázati tényezőjét. A mutációk a BRCA2 (1 1460) találhatók gyakrabban, mint mutációk BRCA1 (1 1960-ban). Ezek a mutációk a mellrák túlzott kockázatán túl a petefészekrák kockázatának túlzott mértékét is előidézik.
Az emlőrák kialakulásának valószínűsége egy BRCA1 mutáció hordozójában körülbelül 65% 70 éves kor előtt (45% a BRCA2 mutáció hordozói esetében ).
A BRCA1 mutációkat hordozó rákos megbetegedések kialakulása még mindig rosszul ismert: egyesek szerint súlyosbodik, mások szerint hasonló súlyosságú a BRCA2 mutációk hordozói vagy a mutációk nem hordozói esetében.
Ezeknek a mutációknak a gyakorisága továbbra is alacsony az emlőrákos betegeknél (kevesebb mint 4% a BRCA1 esetében , bár ez az askenázi zsidóknál kétszerese).
A többi érintett gén a PALB2, amely részt vesz a BRCA2 , ATM , CHEK2 , RAD51C , BARD1 vagy TP53 stabilizálásában .
Genetikai tanácsadásEgyes országokban minden nő, aki erre vágyik, részesülhet genetikai tanácsadásból az örökletes rák kockázatának meghatározásában. Ha a genetikai hajlam valószínűsége meghaladja a 25% -ot, ezeknek a betegeknek molekuláris diagnózist kínálnak. Ez a molekuláris kutatás különösen prediktív, ha ismerjük a mutációt egy már emlőrákban szenvedő, genetikai hajlamú szülőnél.
A magas kockázatú nők felügyeleteA genetikai hajlam vagy mutációt hordozó nőket 20 éves kortól 6 havonta, 30 éves kortól éves mammográfiával figyelik a klinikai megfigyelő csoportok . A kockázatnövelő tényezők között szerepel a ductalis carcinoma in situ , amelyet rák előtti formának tekintenek, és az in situ lobularis carcinoma , amely enyhébb, de az azonosított esetek 20-30% -ában rákká alakulhat.
Szűrés
A daganatok kimutatása és kezelése nagyon kicsi (átmérőjüknél kevesebb, mint egy centiméter) lehetséges a mammográfiának és a rendszeres ellenőrzésnek köszönhetően . Ez csökkenti a mortalitás kockázatát , és lehetővé teszi a kemoterápiánál kevésbé nehéz és kevésbé traumatikus kezeléseket , a „megcsonkító” műtétet (abláció). A nők 50 és 74 év között vannak leginkább kitéve az ilyen típusú ráknak. A kétévenkénti mammográfia lehetővé teszi a hatékony szűrést, de ez felveti a téves pozitív diagnózisnak megfelelő túldiagnózis kockázatát : a nő akkor tekinthető mellrákosnak, amikor még nincs, így indokolatlan kezelésnek teszi ki, minden mellékhatással és kockázattal együtt amelyek következnek. A szűrés előnyeit ezért gondosan dokumentálni kell. Egy 2003 - as metaanalízis szerint egyes esetekben a szűrési mortalitás jelentős csökkenése kimutatható; ugyanakkor ugyanaz a metaanalízis két másik versengő tanulmányról számolt be, amelyek nem mutatnak szignifikáns csökkenést. A kockázatcsökkentés ezen létezését azonban bírálják.
Franciaországban egy tanszéki vagy részlegek közötti irányítási struktúra minden 50–75 éves nőt kétévente meghív egy ingyenes mammográfiára (a társadalombiztosítás 100% -os pénzügyi támogatásával). A meghívót a háziorvos , a nőgyógyász vagy maga a nő kérésére lehet elküldeni . A látogatást akkreditált radiológushoz, az osztályok szintjén felállított , szűrővizsgálatokra szakosodott hálózat tagjához kell megtenni . Ez a stratégia különösen az Országos Egészségügyi Értékelési és Akkreditációs Ügynökség Technológiai Értékelési Osztálya által 2001–2-ben készített szakértői jelentésre épül. A jelentés kitűzött célja emlékeztetett a hatályos francia ajánlásokra. A jelentés arra a következtetésre jutott, hogy mivel a mammográfiás szűrés hatástalansága nem bizonyított, fenn kell tartani az emlőrák szűrésére alkalmazott ajánlásokat.
A mammográfiával társított ultrahang segítségével nagyobb számú rákot lehet kimutatni, de nagyobb számú hamis pozitív eredményt (biopszia érvényteleníti a rák diagnózisát). Ezért a vizsgálat helye a szűrési stratégiában még értékelendő.
A mágneses rezonancia képalkotás (MRI) szintén ígéretes teszt lenne, nagyobb érzékenységgel, mint a mammográfia.
Self - vizsgálat nagyon népszerű volt szűrési technikát az 1980-as és 1990-es, ami még mindig ajánlott, de nem bizonyított, hogy hatékony legyen.
Az infravörös termográfia használata detektálás céljából kevesebb mellékhatással (sugárzás nélkül), jobb érzékenységgel , kevesebb hamis pozitív eredménnyel és korábbi kimutatással végzett vizsgálat, mint a mammográfia. A termográfia költségei szintén lényegesen alacsonyabbak lennének, mint a mammográfiás szűrés költségei, amelynek éves költségvetése 250 millió euró. 2017-ben azonban a termográfiát alig használták Franciaországban. A technika egy hír segítségével mutatta meg egyszerűségét.
75 év után nem bizonyított a szisztematikus szűrés előnye. 70–75 éves kora között gyengének tűnik. 50 éves kor előtt az érdeklődés kétséges, a halálozás bizonyított csökkenése nélkül.
Túl diagnózis
Mielőtt menopauza , szisztematikus szűrés nem bizonyított hatásos, mivel a minimális gyanús rendellenességek gyakori. Úgy tűnik, hogy a hátrányok ebben az esetben meghaladják az előnyöket, kivéve a veszélyeztetett nőket.
A szisztematikus szűrés kockázata a helytelen diagnózis felállítása, és indokolatlan kezeléshez vezet, ennek költsége és kockázata. Ezt nevezzük túldiagnózisnak . Az emlőrákban a mammográfia jelentős mértékű túl diagnózishoz vezethet. Ez az arány tízből egybe, négybe, vagy akár kettőbe is terjedhet. A megmentett életek és a túldiagnózisban szenvedő nők száma aránya (részben tükrözi a vizsgálat haszon / kockázat arányát) 1: 2-től 1-ig 10-ig változhat.
E túldiagnózisok magyarázata nem egyértelmű: a dokumentumok téves értelmezése, nagyon lassú evolúciójú rákok vagy akár egyes rosszindulatú daganatok spontán regressziója.
A Francia Közegészségügyi Felügyeleti Intézet krónikus betegségek osztálya szerint azonban ezeknek az elemzéseknek a jövőben lehetővé kell tenniük a szűrés még hatékonyabbá tételét annak érdekében, hogy azonosítsák azokat a rákos megbetegedéseket, amelyek a látens maradókból alakulnak ki, megkérdőjelezés nélkül. maga a szűrés előnye.
Sűrű mell
Sűrű vagy rendkívül sűrű mell esetén a mammográfia hatástalan lehet a rák kimutatására. Tanulmányok kimutatták, hogy a sűrű mellű nők esetében a mammográfiák nem találnak rákot az esetek csaknem egyharmadánál vagy felénél .
A sűrű mellszövet mammográfiával megzavarja a rák megtalálásának képességét. Felhőként viselkedve a sűrű mellszövet fehér, és elfedheti a rákot, amely szintén fehérnek tűnik.
Az emlő sűrűsége a BI-RADS segítségével mérhető 1-4 pontozási rendszer alkalmazásával. Ez a rendszer lehetővé teszi a radiológusok számára, hogy mérjék és leírják a mell sűrűségét
BI-RADS 1: Sűrű mellszövet <25% BI-RADS 2: Sűrű mellszövet 26 és 50% között BI-RADS 3: Sűrű mellszövet 51 és 75% között BI-RADS 4: Sűrű mellszövet> 75%
Az Egyesült Államokban a nők csaknem felének sűrű a melle. Egyes államokban a radiológusoknak törvényi kötelességük, hogy a nők számára biztosítsák a mell sűrűségét, hogy megalapozott beszélgetést folytathassanak egészségügyi csoportjukkal arról, hogy milyen további vizsgálatokra lehet szükségük.
Öt tény a mell sűrű szövetéről:
. A nők 40% -ának sűrű a melle. . az emlősűrűség a mammográfia hatástalanságának egyik legmegbízhatóbb előrejelzője a meglévő rák kimutatásában. . a mammográfia a vizsgálatok szerint az esetek egyharmadában és felében nem észlel meglévő rákot sűrű mell esetén. . Az emlő sűrűsége az emlőrák kockázatának megalapozott előrejelzője. . a magas mellsűrűség magasabb kockázati tényező, mint két elsődleges rokon mellrákban.
A mammográfiával kombinált ultrahang segítségével nagyobb számú rákot lehet kimutatni a sűrű és a hiper sűrű mellnél. Ultrahangon néhány emlőrák fekete színűnek tűnik, ezért kimutatható. A mell ultrahangja önmagában nem elegendő az emlőrák szűrésére.
A vizsgálat egy másik típusa az MRI.
Egy másik típusú elemzés alakult ki az Egyesült Államokban a mammográfiák hatástalanságának leküzdésére a sűrű mellek rákszűrésére. A mellmolekuláris képalkotás (MBI) rendkívül hatékony másodlagos diagnosztikai eszköz .
Még akkor is, ha a sűrű mellű nőknél a mammográfia eredménye negatív (vagy akiket az emlőrák nagy kockázatának tartanak), további MBI-vizsgálatokat kell fontolóra venni.
Az MBI kép a szövetek aktív molekuláris funkcionális elemzését jelenti a vénákba injektált rádiójelző felvétele miatt. Ezeken a képeken egészséges, sűrű vagy nem sűrű szövet jelenik meg fekete színben, a beteg szövet fehér színű, a rádiójelző aljzatában található gammasugarak gyorsabb felszívódása miatt.
Diagnosztikai
Klinikai
Az első tapintás a mell tapintása. Anatómiai elhelyezkedésük miatt a melle könnyen érezhető, különösen közepes vagy kicsi. Javasoljuk, hogy a betegek ezt a tesztet rutinszerűen végezzék el a menstruáció végén.
A tapintás során a gyanú egy csomó felfedezéséből adódik , amely körülbelül 1 cm átmérőjű tapintással detektálható . A szabálytalanság nem biztos, hogy fájdalmas, de a közelmúltbeli rendellenességeknek különösen fel kell hívniuk a beteg és orvosának figyelmét.
A szabálytalanságok közül a beteg egyedül figyelheti:
- egy gödröcske vagy egy ránc, amely a mell felületét üregeli, „narancshéj” megjelenéssel;
- a mellbimbó deformációja, befelé behúzva;
- a mellbimbó ekcémás megjelenése, amely vörössé, kérgesé vagy erodálttá válik;
- mellbimbó váladék, különösen, ha véres vagy feketés.
Ezen jelek egyikének megfigyelésével nagyon gyorsan orvosi konzultációhoz kell vezetni. Azt azonban, hogy mely további vizsgálatokra van szükség, csak az orvos tudja megítélni, mert ezek a jelek nem csak rákos megbetegedések esetén találhatók meg. A góc jóindulatú lehet:
- ha szilárd állagú, akkor az emlőmirigyben kialakult adenofibroma lehet . Ez egy speciális bakteriális környezet miatt alakulhat ki, amely később adenokarcinómává válhat, vagy nem .
- ha folyékony természetű, akkor ciszta lehet .
Mamográfia
Az orvos dönthet úgy, hogy első diagnózisát mammográfiával erősíti meg . Az ultrahang egy kiegészítő vizsga, amely segíthet megtalálni a hibát az eltávolítás megkönnyítése érdekében, vagy felismerni, hogy folyadékkal töltött ciszta-e, de soha nem pótolhatja a mammogramot. A rendszeresen végzett szűrővizsgálatok részeként végzett mammográfiával kellően korai stádiumban diagnosztizálható a betegség, hogy a kezelés a lehető legkonzervatívabb és ugyanakkor hatékony legyen. Valójában, amíg a daganat mérete kisebb, mint 1-2 cm, a gyógyulás esélye megközelíti a 100% -ot.
A diagnózis megerősítése
Ha az összes vizsgálat még mindig nem teszi lehetővé a jó diagnózis biztosítását, és ha kétségei továbbra is fennállnak, akkor meg kell vizsgálni azt a mintát, amelyet kórházi kezelés nélkül leggyakrabban egy nagy tűvel (trocar) vettek helyi érzéstelenítésben . A mintát vagy biopsziát gyakran ultrahang vagy radiológiai útmutató alapján végzik ; ezután ultrahang-vezérelt biopsziáról és a mell sztereotaxiás biopsziájáról beszélünk . A bizonyosság diagnózisát a vett minta anatómiai-patológiai vizsgálata fogja elvégezni .
A kiterjesztés értékelése
Az áttétek keresése alapvető fontosságú az emlőrák kezelésének stratégiájában. De a sok elvégzett tanulmány vagy egyes kutatások mélyreható ismerete ellenére jelenleg nincs validált stratégia az emlőrák metasztázisának szisztematikus keresésére.
Az ajánlások többsége jelenleg kiterjesztést javasol, beleértve a mellkas röntgenfelvételét, a máj ultrahangját és a csont szcintigráfiáját. Nagyon kicsi daganatok esetén ez az értékelés opcionális lehet. Másrészt előrehaladott daganatok (gyulladásos, multi-fokális daganatok, jelentős nyirokcsomó-invázió) esetében a kezdeti metasztatikus kockázat magas, és indokolttá teheti az alaposabb értékelést, beleértve az egész test komputertomográfiát (CT) és az emlő MRI-t. .
A daganat mérete, az áttétes lymphadenopathia, a bőr vagy a mellkas falának érintettsége vagy távoli áttétek lehetővé teszik az emlőrák klinikai osztályozásának megállapítását.
| TNM osztályozás | Leírás |
|---|---|
| Tx | Olyan daganat, amelyet nem lehet értékelni az információ hiányával |
| T0 | Nincs bizonyíték az elsődleges daganatra |
| Tis | Ductalis carcinoma in situ vagy lobularis carcinoma in situ, vagy a mellbimbó Paget-kórja mögöttes daganat nélkül |
|
T1 T1a T1b T1c |
Daganat a legnagyobb méreténél kevesebb, mint 2 cm - T <0,5 cm - T 0,5 és 1 cm között - T 1 és 2 cm között |
| T2 | Tumor nagyobb, mint 2 cm , és kevesebb, mint 5 cm a legszélesebb helyen |
| T3 | A legnagyobb méretben több mint 5 cm-es daganat |
|
T4 T4a T4b T4c T4d |
Bármilyen méretű daganat kiterjesztéssel: - a mellkasfalig - bőrödéma vagy fekélyesedés vagy áthatolási csomópont - a bőr és a mellkas falán Gyulladásos rák |
Különböző típusú emlőrák és carcinoma
WHO osztályozás
Az anatomopatológiai vizsgálat a mellrák különböző típusainak létezését mutatja be. Az Egészségügyi Világszervezet szerint az alábbi táblázat az összes rákközpontban alkalmazott emlőrák szövettani besorolását mutatja.
Mint minden hámdaganatnál , itt is vannak daganatok . Az emlőrák leggyakoribb változata a ductalis típus .
| Nem beszűrődő hámdaganatok |
| Ductalis carcinoma in situ (intracanalis) (DCIS) |
| Lobuláris carcinoma in situ (LCIS) |
| Infiltráló hámdaganatok |
| Invazív ductalis carcinoma NOS (nincs más jelzés) |
| Invazív ductalis carcinoma, domináns intracanalis komponenssel |
| Invazív lobularis carcinoma |
| Nyálkahártya (kolloid) karcinóma |
| Medulláris carcinoma |
| Papilláris carcinoma |
| Tubuláris karcinóma |
| Adenoid cisztás karcinóma |
| Fiatalkori szekréciós karcinóma |
| Apokrin carcinoma |
| Laphámsejt típusú metaplasztikus karcinóma |
| Orsósejt típusú metaplasztikus karcinóma |
| Chondroid és csont metaplasztikus karcinóma |
| Vegyes típusú metaplasztikus karcinóma |
| A mellbimbó Paget-kórja |
Gyulladásos rák
A gyulladásos emlőrák az emlőrák nagyon ritka formája (1–4%), amely gyorsan fejlődik néhány nap vagy hét alatt. Gyorsan terjed a nyirok útján, anélkül, hogy ideje lenne daganat kialakítására. A nyirokerek rákos sejtek általi elzáródása változó jelentőségű oka a mell helyi gyulladásának. A melltályog diagnózisát kezdetben gyakran említik, különösen azért, mert a képalkotás (mammográfia és ultrahang) gyakran negatív. A mell többé-kevésbé fájdalmas vörösségének fennmaradása biopsziát igényel, amelyek önmagukban megerősítik a betegséget. A kezelés elsősorban kemoterápián alapul, amelyet a közelmúltban elért haladás számos esetben lehetővé tett.
Szövettani és molekuláris osztályozás
Az emlőrák kutatásával összefüggésben az emlőrák négy típusát különböztetik meg főként morfológiájuk és három molekuláris marker jelenléte alapján: az ösztrogén receptor (ER) és a receptor progeszteron (PR) túlexpressziója . HER2 marker , utóbbi EGFR típusú receptor. Az eredményül kapott négy osztály a következő:
- Alap- vagy hármas negatív: ER- / PR- / HER2-
- HER2-túlexpresszálás: ER- / PR- / HER2 +
- A világítótest: ER + / PR + / HER2-
- B luminál: ER + / PR + / HER2 +
A bazális és a luminalis típus neve a daganatok hasonlóságából származik a megfelelő normális emlőhámszövetekkel. Általában a bazális és a HER2 túlexpresszáló daganatok klinikai prognózisa gyenge.
A DNS-chipek szisztematikus alkalmazásán alapuló vizsgálatok a betegek kohorszaiban különféle génexpressziós aláírásokat is képesek elkülöníteni, és a luminal típusú emlőrákok hajlamosak a GATA3 , KRT19 gének és fehérjék expresszálására , másrészt a bazális típusúak nem ezeket fejezi ki, hanem többek között az ETS1 és a CD44 .
Kezelések
Mint minden rák esetében, ideális (orvosi szempontból) a daganat műtéti eltávolítása, amely egyúttal lehetővé teszi a diagnózis biztos felállítását. A következő probléma a kiterjesztés felmérése : az érintett nyirokcsomók jelenléte vagy hiánya, áttétek jelenléte vagy hiánya.
Az emlőcsonkítás azonban a nőknek általában megfelel a pszichológiai és társadalmi megcsonkításnak is, a mell a nőiesség egyik legerősebb szimbóluma. Egyes nők ezt a megcsonkítást nőiességük és ezért személyiségük negációjaként élhetik meg.
Vannak más kezelések is, például kemoterápia , sugárkezelés és hormonterápia , amelyek bizonyos esetekben alkalmazhatók a daganat csökkentésére a műtét előtt. Az egyes kezeléstípusok hatékonysága és kockázata a rák típusától, annak mértékétől és helyétől függ.
Terápiás stratégia
Az emlőrák kezelésére sokféle módszer létezik, de az optimális kezelés érdekében ezeket mindig egyedileg kell meghatározni. Így az emlőrák genomikus elemzése körülbelül ötven különböző emlőrákot tár fel, amelyek mindegyik típusa vagy csoportja hajlamos lehet egy adott célzott terápiára.
A lokalizált emlőrák esetében a kezelésnek szinte mindig gyógyító célja van. A négy terápiás fegyveren alapszik, amelyek a sebészet, kemoterápia, sugárterápia és hormonterápia. A műtét elengedhetetlen lépés az emlőrák gyógyításában, más kezelések általában csak a visszaesés kockázatának csökkentésére irányulnak. Ezért jelezni fogják, ha ez a kockázat jelentős, és ha a kezelés feltételezett előnye elegendő, mert ezeknek a kezeléseknek vannak mellékhatásai. A várható hasznot ezért össze kell mérni a szövődmények kockázatával.
Áttétes mellrák esetén: a fejlődés ezen szakaszában nagyon ritkán lehet gyógyító kezelést ajánlani. De a modern kezelések gyakran lehetővé teszik a túlélés meghosszabbítását több évvel. Itt lehetetlen részletezni a különféle lehetséges terápiás stratégiákat, mert nagyon sok tényezőtől függenek. Az áttétes emlőrák kezelése kemoterápiával és hormonterápiával kezdődik. A metasztatikus helyek műtéti vagy sugárterápiás kezelése megfontolható vagy gyógyító célból, amikor az összes helyszín hozzáférhető a kezeléshez (pl .: egyszeri máj- vagy csigolyatétek), vagy palliatív célokból ( pl .: metasztázis fájdalmas csontjának besugárzása).
Számos genetikai marker van, amely korrelál az emlőrák prognózisával , és ezért potenciálisan irányíthatja a kezelést.
Az emlőrák súlyosságának és prognózisának molekuláris markerei is léteznek. A metallotionein (MT) egy. Könnyen kötődnek bizonyos fémekhez, és legalább 10 funkcionális MT-gén kódolja őket, amelyek az emlőráksejtek, különösen az invazív duktális emlőrákok proliferációjával társulnak. Ez teszi a TM-t az emlőrák prognosztikus biomarkerévé , amely immunhisztokémiai úton detektálható . Minél több TM expresszálódik az emlőrákban, annál súlyosabb a rák.
Bizonyos kezelések (alkilezőszerek vagy tamoxifen ) gátolhatók a metallotionein túlzott mértékű expressziójával (például nehézfém-mérgezésben szenvedő betegeknél)
Sebészet
A daganat eltávolításaA mellműtétnek három típusa van: lumpectomia (a daganat eltávolítása), segmentectomia (a mell egy részének eltávolítása) és mastectomia (a teljes emlő eltávolítása).
Azokban az esetekben, amikor a daganatot elég korán kezelik, minimális műtét (konzervatív műtét) lehetséges. Néha el kell távolítania az egész mellet. A rekonstruktív műtét elvégezhető egyszerre vagy másodlagosan.
- A rekonstruktív mellműtét illusztrációja: a hasizmok egy részének helyreállítása ( restus abdominus ) a mell rekonstrukciójához, National Cancer Institute .
Ez a technika a hónalj üregében (a hónalj szintjén) elhelyezkedő nyirokcsomók eltávolításából áll . Ennek a műveletnek számos mellékhatása van, mert ez az abláció destabilizálja a nyirokhálózatot , ami lymphedema (nagy kar) megjelenéséhez vezethet . Ezeknek a mellékhatásoknak a csökkentése céljából valósították meg az őrszemcsomó technikát .
Sentinel csomópont technikaDaganat esetén az őrszemcsomó kapja meg először a nyirokelvezetést.
Az őrszemcsomópontot festék injektálásával lehet azonosítani, akár radioaktív kolloid kíséretében, akár nem. Ezt követően visszavonják, hogy lehetővé váljon egy anatomopatológiai vizsgálat. Ha a vizsgált nyirokcsomó egészséges, ezzel a technikával elkerülhető, hogy axilláris disszekciót kell igénybe venni (a régió szinte összes nyirokcsomójának eltávolítása), ami jelentős következményekhez vezetne. 3 cm-nél kisebb daganattal rendelkező betegeknél alkalmazható, és akár 70% -ukat is érinti.
Ez a technika validált, 10% -nál kisebb hibaaránnyal.
A műtét utáni fájdalom megelőzéseA krónikus posztoperatív fájdalom kockázatának csökkentése érhető el, ha a műtét idején lokoregionális érzéstelenítést hajtanak végre . Az emlőrákos műtét után három-tizenkét hónappal a krónikus műtét utáni fájdalom minden hetedik embernél megelőzhető ( kezelendő emberek száma ). Bár biztatóak, ezek az eredmények alacsony szintű bizonyítékokon alapulnak.
Műtét utáni ellenőrzésA kezdeti kezelés után elengedhetetlen, hogy a beteget rendszeresen ellenőrizzék.
Több vizsgálat nem szükséges, de az éves bilaterális mammográfia elengedhetetlen, különösen konzervatív műtétek esetén. Esettől függően kombinálható más, az egyes eseteknek megfelelően meghatározott további vizsgálatokkal.
Még az optimálisan kezelt emlőrák is kiújulhat helyileg vagy távolról ( áttét ). A kiújulás évekkel a kezdeti kezelés után előfordulhat, ezért fontos a felügyelet fenntartása.
Sugárterápia
Csökkenti ennek a ráknak a mortalitását, de kifogástalan technikát igényel az egészséges szövetek besugárzásának csökkentése érdekében, amely a szív- és érrendszeri patológiából származó túlzott halálozáshoz vezethet. Különbséget tesznek a mell sugárterápiája és a nyirokcsomó területein. Konzervatív műtét esetén a sugárterápiát mindig el kell végezni, mert ez jelentősen csökkenti a helyi kiújulás kockázatát. A sugárkezelés annál fontosabb lesz, minél fiatalabb a nő. Teljes mell eltávolítás esetén bizonyos esetekben sugárterápia javallt a helyi kiújulás kockázatának csökkentése érdekében. A ganglionláncok besugárzása a daganat helyétől és a ganglionok anatómpatológiás vizsgálatának eredményétől függ.
Hosszú távú mellékhatásokA sugárterápiától másodlagos halálozás kockázata a kardiovaszkuláris halálozáshoz képest csak a kezelés utáni harmadik évtizedben növekszik - derült ki egy több mint 500 000 nőt megfigyelő tanulmányból.
A magzatra jelentett kockázatokról a rák kezelésében alkalmazott sugárterápia vagy kemoterápia összefüggésében végzett európai tanulmány kimutatta, hogy azoknak a magzatoknak, akiknek édesanyját terhesség alatt kezelték, nem lenne több szívhiba, mint egy exponálatlan gyermeknél.
Ahhoz, hogy a kockázatok azonosítása az emlő fibrózis által indukált radioterápia, egy teszt által kifejlesztett Inserm mérésére „aránya rádió-indukált limfocita apoptózis (TALRI)”. Minél magasabb a TALRI szint, annál kisebb a mellfibrózis kockázata.
Kemoterápia
Ez rákellenes gyógyszerek rögzített időközönként történő beadásából áll, általában 3 hetente. Az mellrák adjuváns kemoterápiás tanfolyamainak (műtét után végzett kemoterápia) száma 4 és 6 között van. Az adjuváns kemoterápia előnyei a kemoterápia nélküli műtéti kezeléssel szemben a mortalitás jelentős csökkenése és az alacsonyabb kiújulás aránya. A hónalj nyirokcsomók érintettsége esetén jelenleg a kemoterápia 3 ciklusát antraciklinnel (Farmorubicin °) és ciklofoszfamiddal (Endoxan °), majd 3 ciklust docetaxellel (Taxotere °) kombináló séma a referencia. A hónalj nyirokcsomó invázió nélküli daganatok esetében a rossz prognózissal rendelkező tényezők keresése, amelyek megmagyarázhatják a kedvezőtlen eredményt (magas szövettani fokozat, nincsenek hormonreceptorok, egyeseknél a daganat mérete meghaladja a 15, sőt 10 mm- t, stb.) az adjuváns kemoterápia indikációjának jelzésére.
Előrehaladott vagy gyulladásos daganat esetén néha kemoterápiával ( neoadjuváns kemoterápiával ) kell elkezdeni a kezelést a daganat méretének csökkentése és esetleg konzervatív műtét lehetővé tétele érdekében.
Neo-adjuváns kemoterápiát is alkalmaznak a kivágás méretének korlátozása érdekében: a lumpectomia néha elegendő, ha kezdetben az adjuváns kemoterápiával végzett mastectomiát tervezték.
Ez utóbbi indikációban, míg az általános mortalitás, a betegség romlásáig eltelt idő és a távoli kiújulás aránya nem különbözik az adjuváns kemoterápiától, a lokoregionális kiújulások gyakoribbak. Jelenleg nincs standard neo-adjuváns kemoterápiás protokoll.
Hátrányok: általános fáradtság, hányinger és hányás, ideiglenes hajhullás. A felhasznált termékektől függően változnak, és jobban kontrollálhatók.
Számos termék bizonyult hatékonynak az emlőrák adjuváns kezelésében , és referenciamutatóval rendelkezik, de más termékek piacra lépnek és / vagy tanulmányozás alatt állnak.
Célzott terápiák
A trasztuzumab forradalmasította sok beteg kezelését. Egyéb gyógyszereket értékelnek. Ezeket a molekulákat gyakran jó tolerancia jellemzi, azonban különösen drága termékek.
TrasztuzumabNéhány emlőrák jelentősen túlexpresszálja a Her2 gént (ez az emlőrákok körülbelül 25% -át érinti, gyakran rossz prognózissal, mivel a Her2 - vagy a CerbB2 - a membránreceptor, amely lehetővé teszi a sejtek fokozott proliferációjának egyik útjának aktiválását). A ráksejtek ezután onkogén függőséget mutatnak , túlélésüktől függően a Her2 által kiváltott jelátviteli út működésétől . Ezt gátolja a trasztuzumab (Herceptin °), amely monoklonális antitest blokkolja ezt a receptort. A Herceptint először palliatív helyzetben alkalmazták. Ebben az összefüggésben a Herceptin átlagosan megduplázta ezen betegek túlélési idejét. Az adjuváns kemoterápiához hozzáadva a Herceptin ° infúzió 21 naponta 12 hónapig, a felére és a halálozás mintegy harmadára csökkenti a HER2 + betegeknél a visszaesés kockázatát.
Novembere óta 2017 Ontruzant, hasonló biológiai gyógyszer a trastuzumab , kimondta az első forgalomba hozatali engedélyt adott ki az Európai Bizottság , amely lehetővé teszi annak eloszlása a Európai Unió , valamint Norvégia , Izland és Liechtenstein. .
BevacizumabA 2007 , bevacizumab ( Avastin ) használunk áttétes emlőrák (Franciaországban forgalomba hozatali engedélyt 2007-ben, első vonalbeli áttétes). Ez egy anti- VEGF monoklonális antitest , amelyet infúzióval juttatunk be. Szelektíven kötődik ehhez a növekedési faktorhoz, és így blokkolja a neo- angiogenezist . A paklitaxellel kombinálva ez a kezelés megduplázza a válaszidőt (a betegség előrehaladásáig eltelt idő). Másrészt a túlélési idő nem nő.
Franciaországban, 2011 májusában , a Haute Autorité de Santé arra a következtetésre jutott: „Tekintettel a túlélés alacsony növekedésére a kiújulás nélkül és a bevacizumab / taxán kombinációban a taxánnal szemben a teljes túlélés javulásának hiányára , a bevacizumab paclitaxelhez adásának előnye ma kevésbé van megalapozva. Ez az érdeklődés azokra a betegekre korlátozódik, akik negatívan reagálnak a HER2 receptorokra , az ösztrogénre és a progeszteronra . " .
LapatinibAz orálisan adott lapatinib ( Tyverb ) a HER2 és HER1 receptor (EGFR) kináz aktivitásának intracelluláris tirozin inhibitora . A HER2-t túlzott mértékben expresszáló betegeknél, a herceptin alatt történő tumor előrehaladásakor, akik már antraciklineket és taxánokat kaptak, a lapatinib- kapecitabin kombináció megduplázza a válaszidőt a csak a kapecitabinnal összehasonlítva, a teljes túlélés javulása nélkül. A forgalomba hozatali engedélyt 2008-ban kapták meg.
Hormonterápia
Az emlőrák körülbelül kétharmadában a rákos sejtek felesleges hormonreceptorokkal rendelkeznek. A tumorról akkor azt mondják, hogy hormonérzékeny, mert az ösztrogén ezen receptorokon keresztül serkenti a rákos szaporodást. Az emlőrákban a hormonkezelések vagy az ösztrogénszint csökkentésével járnak a vérben, ezért a hormonreceptorok stimulálásával (kasztráció, anti-aromatázok), vagy a hormonreceptorok ( antiösztrogén ) blokkolásával .
A petefészek elnyomása- műtéti úton, laparotomiával vagy laparoszkópiával
- sugárzás: 12–16 szürke színűvé teszünk 4–8 frakcióban egy kis medencén, miután ultrahanggal meghatároztuk a petefészkek helyzetét;
- Orvosi, általában agonistákat alkalmazó LHRH
- Leuprorelin , Enantone LP 3,75 mg / 4 hét
- Goserelin , Zoladex 3,6 mg / 4 hét
- Megjegyzés: A Decapeptyl nem rendelkezik forgalomba hozatali engedéllyel mellrák esetén.
-
Tamoxifen 20 mg d- 1
- Mechanizmus: részleges ösztradiol receptor antagonista
- Óvintézkedés: évente végezzen endometrium-vizsgálatot, ellenőrizze a máj működését és a triglicerideket, mérje meg az ösztradiolt a plazmában és adjon hozzá LHRH-t, ha fokozott, hatékony fogamzásgátlás (teratogén).
-
Fulvestrant 250 mg IM 28 naponta
- Mechanizmus: ösztrogén receptor antagonista részleges agonista hatás nélkül.
A tamoxifen alkalmazása akkor előnyös, ha a daganatban ösztrogén receptorok vannak, függetlenül a beteg életkorától. A tamoxifen adjuváns hormonterápia alkalmazásának optimális időtartama 5 év 20 mg d- 1 dózis mellett . A tamoxifen használata 8% -kal, a halálozás kockázata 5% -kal csökkenti a megismétlődés kockázatát.
Anti-aromatázok2004 óta új molekulák kínálhatók a posztmenopauzás nők számára. Ezek az aromatáz inhibitorok . A két legjobban értékelt molekula az anasztrozol és a letrozol . Toxikussági profiljuk eltér a tamoxifentől. E két molekula beadása lehetővé teszi az emlőrákos műtét utáni relapszusok csökkentését, a teljes túlélés szempontjából semmilyen előnnyel nem jár ( szemben a tamoxifennel).
-
Letrozole , Femara 2,5 mg d -1
- Mechanizmus: nem szteroid aromatáz inhibitor
- Óvintézkedés: csontsűrűség, diszlipidémia
-
Anastrozole , Arimidex 1 mg
- Mechanizmus: Nem szteroid aromatáz inhibitorok
- Óvintézkedés: csontsűrűség, diszlipidémia
-
Exemestane , Aromasin 25 mg
- Mechanizmus: szteroid aromatáz inhibitor
- Óvintézkedés: csontsűrűség, diszlipidémia
Megelőzés: hogyan csökkenthető a kockázat
Annak tudatában, hogy az emlőrák hormonális betegség, elméletileg minden olyan intézkedés vagy kezelés, amelynek célja az ösztrogénnek vagy az ösztrogént utánzó endokrin rendszert károsító anyagoknak való kitettség időtartamának és intenzitásának csökkentése, hatékony.
A kockázatot csökkentő cselekvések vagy események
Többféle intézkedés hajtható végre az emlőrák kialakulásának kockázatának csökkentésére.
Nőgyógyászati választásokA kockázati tényezőknek közös nevezőjük van: a nők hormonális impregnálásának növekedése: közvetlen, a menopauza hormonális kezelésére, az ösztrogén-progesztogén tabletta, a menstruációs ciklusok számának növekedése (alacsony terhességi szám vagy rövid szoptatási idő), vagy közvetetten az aromatáz enzim aktivitásának növekedése a zsírban, alkohol, túlsúly, fizikai aktivitás hiánya miatt. Így javasolható lenne az emlőrák elsődleges megelőzése, az életmód megváltoztatásával
A fogamzásgátló tabletta választásaEz olyan tablettáknak kedvez, amelyek nem tartalmazzák az ösztrogént blokkoló petefészek aktivitást.
Az első terhesség korai életkorbanAz első terhesség életkorának csökkentése csökkenti az emlőrák kockázatát, mert a pubertás és az első terhesség közötti ciklusok ebből a szempontból a legveszélyesebbnek tűnnek. Az első terhesség a vakcinára úgy hatna, mint a rák elleni oltás, megkülönböztetve a szöveteket, így kevésbé sérülékenyek a hormonokkal szemben. A terhesség ezért oltóanyagként hat az ösztrogén ellen. Minél korábban jelentkezik ez az első terhesség, annál jobban működik.
Hosszan tartó szoptatásA hosszan tartó szoptatás (mert a petefészkek „elalvása” ) csökkenti a kockázatot. A WCRF jelentése szerint a szoptatás előnyös, függetlenül a rák kialakulásának idejétől ( menopauza előtti vagy utáni időszak ).
A menopauza hormonterápia (HRT) elkerülése"A menopauza hormonális kezelését ma az emlőrák kockázati tényezőjének tekintik, különösen akkor, ha több mint 5 évig szedik" - számolt be Le Figaro 2008-ban.
Életmódválasztás FogyásAz elhízás és a túlsúly növeli az emlőrák kockázatát. Pierre Kerbrat professzor (Eugène-Marquis központ, Rennes) 2008-ban úgy becsülte, hogy a női elhízás elleni küzdelem évente 13 000 új emlőrákos esetet akadályoz meg az Európai Unióban.
TestmozgásKerbrat professzor szerint a heti 5 nap 30 perces fizikai aktivitásának gyakorlása 30% -ról 40% -ra csökkentené az új esetek számát. A védőhatás mind az elhízás elleni küzdelemből, mind pedig a hormonális váladékra gyakorolt testmozgásból származik. Amerikai tanulmányok kimutatták megelőző hatását is a betegség megismétlődése ellen.
Az alkoholfogyasztás csökkentéseAz alkohol bevitelével nő a mellrák kockázata. A mértékletes alkoholfogyasztás 20–30% -kal növeli a kockázatot. Pontosabban, a kockázat 10% -kal nő, ha a napi alkoholfogyasztás 10 g alkohollal (azaz egy pohárral) nő .
ÉtelválasztásCsökkentenék a kockázatot.
- 334 850, 35–70 éves nő kérdőívének felhasználásával, az EPIC (European Prospective Investigation on Cancer and Nutrition) kohorszba (nyomon követési időtartam: 11,5 év) felvett tanulmány 2013. áprilisazt mutatja, hogy nincs kapcsolat a flavonoidok és a lignán ( fitoösztrogének ) fogyasztása és az emlőrák kockázata között, függetlenül attól, hogy figyelembe veszik-e a menopauza állapotát és a hormonreceptorok állapotát .
A vérben lévő transz-zsírsavak csaknem 50% -kal növelik a nők mellrák kockázatát. A transz-zsírsavakat olyan feldolgozott élelmiszerekben használják, mint a kenyér és az ipari sütemények, sütemények, sütemények, chipsek, pizzák, ipari tészták.
- A zöld tea és / vagy a szója védő tulajdonságokkal bírhat (ezek magyarázhatják azt a tényt, hogy Európában 12 nőből 1 nőnél alakul ki ez a rák, szemben Japánban 80-zal, ahol ezeket az ételeket fogyasztják) .
- Az emlőrák megjelenése után úgy tűnik, hogy a gyümölcsök és zöldségek fogyasztásának megkétszereződése nem csökkenti a kiújulás kockázatát.
- Az Omega 3 kiegészítést 2008-ban tesztelték, hogy javítsa-e a kemoterápiát.
- A hormonkezelések elmaradása csökkentené az emlőrák kockázatát.
- A SERM típusú kezelések ( tamoxifen , raloxifene ) csökkentenék a kockázatot. Ezeknek a gyógyszereknek azonban jelentős mellékhatásaik vannak ( a két molekula tromboembóliás megbetegedéseinek növekedése, a tamoxifennél az endometrium rákja ), és helyüket még nem kell meghatározni.
"Megelőző" műtéti kezelések
Megelőző műtéti kezeléseket javasoltak azoknál a nőknél, akiknek családtörténetében emlőrák található, mutációval a BRCA1 vagy BRCA2 génekben. Ezekben a nőkben az emlőrák kockázata 80 és 80 éves kor előtt 40 és 85% között változik. A műtéti javaslatok vagy mindkét emlő eltávolítása kétoldali oophorectomiával vagy anélkül , vagy önmagában kétoldalú oophorectomia.
A megelőző bilaterális mastectomia (MBP) jelenlegi megfigyelési tanulmányai azt mutatják, hogy ez csökkentheti az emlőrák és / vagy a halál előfordulását, bár ezeknek a tanulmányoknak módszertani korlátai vannak. Az eljárás utáni elégedettség jónak tűnik, csökkenő rákos aggodalom, csökkent testkép és szexuális érzetek kísérik. Azoknál a nőknél, akiknél az egyik mell daganatos megbetegedést szenvedett, a másik emlő eltávolítása látszólag csökkenti a rák előfordulását, de a hosszú távú túlélésre gyakorolt hatás bizonytalan az eredeti rák megismétlődésének vagy áttétének folyamatos kockázata miatt.
Pszichológiai szempontok
Nagyon nehéz megbékélni azzal, hogy rákja van, mivel ezt a hírt régóta a közvetlen halál hírének tekintik. Ezenkívül a kórházi kezelés, a műtét és az adjuváns kezelések mélyen megváltoztatják a beteg életét. Ezért elengedhetetlen a betegeknek megfelelő pszichológiai támogatást nyújtani, amely általában magában foglalja az azonos megpróbáltatásokon áteső betegcsoportokban való részvételt.
A későn diagnosztizált emlőrák azonban gyakran nagyon megcsonkítja. A nőknél ez az emlőcsonkítás általában megfelel a pszichológiai és társadalmi megcsonkításnak. A mell, amely a nőiesség egyik legerősebb szimbóluma , egyes nők ezt a megcsonkítást nőiességük és ezért személyiségük negációjaként élhetik meg.
A párkapcsolat gyakran szenvedi a betegség következményeit. A kezelést követő időszakban a beteg vagy partnere negatív érzelmeket fejezhet ki, például szemrehányást. Az ilyen típusú helyzetet a szakembereknek komolyan kell venniük, mivel összefüggésbe hozhatók pszichológiai rendellenességekkel, például depresszióval. Nicolas Favez, Sarah Ciro Notari, Tania Antonini és Linda Charvoz szerint ez a fajta helyzet valószínűleg a betegség korai szakaszában jelentkezik, és még akkor is, ha az orvosi prognózis optimista. Ebben az összefüggésben rekonstruktív műtét ajánlható fel, pszichológiai ellátással együtt.
Az emlőrák tehát nemcsak orvosi probléma. Hatással van az életre, a testre és az önbizalomra. Amikor egy nő megkapja az „emlőrák” ítéletet, félelemmel a gyomrában távozik az orvosi rendelőből, sok kérdéssel, hogy milyen lesz az élete a jövőben. Hogyan lehet erről beszélni a rokonainak? Hogyan kezeljük a hajhullást és a szemöldökvesztést? Hogyan lehet kijutni otthonról, és szembenézni mások tekintetével? Hogyan tudja továbbra is gondoskodni gyermekeiről? Vajon képes lesz még valamire? El fogja veszíteni az állását? Mi lesz az életében a férfival való kapcsolatával? Ennyi kérdés, kevés lehetőség a párbeszédre, sok tabu. A nők gyakran visszaesnek a betegségbe, és ez még a terápia sikerét is hátrányosan befolyásolja.
Sok tennivaló van még a betegekkel és családtagjaikkal való megfelelő kommunikáció érdekében, de a nőknek nyújtott egészségügyi ellátás és általában az életminőségük konkrét javítása érdekében is.
A népi kultúrában
A humorista, Marie Reno humoros dalával figyelem a mellére ! .
Megjegyzések és hivatkozások
- https://www.francetvinfo.fr/sante/cancer/cancer-du-sein-il-y-a-une-vraie-recrudescence_1815585.html
- André Cicolella, Mellrák. A járvány vége , szerk. Les Petits Matins, 2016.
- (a) PM Ravdin, Cronin KA, Howlader N et al. „ Az emlőrák előfordulásának csökkenése 2003-ban az Egyesült Államokban ” , New Eng J Med , 2007; 356: 1670-1674
- "Az emlőrák előfordulásának csökkenése 2005-ben és 2006-ban Franciaországban: paradox jelenség" Cancer Bulletin , 2008; 95: 11-5
- (in) Forouzanfar MH, KJ Foreman, Delossantos AM et al. „ Mell- és méhnyakrák 187 országban 1980 és 2010 között: szisztematikus elemzés ” , Lancet , 2011
- Boyle és Ferley, 2004
- WCRF - Mellrák statisztikák
- IARC - Tájékoztató az emlőrákról
- Forrás Inserm 2008, konzultáció: 2008 10 04
- "Antoine Spire David Khayat-tal beszél a Le Monde de l'Educationért" kivonatok egy cikkből, amely 2006 áprilisában jelent meg a Le Monde de l'Education-ban
- "Fejlett emlőrák: egy új kezelés ígéretei" a futura-sciences.com oldalon
- Népegészségügyi Felügyeleti Intézet (InVS) INSERM
- „ Emlőrák: a kevésbé intenzív kezelések ” (megajándékozzuk 1 -jén október 2015 )
- Nemzeti Rákkutató Intézet, Mellrák, 2008. április frissítés.
- " Rák: a túlélés javul Franciaországban " , a sante.lefigaro.fr oldalon (hozzáférés : 2016. február 2. )
- Wang B, He M, Wang L, Engelgau MM, Zhao W, Wang L. Mellrák-szűrés felnőtt nők körében Kínában, 2010. Prev Chronic Dis 2013; 10: 130136. DOI: https://dx.doi.org/10.5888/pcd10.130136
- (in) Nagata, Chisato, " A szója-izoflavon bevitel és a mellrák kockázatának társulásában figyelembe veendő tényezők " , J Epidemiol , vol. 20, n o 22009, P. 83-89 ( ISSN 1349-9092 , DOI 10,2188 / jea.JE20090181 , olvasható online )
- Wooster R, Weber BL. Mell- és petefészekrák . N Engl J Med 2003; 348: 2339-47
- Általános ráktanfolyam P r JF HERON
- Loibl S, Poortmans P, Morrow M, Denkert C, Curigliano G, Mellrák , Lancet, 2021; 397: 1750-1769
- Isabelle Plo, Corentin Laulier, Fabienne Lebrun, Laurent Gauthier, Fabien Calvo és Bernard Lopez. Az AKT1 a BRCA1 és RAD51 citoplazmatikus retenciójának indukálásával gátolja a homológ rekombinációt . Rákkutatás. 2008. november 15.
- [A hormonális kezelések elősegítenék-e az emlőrákot? CEA sajtóközlemény]
- Sajtóközlemény / Kutatás a Joseph-Fourier Egyetemtől (Grenoble) ; [CK2: fontos szerep az emlődaganatok progressziójában] ; 2012. május 10
- Clavel-Chapelon F, A menstruációs ciklusok összesített száma és az emlőrák kockázata: a francia nők E3N kohorszvizsgálatának eredményei , Cancer Causes and Control, 2002; 13: 831-838
- Beral V, Mellrák és hormonpótló terápia a nők millió tanulmányában , Lancet, 2003; 362: 419-27
- lányok már korábban is elérik a pubertást
- (in) Merrill RM Fugal S Novilla LB, Raphael ™, " Az anya korai és késői életkorához kapcsolódó rák kockázata az első születéskor " , Gynecol Oncol , Vol. 96, n o 3,2005, P. 583-93. ( PMID 15721398 , DOI j.ygyno.2004.11.038 )
- (en) FAUPEL-Badger JM, Arcaro KF, Balkam JJ, Eliassen AH, Sherman ME és mtsai. , „ Szülés utáni átalakítás, laktáció és emlőrák kockázata: összefoglaló egy Nemzeti Rákkutató Intézet által támogatott műhelyről ” , J Natl Cancer Inst , vol. 105, n o 3,2013, P. 166-74. ( PMID 23264680 , PMCID PMC3611853 , DOI 10.1093 / jnci / djs505 , online olvasás [html] )
- (en) Diamanti-Kandarakis E, Bourguignon JP, Giudice LC, et al. , „ Endokrin rendszert károsító vegyi anyagok: az Endokrin Társaság tudományos nyilatkozata ” , Endocr. Fordulat. , vol. 30, n o 4,2009. június, P. 293–342 ( PMID 19502515 , PMCID 2726844 , DOI 10.1210 / er.2009-0002 )
- Romain Loury (2015) Az emlőrák mögött, DDT , 2015. június 16
- „Dr. de LORGERIL - Az oka az emlőrák végre azonosította. Hogyan védekezhet?”
- Zsírsejtek és emlőrák - veszélyes kombináció (a CNRS sajtóközleménye szerint) 2011/04/05
- Mellrák: megelőző kampányokat kell folytatni , Le Figaro , 2008. október 23., 11. oldal
- Megnövekedett emlőrák kockázat a posztmenopauzás nőknél súlygyarapodásuk alapján
- Béatrice Dirat; A rákkal társult adipociták aktivált fenotípust mutatnak és hozzájárulnak az emlőrák inváziójához ; Cancer Research, doi: 10.1158 / 0008-5472.CAN-10-3323 Cancer Res 2011. április 1. 71; 2455 Összegzés )
- B. Dirat és mtsai. Rákkutatás , 1 st április 2011
- Tanulmány közötti összefüggést mutató emlőrák, és az állati zsírok társkereső 1986-tól
- Tanulmány a rák azonosított tényezőiről Spanyolországban
- Étrendi zsírbevitel és az emlőrák kockázata: eset-kontroll tanulmány Kínában
- Inserm és az Institut Gustave-Roussy munkájának következtetései, amelyek célja a különböző zsírsavak szerepének felmérése az emlőrák kialakulásában, az 1995 és 1998 között összegyűjtött vérvizsgálatokból 100 000 nő közül 25 000 között 100 000 nő után következtek. - hívták E3N vizsgálatnak .
- in (in) növekedési tényező növeli a rák kockázatát
- (in) Tej, tejtermékek és laktózbevitel és petefészekrák kockázata: Az epidemiológiai vizsgálatok metaanalízise , International Journal of Cancer , vol. 118. szám, 2. szám, o. 431-441
- (in) Változás a plazma inzulinszerű növekedési faktor 1-ben és az inzulin-szerű növekedési faktor kötő fehérje-3-ban: személyes és életmódbeli tényezők (Egyesült Államok)
- "Andok jelentése, p76 / 210"
- (in) "Különböző fajokból származó nyers vagy felhevített tej fogyasztása: A lehetséges táplálkozási és egészségügyi előnyök értékelése, p4 / 14
- (a) "Association of IGF-1-tartalom a teljes kiőrlésű, csökkentett zsírtartalmú, és alacsony zsírtartalmú tej México"
- ( tejtermékek), kalcium és D-vitamin bevitele és az emlőrák kockázata
- (in) Tejtermékek és emlőrák kockázata
- [PDF] Jelentés az alkoholról és a rák kockázatáról (60 oldal), Nemzeti Rákkutató Intézet és Nacre hálózat, 2007)
- Xue F, Willett WC, Rosner BA, Hankinson SE, Michels KB, Cigarettadohányzás és az emlőrák előfordulása , Arch Intern Med, 2011; 171: 125-133
- (en) Lundqvist J, M Norlin, Wikvall K, " 1α, 25-dihidroxi-D (3) fejt ki szövet-specifikus hatásokat ösztrogén androgén metabolizmus " , Biochim Biophys Acta ,2011. január( PMID 21262387 , DOI 10.1016 / j.bbalip.2011.01.004 )
- (en) Napoli N, Vattikuti S, Ma C, et al. , „ Az alacsony D-vitamin és mozgásszervi panaszok magas gyakorisága mellrákos nőknél ” , Breast J , vol. 16, n o 6,2010, P. 609–16 ( PMID 21070438 , DOI 10.1111 / j.1524-4741.2010.01012.x )
- (in) Grant WB, Peiris AN, " A lehetséges szérum 25-hidroxi-D-vitamin szerepe fekete-fehér egészségügyi eltérésekben az Egyesült Államokban " , J Am Med Dir Assoc , Vol. 11, n o 9,2010. november, P. 617–28 ( PMID 21029996 , DOI 10.1016 / j.jamda.2010.03.013 )
- (in) Engel P Fagherazzi G, S Mesrine, Boutron-Ruault MC, Clavel-Chapelon F, " Az étrendi D-vitamin és a napsugárzás együttes hatása mellrák kockázata: a francia E3N kohorsz eredményei " , Cancer Epidemiol. Biomarkerek Előző , vol. 20, n o 1,2011. január, P. 187–98 ( PMID 21127286 , DOI 10.1158 / 1055-9965.EPI-10-1039 )
- (in) Mammográfiai sűrűség és az emlőrák kimutatásának kockázata és Norman F. Boyd, Helen Guo, Lisa J. Martin, Limei Sun, Jennifer Stone, Eve Fishell, Roberta A. Jong, Greg Hislop, Anna Chiarelli, Salomon Minkin, Martin J. Yaffe, New Eng J Med , 2007; 356: 227-236
- (en) Travis LB, Hill D, Dores GM, Gospodarowicz M, van Leeuwen EF, Holowaty E et al. „ Halmozott abszolút emlőrák-kockázat a Hodgkin-limfóma miatt kezelt fiatal nőknél ” J Natl Cancer Inst . 2005; 97: 1428-37
- (in) Einstein AJ, Henzlova MJ, Rajagopalan S, " A sugárterheléssel járó rák kockázatának becslése 64 szeletes számítógépes tomográfia koszorúér-angiográfiából " JAMA 2007; 298: 317-323
- (in) Kolstad HA, "Az éjszakai műszak munkája, valamint az emlőrák és más rákos megbetegedések kockázata - az epidemiológiai bizonyítékok kritikus áttekintése " Scand J Work Around Health . 2008; 34: 5-22
- krónikusan váltakozó fényciklusok növelik az egerek mellrák kockázatát
- (en) Wise J, „ dán éjszakai műszakban dolgozók mellrákos dátuma kompenzáció ” BMJ . 2009; 338: b1152
- (a) Stuebe AM, Willett WC, Fei Xue, Michels KB, " szoptatás és gyakorisága a premenopauzális emlőrákos ," Arch Intern Med . 2009; 169 (15): 1364-1371
- "A terhesség önkéntes megszakítása nem növeli az emlőrák kockázatát" (WHO, online közzététel: 2000. június)
- Silva azonosítók Stavola BD McCormack V, Collaborative Group on szülés előtti kockázati tényezők és későbbi mellrák kialakulásának kockázatát (2008), „ Született mérete és a mellrák kockázata: Re-elemzés egyéni résztvevő adatai 32 Studies ” ( Archív • Wikiwix • Archive.is • Google • Mi a teendő? ) (Hozzáférés : 2017. augusztus 2. ) . PLoS Med 5 (9): e193
- Országos Rákellenes Intézet, Emlőrák férfiaknál .
- Maalej M, Hentati D, Messai T, Kochbati L, El May A, Mrad K, Romdhane KB, Ben Abdallah M, Zouari B. Mellrák Tunéziában 2004-ben: összehasonlító klinikai és epidemiológiai tanulmány. Bikarák. 2008. február; 95 (2): E5-9.
- Antoniou A, Pharoah PD, Narod S et als. A BRCA1 vagy BRCA2 mutációkkal társult emlő- és petefészekrák átlagos kockázata a családtörténet szempontjából nem kiválasztott esetsorokban: 22 tanulmány együttes elemzése , Am J Hum Genet, 2003; 72: 1117-1130
- Robson ME, Chappuis PO, Satagopan J, et al. Az emlőrák utáni eredmény kombinált elemzése: túlélési különbségek a BRCA1 / BRCA2 mutáció státusza és az adjuváns kezelés alapján , Breast Cancer Res 2004; 6: R8-R17
- Rennert G, Bisland-Naggan S, Barnet-Griness O és mtsai. Az emlőrák klinikai eredményei a BRCA1 és BRCA2 mutációk hordozóiban , N Engl J Med 2007; 357: 115-123
- John EM, Miron A, Gong G és Als. [2007; 298 (24): 2869-2876 A patogén BRCA1 mutációs hordozók prevalenciája 5 amerikai faji / etnikai csoportban ], JAMA, 2007; 298: 2869-2876
- Antoniou AC, Casadei S, Heikkinen T és mtsai. Mellrák kockázata mutációkkal rendelkező családokban a PALB2-ben , N Engl J Med, 2014; 371: 497-506
- In situ emlőrák a rákszűrést végző egyesület honlapján (Meurthe et Moselle, 2016. január 13-án konzultáltak)
- "Mellrák: a szűrés illúziói", Coisne S és Lemarchand F., La Recherche , 395, 2006. március: 44-48
- Humphrey LL, Helfand M, Chan BKS, Woolf SH, Mellrák-szűrés: Az amerikai prevenciós szolgálatok munkacsoportjának bizonyítékainak összefoglalása , Ann Intern Med , 2002: 137: 347-360
- eredmények a két-County pere mammográfiás szűrés nem kompatibilisek egyidejű hivatalos svéd mellrák statisztikák . Zahl PH, Peter C. Gøtzsche , Andersen JM, Mæhlen J. Dan Med Bull. 2006. november; 53 (4): 438-40.
- Berg WA, Blume JD, Cormack JB, Kombinált szűrés ultrahanggal és mammográfiával, illetve egyedül a mammográfiával az emlődaganat fokozott kockázatú nőknél JAMA, 2008; 299: 2151-2163
- Leach MO, Boggis CR, Dixon AK és mtsai. Szűrés mágneses rezonancia képalkotással és mammográfiával egy olyan nagy-britanniai populációban, akiknél magas az emlőrák családi kockázata: prospektív multicentrikus kohortvizsgálat (MARIBS) , Lancet, 2005; 365: 1769-78
- Kösters JP, Peter C. Gøtzsche , Rendszeres önvizsgálat vagy klinikai vizsgálat az emlőrák korai felismeréséhez , Cochrane Database of Systematic Reviews 2003, 2. kiadás. Art. Sz .: CD003373. DOI: 10.1002 / 14651858.CD003373
- "A Niramai a képalkotás és az AI használatával forradalmasítja az emlőrák diagnosztikáját"
- "Te tubus, mell termográfia"
- "You tube: Mammográfia és Thermal Imaging"
- "Ncbi, 2014: Új modell az intelligens emlőrák detektálására a termogram képeken."
- "2017. március: Támogató noninvazív eszköz az emlőrák diagnosztizálásához hőkamerás érzékelőként"
- "10Systematic Reviews in Pharmacy, 9. évfolyam, 1. szám, 2018. január-dec., A termográfia hatása az emlőrák kimutatására"
- "2012, Pala: Mellrák: francia botrány?"
- "Termográfia az emlőrák kimutatására"
- "A mell infravörös képalkotása - áttekintés, 18. oldal"
- [cikk - [kapcsolódó] "France-info, 2019: A brit turista felfedezi mellrákját ... múzeumlátogatás közben"]
- Warner E, mellrák-szűrés , N Engl J Med, 2011; 365: 1025-1032
- Miller AB, To T, Baines CJ, Wall C, The Canadian National Breast Screening Study-1: emlőrák mortalitása 11-16 éves követés után: randomizált szűrővizsgálat a mammográfiáról 40–49 éves nőknél , Ann Intern Med, 2002; 137: 305-312
- Moss SM, Cuckle H, Evans A, Johns L, Waller M, Bobrow L, A mammográfiai szűrés hatása 40 éves kortól az emlőrák mortalitására 10 éves utánkövetés során: randomizált kontrollált vizsgálat , Lancet, 2006; 368: 2053-2060
- Zackrisson S, Andersson I, Janzon L, Manjer J, Garne JP, Az emlőrák túlzott diagnózisának aránya 15 évvel a malmöi mammográfiai szűrővizsgálat befejezése után: nyomonkövetési tanulmány , BMJ, 2006; 332: 689-92
- Welch HG, Schwartz LM, Woloshin S, Az emlőrák szűrésének károsodásai : A mammográfiával kimutatott 4 rák egyike álrákos , BMJ, 2006; 332: 727
- Jørgensen KJ, Peter C. Gøtzsche , Túladiagnózis a nyilvánosan szervezett mammográfiai szűrővizsgálatokban: az incidencia trendek szisztematikus áttekintése , BMJ, 2009; 339: b2587
- Zahl PH, Maehlen J, Welch HG, A mammográfiás szűréssel kimutatott invazív emlőrák természeti története , Arch Intern Med, 2008; 168: 2311-6
- [1] .
- "A Methylobacterium baktériumok hibája a rákos emlőszövetben"
- "EverZen: Mi az emlőrák túlélési aránya?"
- a Cabarrot E.-től az emlőrák természetes története. Medico-sebészeti enciklopédia . Tudományos és orvosi kiadások Elsevier SAS, Párizs. Nőgyógyászat, 865-A-10, 2000.
- Gyulladásos emlőrák: kérdések és válaszok az Országos Rák Intézet weboldalán .
- (in) X. Dai , " Mellrák belső altípusának osztályozása, klinikai felhasználás és jövőbeli trendek " , Am J Cancer Res , vol. 5, n o 10,2015. szeptember 15, P. 2929–2943 ( online olvasás ).
- (a) E. Charaffe-JAUFFRET , " Gene Expression profiling breast sejtvonalak azonosított potenciális új bazális markerek " , Oncogene , vol. 25,2006. április 6, P. 2273–2284 ( online olvasás ).
- "Genomikai forradalom" , 1 perc 33 s / 3 perc
- "Célzott terápia 3m39 / 5m33"
- van 't Veer LJ, Dai H, van de Vijver MJ és Als. A génexpresszió-profilozás megjósolja az emlőrák klinikai kimenetelét , Nature, 2002; 415: 530-536
- Paik S, Shak S, Tang G és Als. Multigén vizsgálat a tamoxifennel kezelt, csomópont-negatív emlőrák megismétlődésének előrejelzésére , N Engl J Med, 2004; 351: 2817-2826
- Wang Y, Klijn JG, Zhang Y és Als. Gén-expressziós profilok a nyirokcsomó-negatív primer emlőrák távoli metasztázisának előrejelzésére , Lancet, 2005; 365: 671-679
- Jelentése: MA, Somji S, Lamm DL, Garrett SH, Slovinsky F, Todd JH, jelentése: DA. A metallothionein 3 izoform túlzott expressziója rossz prognózisú mellrákokkal jár . Am J Pathol 159: 21–26, 2001.
- Nartey N, Cherian MG, Banerjee D. immunhisztokémiai lokalizációja metallotionein humán pajzsmirigy daganatok . Am J Pathol 129: 177–182, 1987.
- Haerslev T, Jacobsen K, Nedergaard L, Zedeler K. immunhisztokémiai kimutatását metallotionein a primer emlőrák és hónalji nyirokcsomó-metasztázisok. Pathol Res Pract 190: 675–681, 1994. 64.
- Haerslev T, Jacobsen K, Zedeler K. Az immunhisztokémiailag detektálható metallothionein prognosztikai jelentősége primer emlő karcinómákban. APMIS 103: 279–285, 1995.
- Fresno M, Wu W, Rodriguez JM, Nadji M. A metallotionein lokalizációja mellrákokban. Immunhisztokémiai vizsgálat. Virchows Arch A Pathol Anat Histopathol 423: 215–219, 1993.
- 5. NEMZETKÖZI KONFERENCIA A METALLOTHIONEIN SZIMPÓZIUMPAPÍROKRÓL A metallotionein mint prognosztikai biomarker a mellrákban Boon-Huat Bay, Rongxian Jin, Jingxiang Huang és Puay-Hoon Tan ( „ Összefoglaló ” ( Archívum • Wikiwix • Archívum ?, • Google • Mit • ) (elérhető augusztus 2, 2017 ) és a „teljes PDF cikk (6 oldal) ” ( Archív • Wikiwix • Archive.is • Google • Mit kell tenni? ) (elérhető augusztus 2, 2017 ) )
- Ioachim E, Tsanou E, Briasoulis E, Batsis Ch, Karavasilis V, Charchanti A, Pavlidis N, Agnantis NJ. A hsp27, pS2, katepszin D és metallotionein expressziójának klinikai-patológiai vizsgálata primer invazív emlőrákban . Mell 12: 111–119, 2003.
- Surowiak P, Matkowski R, Materna V, Gyorffy B, Wojna A, Pudelko M, Dziegiel P, Kornafel J, Zabel M. Az invazív ductalis emlőrákban a megemelkedett metallotionein (MT) expresszió megjósolja a tamoxifen-rezisztenciát . Histol Histopathol 20: 1037–1044, 2005.
- [PDF] A Liberális Ápolók Szakszervezeteinek Nemzeti Szervezete honlapja
- Mansel RE, Fallowfield L, Kissin M és mtsai. Randinizált, multicentrikus vizsgálat az őrszemcsomó-biopsziával szemben a standard axilláris kezeléssel operálható emlőrákban: az ALMANAC-vizsgálat , J. Natl Cancer Inst. 98: 599-609
- Erica J Weinstein , Jacob L Levene , Marc S Cohen és Doerthe A Andreae , „ Helyi érzéstelenítők és regionális érzéstelenítés kontra hagyományos fájdalomcsillapítással a tartós műtét utáni fájdalom megelőzésében felnőtteknél és gyermekeknél ”, Cochrane szisztematikus áttekintések adatbázisa ,2018. június 21( ISSN 1465-1858 , PMID 29.926.477 , PMCID PMC6377212 , DOI 10.1002 / 14651858.cd007105.pub4 , olvasható online , elérhető 21 július 2020 )
- (en) Clarke M, Collins R, S Darby et al. „A sugárterápia és a korai emlőrákos műtét mértékének különbségei a helyi kiújulásra és a 15 éves túlélésre: áttekintés a randomizált vizsgálatokról” Lancet 2005; 366: 2087-106
- (en) Henson KE, McGale P, Taylor C, Darby SC. „A szívbetegség és a tüdőrák sugárzással összefüggő mortalitása több mint 20 évvel az emlőrák sugárkezelését követően.” British Journal of Cancer , 2012. december 20. DOI : 10.1038 / bjc.2012.575
- "A rák terhesség alatt kezelhető " (hozzáférés : 2015. október 2. )
- " Mellrák: vérvizsgálat a sugárterápia hatásának előrejelzésére " , a Santé Magazinra (megtekintve : 2016. január 27. )
- (en) Romond EH, Perez EA, Bryant J et al. „Trastuzumab plusz adjuváns kemoterápia operálható HER2-pozitív emlőrák esetén” N Engl J Med. 2005; 353: 1673-84
- " Medscape France - Egészségügyi Információs és erőforrások orvosoknak | Medscape France ” , a francais.medscape.com oldalon (elérhető : 2018. szeptember 4. )
- (hu-GB) John Wiley & Sons Ltd és az Atrium, a déli kapu : „Az Ontruzant elindul, hogy az első Herceptin biohasonlóvá váljon az Egyesült Királyságban | Pharmafile ” , www.pharmafile.com (elérhető : 2018. szeptember 4. )
- (en) Miller K, Wang M, Gralow J et al. „A paclitaxel és a bevacizumab, valamint a paklitaxel önmagában metasztatikus emlőrák esetén” N Engl J Med. 2007; 357: 2666-76.
- A Haute Autorité de Santé (Franciaország) véleményének összefoglalása , 2011. május
- (en) Geyer és mtsai. „Lapatinib plusz kapecitabin a HER2-pozitív fejlett mellrákhoz ” ( Archívum • Wikiwix • Archive.is • Google • Mit kell tenni? ) (Hozzáférés : 2017. augusztus 2. ) N Engl J Med. 2006; 355: 2733-43.
- Az anasztrozol esetében kevesebb az endometrium rákja, kevesebb az agyi érrendszeri ischaemia, kevesebb a mélyvénás trombózis, de több a törés és az arthralgia. Mert letrozol , kevesebb vénás tromboembóliás események, de ízületi fájdalom, törések, szívproblémák, a magas koleszterinszint
- Colditz, GA és Bohlke, K. (2014), Az emlőrák elsődleges megelőzésének prioritásai. CA: Cancer Journal for Clinicians, 64: 186–194. doi: 10.3322 / caac.21225
- IARC Monográfiai Programja a kombinált kombinált fogamzásgátlókat és a monopauzális hormonterápiát rákkeltő anyagnak minősíti , Nemzetközi Rákkutató Ügynökség , 2005. július 29-i sajtóközlemény
- (en) Chavez-MacGregor M Elias SG, Onland-C Moret et al. A posztmenopauzás emlőrák kockázata és a menstruációs ciklusok összesített száma , Cancer Epidemiology Biomarkers & Prevention, 2005; 14: 799-804
- "Mellrák: megelőző kampányokat szerveznek " Le Figaro , 2008. október 23.
- (in) E. Riboli és mtsai. " European Prospective Investigation on Cancer and Nutrition (EPIC)" tanulmányi populációk és adatgyűjtés " Public health Nutrition , vol. 5, n o 6B,2002, P. 1113-1124 ( PMID 12639222 , online olvasás [html] , hozzáférés : 2013. április 16 )
- (in) R. Zamora-Ros és munkatársai: "Az étrendi flavonoid- és lignánbevitel és az emlőrák kockázata a menopauza és a hormonreceptorok státusza a rák és táplálkozás európai prospektív vizsgálata (EPIC) " Mellrák kutatása és kezelése " tanulmányában ,2013( PMID 23572295 , online olvasás [html] , hozzáférés : 2013. április 16 )
- A nők egészséges táplálkozás és életmód (WHEL) tanulmányának következtetése, amelyet 2007 nyarán tettek közzé a JAMA-ban
- Az INSERM által Toursban végzett kísérlet (forrás: Science et Avenir , 2008. április)
- Bevers, Therese B, bizonyítékok a raloxifenre, mint mellrák kockázatának csökkentésére a posztmenopauzás nők számára , JNCCN, 2007; 5: 817-822
- Nelson HD, Smith MB, Griffin JC, Fu R, Gyógyszerek használata az elsődleges emlőrák kockázatának csökkentésére , Ann Intern Med, 2013; 158: 604-614
- (a) Nora E Carbine , Liz Lostumbo Judi Wallace és Henry Ko , " kockázatcsökkentőnek mastectomia megelőzésére primer emlőrák " , Cochrane Database Systematic Reviews ,2018. április 5( PMID 29620792 , PMCID PMC6494635 , DOI 10.1002 / 14651858.CD002748.pub4 , olvasható online , elérhető május 13, 2019 )
- (in) Nicolas Favez , Sarah Kairó Notari , Tania Antonini és Linda Charvoz , " Kötődés és nyomaték elégedettség becsléséhez Expresszált Emotion nők előtt álló mellrák és partnerei a közvetlen műtét utáni időszakban " , British Journal of Health Psychology , repülési. 22, n o 1,1 st február 2017, P. 169–185 ( ISSN 2044-8287 , DOI 10.1111 / bjhp.12223 , online olvasás , hozzáférés: 2017. augusztus 23. )
- " Marie Reno - Rózsaszín október - A hírek teteje - 2019. szeptember 27. - Marie Réno - A hírek teteje a Rire & Chansons - Rire & Chansons " -on, a Rire & Chansons.fr oldalon (elérhető : 2019. október 7. )
Lásd is
Kapcsolódó cikkek
- Mell
- Petefészekrák
- Méh rák
- Mastectomia , protézis
- Mitoxantron
- A kemoterápia utáni kognitív zavar
- Atossa
- DX onkotípus
- Seintinelles
Külső linkek
- Hatósági nyilvántartások :
- Közlemények az általános szótárakban vagy enciklopédiákban : Brockhaus Enzyklopädie • Encyclopædia Britannica
- Egészségügyi források :
- ICD-10 verzió: 2016
- MalaCards
- Országos Rákintézet
- NCI szinonimaszótár
- Orphanet
- (en) Az alapellátás nemzetközi osztályozása
- (en) Betegségek ontológiája
- (en) BetegségekDB
- fr ) Mendeli örökség az emberekben
- fr ) Mendeli örökség az emberekben
- sv) Internetmedicin
- (en + es) MedlinePlus
- (no + nn + nb) Tárolja a medisinske leksikon-t
- Mellrák az egészségbiztosítási weboldalon
- www.cancerdusein.org A „Mellrák Egyesület, Parlons-en! », Október hónap elején Rose felhívta a figyelmet az emlőrák elleni küzdelemre és a korai felismerésre, Franciaországban 1994 óta
- Mellrák a Nemzeti Rákellenes Szövetség honlapján
- A dmoz könyvtár mellrák kategóriája
- GRCS, a montreali CHUM kutatóközpont mellrákkutató csoportja
- Radio Curie Információs webrádió, amely emlőrákban szenvedő nőknek és szeretteiknek szól